
A névoa atmosférica de Titã, A maior lua de Saturno (retratada aqui ao longo da seção mediana de Saturno), é capturado nesta imagem de cor natural (caixa à esquerda). Um novo estudo, que envolveu experimentos na fonte de luz avançada do Berkeley Lab, forneceu novas pistas sobre as etapas químicas que podem ter produzido essa névoa. Crédito:Laboratório de Propulsão a Jato da NASA, Space Science Institute, Caltech
A maior lua de Saturno, Titã, é única entre todas as luas de nosso sistema solar por sua atmosfera densa e rica em nitrogênio, que também contém hidrocarbonetos e outros compostos, e a história por trás da formação dessa rica mistura química tem sido a fonte de alguns debates científicos.
Agora, uma colaboração de pesquisa envolvendo cientistas da Divisão de Ciências Químicas do Laboratório Nacional Lawrence Berkeley do Departamento de Energia (Berkeley Lab) se concentrou em um mecanismo químico de baixa temperatura que pode ter levado à formação de moléculas de anéis múltiplos - os precursores de moléculas mais complexas química agora encontrada na camada de névoa marrom-laranja da lua.
O estudo, co-liderado por Ralf Kaiser na Universidade do Havaí em Manoa e publicado na edição de 8 de outubro do jornal Astronomia da Natureza , vai contra as teorias de que os mecanismos de reação de alta temperatura são necessários para produzir a composição química que as missões de satélite observaram na atmosfera de Titã.
A equipe também incluiu outros pesquisadores do Berkeley Lab, a Universidade do Havaí em Manoa, Universidade Samara na Rússia, e a Florida International University. A equipe usou experimentos de luz ultravioleta a vácuo no Berkeley Lab's Advanced Light Source (ALS), junto com simulações de computador e trabalho de modelagem para demonstrar as reações químicas que contribuem para a química atmosférica moderna de Titã.
"Nós fornecemos evidências aqui para uma via de reação de baixa temperatura que as pessoas não pensaram, "disse Musahid Ahmed, um cientista da Divisão de Ciências Químicas do Berkeley Lab e co-líder do estudo no ALS. "Isso dá origem a um elo perdido na química de Titã."
Titã pode fornecer pistas para o desenvolvimento da química complexa em outras luas e planetas, incluindo a Terra, ele explicou. "As pessoas usam Titã para pensar sobre uma Terra 'pré-biótica' - quando o nitrogênio era mais prevalente na atmosfera da Terra primitiva."
Benzeno, um hidrocarboneto simples com uma estrutura molecular de anel único de seis carbonos, foi detectado em Titã e acredita-se ser um alicerce para moléculas de hidrocarbonetos maiores com estruturas de dois e três anéis que, por sua vez, formou outros hidrocarbonetos e partículas de aerossol que agora constituem a atmosfera de Titã. Essas moléculas de hidrocarbonetos de múltiplos anéis são conhecidas como hidrocarbonetos aromáticos policíclicos (PAHs).
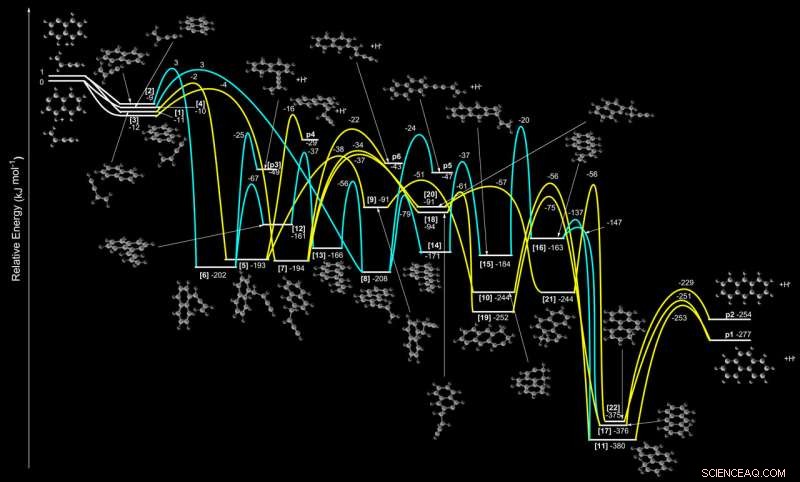
Este gráfico mostra cálculos para superfícies de energia potencial em processos de reação química envolvendo radicais naftilos e gases vinilacetileno. A combinação desses gases pode produzir uma série de compostos, incluindo estruturas moleculares de três anéis. Crédito:Long Zhao, Ralf I. Kaiser, et al., Astronomia da Natureza , DOI:10.1038 / s41550-018-0585-y
No último estudo, pesquisadores misturaram dois gases - um PAH de dois anéis de vida curta conhecido como radical naftilo (C10H7) e um hidrocarboneto chamado vinilacetileno (C4H4) - no ALS, e produziu PAHs de três anéis no processo. Os dois produtos químicos usados para conduzir a reação são considerados existentes em Titã com base no que se sabe sobre a composição química de sua atmosfera.
Os experimentos de ALS eliminaram os produtos finais das reações de uma pequena câmara de reação. Os pesquisadores usaram um detector conhecido como espectrômetro de massa de tempo de vôo de refletor para medir a massa de fragmentos moleculares produzidos na reação dos dois gases. Essas medições forneceram detalhes sobre a química dos PAHs de três anéis (fenantreno e antraceno).
Enquanto os experimentos ALS usaram um reator químico para simular a reação química e um feixe de luz ultravioleta a vácuo para detectar os produtos da reação, cálculos de apoio e simulações mostraram como os produtos químicos formados nos experimentos ALS não requerem altas temperaturas.
Os PAHs, como os produtos químicos estudados no ALS, têm propriedades que os tornam particularmente difíceis de identificar no espaço profundo, Kaiser disse. "Na verdade, nem um único, PAH individual foi detectado na fase gasosa do meio interestelar, "que é o material que preenche o espaço entre as estrelas.
Ele adicionou, "Nosso estudo demonstra que os PAHs são mais amplamente disseminados do que o previsto, uma vez que eles não requerem as altas temperaturas que estão presentes em torno das estrelas de carbono. Prevê-se que este mecanismo que exploramos seja versátil e que leve à formação de PAHs ainda mais complexos. "
E porque os PAHs são considerados precursores para a formação de nuvens moleculares - as chamadas "fábricas moleculares" de moléculas orgânicas mais complexas que podem incluir os precursores da vida como a conhecemos - isso poderia abrir teorias e novos modelos de como o carbono contém o material no espaço profundo e nas ricas atmosferas de planetas e suas luas em nosso sistema solar evoluem e se originam, " ele disse.
Alexander M. Mebel, professor de química na Florida International University e co-líder do estudo, realizou cálculos que mostraram como os reagentes podem naturalmente se juntar e formar novos compostos em temperaturas muito baixas.
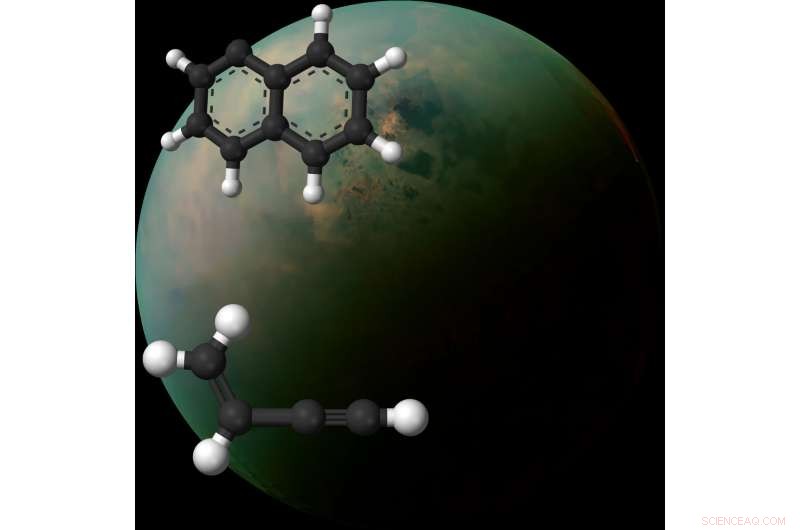
Os cientistas exploraram a química em funcionamento ao combinar dois gases:um composto de estrutura molecular de dois anéis conhecida como radicais naftila (canto superior esquerdo), e o outro composto por um hidrocarboneto denominado vinilacetileno (inferior esquerdo). As esferas brancas representam átomos de hidrogênio e as esferas escuras representam átomos de carbono. Por trás dessas representações moleculares 3D está uma imagem da lua de Saturno, Titã, tomadas pela nave espacial Cassini da NASA. Crédito:Wikimedia Commons, Laboratório de propulsão a jato da NASA, Caltech, Space Science Institute, Laboratório de Física Aplicada da John Hopkins University, Universidade do Arizona
"Nossos cálculos revelaram o mecanismo de reação, "Mebel disse." Nós mostramos que você não precisa de nenhuma energia para conduzir a reação do naftil e do vinilacetileno, portanto, a reação deve ser eficiente mesmo nas condições atmosféricas de baixa temperatura e baixa pressão em Titã. "
Uma chave para o estudo estava na modelagem detalhada da célula do reator onde os gases foram misturados.
Mebel observou que a modelagem das energias e simulações da dinâmica do fluxo de gás em jogo dentro do reator ajudam a monitorar o progresso da reação dentro do reator, e permitiu aos pesquisadores vincular os resultados teóricos às observações experimentais.
O trabalho de modelagem, que ajudou a prever os produtos químicos produzidos nas reações com base nos gases iniciais e na temperatura e pressão da câmara aquecida onde os gases foram misturados e atingidos com o feixe ultravioleta de vácuo, foi liderado pela equipe de pesquisa da Universidade de Samara.
“Esta verificação do modelo, comparando-o com experimentos, can also be helpful in predicting how the reaction would proceed in different conditions—from Titan's atmosphere to combustion flames on Earth."
An aim of the continuing research, Kaiser said, is to unravel the details of how carbon-containing compounds with similar structures to DNA and RNA can develop even in extreme environments.