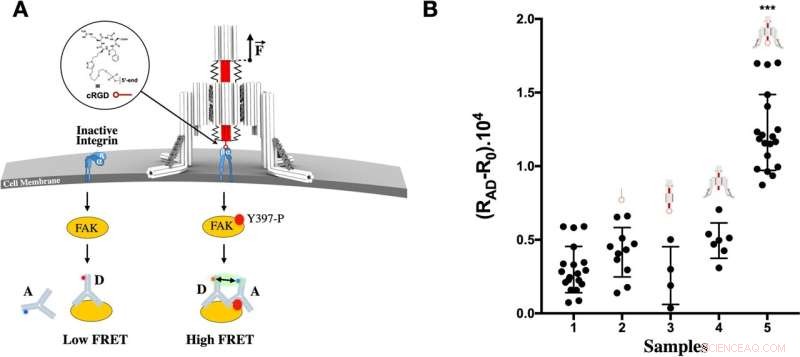
Ativação de nano-guincho de DNA autônomo da sinalização de integrina. A O receptor transmembranar integrina (azul) existe como um heterodímero αβ compacto. As integrinas transmitem tensões mecânicas aplicadas, entre 1 e 15 pN, e recrutam proteínas adicionais para montar adesões focais, incluindo Focal Adhesion Kinase (FAK), que se torna fosforilada no resíduo Y397 após estimulação mecânica da integrina. A adição de dois anticorpos com marcadores doador, D e aceitador, A, permite a detecção de FAK fosforilada em um ensaio LRET. Ambos os anticorpos se ligam a FAK fosforilada (Y397-P) induzindo um sinal LRET alto detectável, enquanto apenas um único anticorpo se liga na ausência de fosforilação produzindo um sinal LRET baixo. As células B MCF-7 em suspensão foram 1, controle não tratado, 2, incubadas com oligonucleotídeo conjugado com RGD, 3, incubadas com origami de pistão-cilindro funcionalizado com cRGD, 4, incubadas com Nano-guinchos não funcionalizados, 5, incubadas com cRGD funcionalizado Nano-guincho. As células foram então lisadas e fosforilação de FAK. O sinal de fundo, R0 , de anticorpos sozinhos foi subtraído do sinal de células lisadas em condições experimentais e de controle calculadas a partir de razões de intensidades de fluorescência do aceitador e doador, RAD . Os resultados são a média de pelo menos três experimentos independentes. As barras de erro representam o desvio padrão, a significância estatística foi determinada por análise de variância unidirecional com comparação com o controle não tratado (***P < 0,001). Crédito:Comunicação da Natureza (2022). DOI:10.1038/s41467-022-30745-2, https://www.nature.com/articles/s41467-022-30745-2
Construir um pequeno robô de DNA e usá-lo para estudar processos celulares invisíveis a olho nu... Você seria perdoado por pensar que é ficção científica, mas na verdade é objeto de séria pesquisa por cientistas do Inserm, CNRS e Université de Montpellier no Structural Biology Center em Montpellier. Este "nano-robô" altamente inovador deve permitir um estudo mais próximo das forças mecânicas aplicadas em níveis microscópicos, que são cruciais para muitos processos biológicos e patológicos. É descrito em um novo estudo publicado na
Nature Communications .
Nossas células estão sujeitas a forças mecânicas exercidas em escala microscópica, desencadeando sinais biológicos essenciais a muitos processos celulares envolvidos no funcionamento normal do nosso corpo ou no desenvolvimento de doenças.
Por exemplo, a sensação do toque é parcialmente condicionada à aplicação de forças mecânicas em receptores celulares específicos (cuja descoberta foi este ano recompensada com o Prêmio Nobel de Fisiologia ou Medicina). Além do tato, esses receptores sensíveis a forças mecânicas (conhecidos como mecanorreceptores) permitem a regulação de outros processos biológicos importantes, como constrição dos vasos sanguíneos, percepção da dor, respiração ou mesmo a detecção de ondas sonoras no ouvido, etc.
A disfunção dessa mecanosensibilidade celular está envolvida em muitas doenças – por exemplo, câncer:as células cancerígenas migram dentro do corpo pelo som e se adaptando constantemente às propriedades mecânicas de seu microambiente. Tal adaptação só é possível porque forças específicas são detectadas por mecanorreceptores que transmitem a informação ao citoesqueleto da célula.
Atualmente, nosso conhecimento sobre esses mecanismos moleculares envolvidos na mecanosensibilidade celular ainda é muito limitado. Várias tecnologias já estão disponíveis para aplicar forças controladas e estudar esses mecanismos, mas elas apresentam uma série de limitações. Em particular, eles são muito caros e não nos permitem estudar vários receptores celulares ao mesmo tempo, o que torna seu uso muito demorado se quisermos coletar muitos dados.
Estruturas de origami de DNA Para propor uma alternativa, a equipe de pesquisa liderada pelo pesquisador do Inserm, Gaëtan Bellot, do Centro de Biologia Estrutural (Inserm/CNRS/Université de Montpellier) decidiu usar o método de origami de DNA. Isso permite a automontagem de nanoestruturas 3D em uma forma pré-definida usando a molécula de DNA como material de construção. Nos últimos dez anos, a técnica permitiu grandes avanços no campo da nanotecnologia.
Isso permitiu que os pesquisadores projetassem um "nano-robô" composto por três estruturas de origami de DNA. De tamanho nanométrico, é, portanto, compatível com o tamanho de uma célula humana. Ele torna possível pela primeira vez aplicar e controlar uma força com uma resolução de 1 piconewton, ou seja, um trilionésimo de Newton - com 1 Newton correspondendo à força de um dedo clicando em uma caneta. Esta é a primeira vez que um objeto baseado em DNA feito por humanos e automontado pode aplicar força com essa precisão.
A equipe começou acoplando o robô a uma molécula que reconhece um mecanorreceptor. Isso possibilitou direcionar o robô para algumas de nossas células e aplicar forças especificamente a mecanorreceptores direcionados localizados na superfície das células para ativá-los.
Tal ferramenta é muito valiosa para a pesquisa básica, pois pode ser utilizada para melhor compreender os mecanismos moleculares envolvidos na mecanosensibilidade celular e descobrir novos receptores celulares sensíveis a forças mecânicas. Graças ao robô, os cientistas também poderão estudar com mais precisão em que momento, ao aplicar a força, as principais vias de sinalização para muitos processos biológicos e patológicos são ativadas em nível celular.
“O projeto de um robô que permite a aplicação in vitro e in vivo de forças de piconewton atende a uma demanda crescente da comunidade científica e representa um grande avanço tecnológico. também pode representar uma fraqueza com sensibilidade a enzimas que podem degradar o DNA. Portanto, nosso próximo passo será estudar como podemos modificar a superfície do robô para que seja menos sensível à ação de enzimas. Também tentaremos encontrar outras modos de ativação do nosso robô usando, por exemplo, um campo magnético", diz Bellot.
+ Explorar mais O que as forças mecânicas por trás do dobramento de proteínas podem nos dizer sobre o câncer metastático
