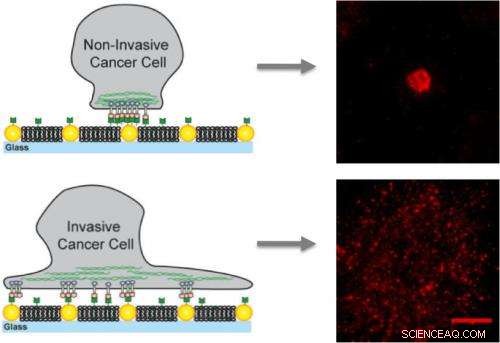
Em membranas artificiais incorporadas com nanopontos de ouro, as células cancerígenas não invasivas ligam-se apenas aos nanopontos e ficam imobilizadas enquanto as células invasivas se ligam à membrana, bem como os nanopontos criando clusters móveis que contribuem para a metástase.
(Phys.org) - Há evidências de que o desenvolvimento e a disseminação do câncer, há muito atribuído à expressão gênica e à sinalização química que deu errado, envolve um componente biomecânico também. Pesquisadores do Laboratório Nacional Lawrence Berkeley (Berkeley Lab) acrescentaram a esse corpo de evidências, demonstrando que a atividade maligna de um sistema de proteína celular crítico pode surgir do que são essencialmente engarrafamentos de proteínas.
Usando uma membrana artificial única imbuída de uma pista de obstáculos de nanopontos de ouro, uma equipe de pesquisa liderada pelo químico Jay Groves estudou o transporte do complexo de sinalização de proteína EphA2 / ephrin-A1 através das superfícies de 10 diferentes linhagens de células de câncer epitelial de mama exibindo uma ampla gama de características de doenças. Os pesquisadores descobriram que o transporte desse complexo receptor-ligante era normal em linhas de células mais saudáveis, mas ficou preso nas linhas de células doentes, com o pior congestionamento ocorrendo nas células que estavam mais doentes.
"Há algo sobre o quão fortemente as proteínas EphA2 estão agrupadas na superfície da célula que está relacionado e pode até contribuir para o comportamento maligno das células cancerosas, "Groves diz." O bloqueio diferencial do transporte de EphA2 entre as várias linhas de células de câncer de mama e sua correlação com as características da doença sugere que o próprio agrupamento de EphA2 pode contribuir para efeitos patológicos. "
Groves tem nomeações conjuntas com a Divisão de Biociências Físicas do Berkeley Lab e com o Departamento de Química da UC Berkeley, e também é investigador do Howard Hughes Medical Institute (HHMI). Ele é o autor correspondente de um artigo que descreve esta pesquisa na revista Nano Letras intitulado "Nanoscale Obstacle Arrays Frustrate Transport of EphA2 / ephrin-A1 Clusters in Cancer Cell Lines." Os co-autores deste artigo foram Theobald Lohmuller e Qian Xu.
O EphA2 pertence a uma família de enzimas que são os principais reguladores dos processos celulares. Efrina-A1 é uma proteína sinalizadora que se liga ao EphA2. Os complexos de EphA2 / efrina-A1 se agrupam em aglomerados que são então transportados pela superfície da célula. A superexpressão de EphA2 foi associada a uma série de cânceres humanos, mas é especialmente proeminente no câncer de mama.
"Cerca de 40 por cento de todos os pacientes com câncer de mama mostram uma superexpressão de EphA2 que está correlacionada com metástases tumorais, consequentemente, muito esforço tem sido direcionado para o desenvolvimento de terapêuticas que visam o EphA2, "Groves diz." No entanto, precisamente o que há de errado com o EphA2 que contribui para o comportamento patológico das células permanece obscuro, já que o EphA2 geralmente não sofre mutação nas células cancerosas. "
Groves é uma autoridade líder no campo emergente da mecanobiologia, que busca entender como as células sentem e respondem às forças mecânicas. Para investigar um possível fator mecânico na ligação do EphA2 ao câncer de mama, Groves usou uma técnica desenvolvida por seu grupo na qual membranas artificiais compostas de uma bicamada fluida de moléculas de lipídios são incorporadas a matrizes fixas de nanopontos de ouro. Isso permite que os pesquisadores controlem o espaçamento ou transporte de proteínas e outras moléculas celulares colocadas nas membranas.
Para este estudo, Groves e seus colegas usaram matrizes de nanopontos de ouro para apresentar obstáculos definidos para o movimento e montagem de clusters EphA2 / efrina-A1. Os ligantes de efrina-A1 podem se ligar à membrana, o que permitiu que os clusters fossem móveis, ou para os nanopontos, que imobilizou os aglomerados, ou para ambos. Os pesquisadores trabalharam com linhas de células de câncer de mama que têm níveis semelhantes de expressão de EphA2 e incluíram MDA-MB-231, uma linha altamente invasiva e tumorigênica, e MCF10A, uma linha relativamente benigna e não tumorigênica.
"Quando vemos células que têm os mesmos níveis de EphA2, mas o MDA-MB-231 está bloqueado enquanto o MCF10A não, então podemos dizer que é algo além dos números de EphA2 que importa, algo sobre a forma como o EphA2 está conectado ao resto da célula que não está relacionado, "Groves diz." Nossas observações sugerem que o citoesqueleto é o culpado e que as drogas que modulam o citoesqueleto também podem modular terapeuticamente o agrupamento de EphA2, reduzindo assim o comportamento patológico. "