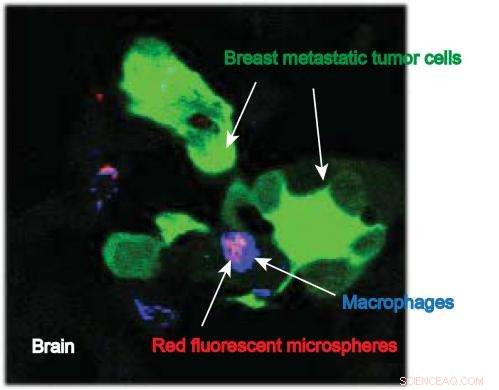
Esta imagem da pesquisadora da IU School of Medicine, Susan Clare, mostra macrófagos carregando nanopartículas (com um corante fluorescente anexado) no local das células tumorais de mama metastáticas no cérebro. Crédito:Susan Clare, M.D., Ph.D.
Um cirurgião de câncer de mama da Escola de Medicina da Universidade de Indiana está desenvolvendo pesquisas que utilizem vidro, ouro, nanotecnologia e mitologia grega na esperança de vencer o câncer de mama que se espalhou para o cérebro.
Susan E. Clare, M.D., Ph.D., professor associado de cirurgia na IU School of Medicine, é o investigador principal iniciador por US $ 573, 000 Subsídio do Departamento de Defesa que permitirá que ela explore uma nova abordagem para administrar terapia para metástases cerebrais de câncer de mama primário.
Assim como os gregos de antigamente, A Dra. Clare espera entregar secretamente "guerreiros" à fortaleza inimiga, neste caso, um tumor cerebral metastático. Sua pesquisa explorará o uso de uma célula do sistema imunológico do corpo para administrar quimioterapia diretamente nas metástases cerebrais. A droga ou outro agente terapêutico é anexado às nanoesferas, que são transportados dentro da célula imune, tanto quanto os soldados eram carregados dentro do Cavalo de Tróia. As células imunes viajam na corrente sanguínea e liberam a droga quando ela atinge o local do tumor.
Os dois tipos de câncer de mama que mais comumente metastatizam para o cérebro são HER2 positivo e triplo negativo. Não há tratamento direcionado especificamente disponível para tratar tumores metastáticos triplo-negativos, mas o lapatinibe é um tratamento padrão para o câncer HER2 positivo que se espalhou para outras partes do corpo.
"O problema de quase todas as drogas, e drogas direcionadas a HER2 não são exceção, é que a barreira hematoencefálica é um impedimento significativo para a administração de terapias em concentrações que podem ser eficazes, "Disse a Dra. Clare. Esse problema biológico levou a Dra. Clare a explorar outros métodos de entrega de drogas para tumores cerebrais metastáticos.
Usando nanopartículas chamadas "nanoconchas, "desenvolvido por Naomi J. Halas, Ph.D., D.Sc., diretor do Laboratório de Nanofotônica da Rice University, A Dra. Clare espera atingir os tumores cerebrais com lapatinibe em uma dose suficiente para interromper a via de sinalização necessária para a proliferação das células cancerosas.
Em um artigo de julho na revista Nanotecnologia do câncer , Drs. Clare, Halas e colegas mostraram que as células imunológicas que carregam as nanopartículas foram capazes de cruzar a barreira hematoencefálica e se estabelecer em metástases cerebrais em um modelo experimental de camundongo.
Primeiro, um componente dos glóbulos brancos chamados macrófagos - células versáteis que iniciam uma resposta imune após infiltração de células anormais (cancerosas) - são coletados. As nanopartículas são ingeridas pelos macrófagos, que são então liberados na corrente sanguínea. Dr. Clare disse que os macrófagos são atraídos para as metástases por quimioatraentes, que são produtos químicos produzidos pelo tumor.
Essas nanopartículas estão em estudos clínicos de Fase I para o tratamento de câncer de cabeça e pescoço, câncer de próstata avançado e câncer de pulmão por meio da Nanospectra Biosciences, baseado em Houston, Texas. Como a barreira hematoencefálica era considerada um impedimento significativo ao parto, a eficácia do tratamento para metástases cerebrais não foi incluída nos testes iniciais. A bolsa do Departamento de Defesa da Dra. Clare permitirá a pesquisa em três áreas principais.
O primeiro objetivo é mostrar que as drogas da quimioterapia podem ser amarradas às nanopartículas e liberadas à vontade no local apropriado no cérebro, Dr. Clare disse. Liberar "à vontade" é fundamental no processo.
"A droga é liberada da partícula ao lançar um laser sobre a partícula, "ela disse." A droga é transportada entre dois pedaços de DNA que são carregados negativamente. Quando exposto à luz do laser, os elétrons mudam da nanopartícula para o DNA, permitindo que ele libere a droga. "
Os macrófagos carregam as nanopartículas diretamente para as células cancerosas, então, quando a droga é liberada, está exatamente onde precisa estar para se difundir para o tumor e interromper a atividade celular das células metastáticas.
Por mais simples que pareça, não é.
A nanopartícula é uma bola de sílica coberta de ouro, que provou ser não tóxico em extensas, estudos científicos de longo prazo. A espessura da casca de ouro determina onde no espectro de luz a luz do laser é absorvida. Para máxima penetração no tecido, as nanopartículas devem absorver luz no infravermelho próximo. As nanopartículas desenvolvidas pelo Dr. Halas fazem exatamente isso.
Contudo, o osso do crânio apresenta um desafio adicional para fornecer potência de laser suficiente para a nanopartícula. Aumentar a potência do laser não é a resposta, pois isso queimará a pele. Existem muitas variáveis para o enigma, mas a Dra. Clare contratou Keith Stantz, Ph.D., professor assistente adjunto de radiologia do Indiana Institute of Biomedical Imaging Sciences, e Jacqueline A. Johnson, Ph.D., professor associado do Instituto Espacial da Universidade do Tennessee, ambos são especialistas em lasers de nanossegundos e femtosegundos. A equipe acredita ter uma solução para o desafio de energia e irá testá-la em modelos de mouse.
"Essa é uma grande peça do quebra-cabeça, "Dr. Clare disse." O ouro é usado como a casca da partícula por causa de suas propriedades físicas. Cálculos precisos para a espessura do ouro, a profundidade de penetração ideal e o poder do laser eram desafios que precisavam ser resolvidos antes que a eficácia do sistema de liberação da droga pudesse ser estudada ”.