
Jennifer Roberts coletou amostras de solo na região de Kongsfjorden de Svalbard, Noruega, que mostrou que genes resistentes a antibióticos foram transferidos para populações de micróbios do solo em um dos locais mais remotos da Terra. Crédito:Jennifer Roberts / KU
O trabalho de um geólogo da Universidade do Kansas no remoto Alto Ártico da Noruega expôs a espantosa disseminação global de micróbios resistentes a antibióticos - incluindo "superbactérias" resistentes a múltiplas drogas - que poderia ter implicações terríveis para a saúde humana em todo o mundo.
Jennifer Roberts, professor e catedrático de geologia da KU, começou investigando a geoquímica microbiana do degelo do permafrost e sua liberação de metano, um poderoso gás de efeito estufa que acelera a mudança climática global.
Mas a análise de acompanhamento das amostras de solo que Roberts coletou na região de Kongsfjorden de Svalbard, Noruega, também mostrou que genes resistentes a antibióticos foram transferidos para populações de micróbios do solo em um dos locais mais remotos da Terra. As descobertas de Roberts e uma equipe internacional de colegas do Reino Unido e da China acabaram de ser publicadas na revista revisada por pares Meio Ambiente Internacional .
"O estudo ofereceu uma boa oportunidade para testar amostras de solo para genes de antibióticos com a hipótese de que Svalbard era um lugar tão remoto e isolado, não encontraríamos nenhuma evidência de tais genes, "Roberts disse." Em contraste, encontramos alguns, incluindo genes resistentes a antibióticos de superbactérias, como o gene de Nova Delhi, que surgiu pela primeira vez na Índia não muito tempo atrás. Isso foi uma surpresa - os genes que encontramos claramente tiveram um curto tempo de transferência entre serem descobertos na Índia e nosso grupo detectá-los no Ártico apenas alguns anos depois. "
A equipe de pesquisa sequenciou geneticamente o DNA de 40 amostras de solo em oito locais em Svalbard, encontrar 131 genes resistentes a antibióticos. Um gene resistente a antibióticos encontrado é chamado blaNDM-1. Detectado inicialmente em Nova Delhi em 2007, o gene desencadeia resistência aos antibióticos carbapenêmicos - um remédio de último recurso para doenças infecciosas que de outra forma seriam intratáveis. A disseminação demonstrada de blaNDM-1, em particular, é altamente preocupante, chamando a atenção para a crise crescente de resistência global aos antibióticos.
Os pesquisadores afirmam que os genes resistentes a antibióticos podem ter percorrido apenas alguns caminhos até o Ártico.
"Eles provavelmente se originaram de patógenos que foram expostos várias vezes a diferentes tipos de antibióticos - é assim que obtemos essas cepas agudamente resistentes a antibióticos, onde eles persistem, mesmo apesar do uso de tratamentos de 'último recurso', "Roberts disse." Alguns dos locais onde encontramos a cepa do gene de Nova Delhi não estão muito longe da principal base de pesquisa, então existe a possibilidade de haver resíduos humanos envolvidos. Também observamos colônias de pássaros em nidificação em locais de baixa altitude, como pequenos lagos e outras fontes de água aberta durante o degelo máximo, e foi aí que vimos as maiores concentrações desses genes. Também os detectamos em lugares que não tinham mar aberto, mas tinham muitos pequenos animais como raposas, e você pode rastrear um vetor entre um bebedouro ou um pequeno lago onde há muitos pássaros e pequenos mamíferos indo beber e, em seguida, pegando quaisquer genes que estejam lá. "
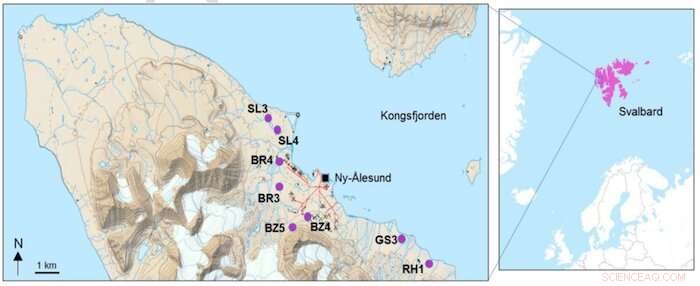
Locais de amostragem dos oito aglomerados de solo em Kongsfjorden e a localização geográfica de Svalbard, Alto Ártico. Crédito:Jennifer Roberts / KU / mapa adaptado do Instituto Polar Norueguês
Roberts, cuja experiência de pesquisa é em hidroquímica e geoquímica microbiana, trabalhou para desenvolver uma referência para genes resistentes a antibióticos encontrados naturalmente em Svalbard para que a equipe pudesse distingui-los de genes multirresistentes "estrangeiros" transferidos para o Ártico de regiões onde os antibióticos são usados em populações humanas e animais para tratar doenças.
"Porque a migração desses genes é uma grande preocupação, a próxima pergunta se torna, 'Esses genes resistentes a antibióticos são nativos - ou foram transferidos?' ", Disse ela." Meu papel foi usar linhas de evidência em nossa pesquisa para nos ajudar a ter clareza sobre o que era um gene nativo que se desenvolveu no solo e o que era trazidos de outras fontes. Fizemos isso observando os suprimentos nutricionais do solo, que são muito, muito baixo nesses solos árticos. Fomos então capazes de ligar os genes resistentes a antibióticos ao que parece ser uma nova fonte de fosfato sendo trazido de fora - e a fonte mais provável de fosfato são as fezes, seja em esgoto humano ou, mais do que provável, pássaro guano. "
De acordo com Roberts, a resistência aos antibióticos viajou entre os micróbios por meio de "transferência lateral de genes". Nesse processo, os patógenos viajam para a água através das fezes, morrer e liberar grandes quantidades de material genético livre na água. Este material genético não se degrada facilmente, com o resultado de que outros organismos acabam pegando os genes - bem como sua resistência.
"Não é que tenhamos algum tipo de comunidade robusta de E. coli ou outro patógeno vivendo nas águas superficiais do Ártico, "Roberts disse." Em vez disso, algum patógeno resistente a antibióticos foi trazido de fontes externas - e agora essa resistência foi dispersada à medida que os genes são captados por outros organismos que já eram populosos no ambiente. "
Roberts disse que a descoberta da equipe mostra que a resistência a antibióticos a múltiplos fármacos é agora de natureza global.
"Temos que lembrar que temos antibióticos, como penicilina, de microrganismos do solo, para começar, "disse ela." Os microrganismos têm usado capacidades de resistência para superar as imunidades no ambiente por muito tempo, produzindo genes resistentes a antibióticos que são considerados naturais e nativos. Mas com o uso de antibióticos manufaturados para humanos e animais em todo o mundo, vimos uma evolução rápida de genes resistentes. Encontramos genes resistentes a antibióticos nativos e evoluídos no Ártico. A preocupação é que, com a resistência se espalhando nessa escala, podemos estar nos aproximando de uma era pós-antibióticos em que nenhum de nossos antibióticos funciona porque os patógenos que estamos tentando combater adquiriram genes resistentes por meio da evolução ou transferência lateral. "
Roberts disse que as descobertas da equipe mostram a importância de uma administração mais cuidadosa do uso de antibióticos e a necessidade de um melhor tratamento das águas residuais em todo o mundo.
"Nosso uso de antibióticos por humanos e animais pode ter impactos que vão além de nós mesmos e de nossas comunidades locais - elas são globais, "Ela disse." É muito importante para nós começarmos a pensar no gerenciamento do sistema de água e no uso de antibióticos de maneiras globais - e começar a reduzir e controlar parte da disseminação que claramente não está controlada no momento. "