Pesquisadores identificam como um aditivo comum aumenta as baterias de íons de lítio
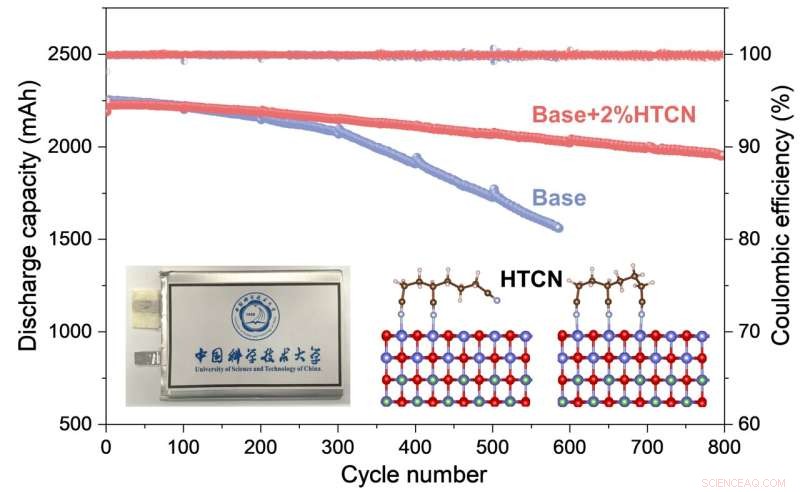
O desempenho eletroquímico e o mecanismo de trabalho do aditivo HTCN em LiCoO de alta tensão2 cátodo para células de bolsa práticas são estudados de forma abrangente. Crédito:Nano Research
Nitrilos – um composto orgânico com um átomo de carbono ligado triplamente a um átomo de nitrogênio – são comumente adicionados à fórmula de eletrólitos para baterias usando um cátodo de óxido de cobalto de lítio, fazendo com que essas baterias cheguem muito mais perto de realizar seu desempenho teórico completo. Até agora, os pesquisadores de baterias não entenderam realmente por que esses nitrilos funcionam dessa maneira. Mas um grupo de eletroquímicos usou técnicas avançadas de microscopia para examinar mais de perto o que acontece na escala molecular e identificar o que está acontecendo, abrindo novos caminhos para melhorias ainda maiores no desempenho da bateria.
O estudo foi publicado na revista
Nano Research em 22 de setembro de 2022 ..
Óxido de cobalto de lítio (LiCoO
2 , ou apenas "LCO") é o material mais usado para cátodos - os eletrodos positivos - em baterias de íons de lítio. Isto é especialmente verdadeiro para baterias usadas em dispositivos eletrônicos portáteis, graças à alta tensão de operação do LCO, sua alta capacidade e estabilidade de seu desempenho a longo prazo.
Mas o que tornou os cátodos LCO particularmente atraentes é que eles oferecem mais energia para uma quantidade menor de espaço (maior densidade de energia), o que é muito útil para dispositivos de consumo menores, como telefones, smartwatches e gadgets que têm restrições de espaço ainda mais rigorosas, como como sensores inteligentes domésticos e industriais.
No entanto, no momento, os cátodos LCO podem fornecer apenas cerca de metade de sua capacidade teórica específica. Isso significa que o que eles realmente entregam é muito menos do que teoricamente deveriam ser capazes de produzir. E, portanto, muitas vezes eles acham difícil atender às crescentes demandas de densidade de energia dos eletrônicos portáteis.
Uma maneira de contornar esse obstáculo seria aumentar a tensão de carga limitada das baterias usando cátodos LCO. A tensão de carga limitada descreve o ponto em que uma bateria é considerada completamente carregada. Além desse ponto, a bateria pode ser danificada e muitos dispositivos simplesmente desligam quando o limite de corte é atingido. Esse limite é definido de forma um tanto arbitrária e, portanto, pode ser aumentado, e essa operação de alta tensão oferece a promessa de aumentar a densidade de energia dessas baterias.
Mas aqui surge um novo problema:a operação de alta tensão pode exacerbar reações químicas prejudiciais na interface entre o cátodo e o eletrólito. Isso pode resultar em rachaduras e outros danos internos, que por sua vez podem deteriorar ainda mais a interface entre os eletrodos. Em última análise, tudo isso pode resultar em um declínio radical na capacidade da bateria e um aumento acentuado nos problemas de segurança. A temperatura de trabalho nesses dispositivos pode atingir 45℃ devido à sua própria geração de calor, reduzindo ainda mais a vida útil da bateria.
E assim, há algum tempo, misturando compostos adicionais à fórmula do eletrólito para ajustar a atividade de reação do eletrólito (o meio contendo íons que ajuda a estabelecer uma corrente através do movimento de íons positivos e negativos através dele) na interface entre o cátodo e eletrólito provou ser uma estratégia muito eficaz para diminuir a atividade da reação eletrolítica.
Existem vários compostos diferentes usados como aditivos eletrolíticos, mas para baterias de íons de lítio, os nitrilos são talvez os mais amplamente utilizados. Nitrilos são qualquer composto orgânico que tem uma seção da molécula (um grupo funcional) composta de um átomo de carbono ligado triplamente a um átomo de nitrogênio.
No entanto, o mecanismo de trabalho dos aditivos nitrílicos em cátodos de alta tensão ainda não é totalmente compreendido, particularmente no tipo de baterias de bolsa LCO de alta tensão práticas e cotidianas. (As baterias de bolsa são um tipo de bateria "soft" sem uma caixa de metal duro e, em vez disso, cujos componentes são fechados em um filme plástico revestido de alumínio, parecendo um pouco com uma "bolsa" de goma de mascar ou tabaco solto. Desenvolvido pela primeira vez em 1995 e permitindo um uso muito mais eficiente do espaço, as baterias de bolsa tornaram-se uma escolha comum para os fabricantes devido a essa vantagem de design.)
Existem duas teorias principais que tentam explicar o mecanismo dos aditivos nitrílicos, mas ambas apresentam deficiências significativas em seu poder explicativo.
"Os nitrilos funcionam bem, mas não sabemos realmente por que eles funcionam bem, por que essa ação estabilizadora está ocorrendo. Exatamente o que está acontecendo permanece bastante misterioso", disse Shuhong Jiao, eletroquímico da Universidade de Ciência e Tecnologia da China. (USTC). “E se não soubermos por que o que estamos fazendo para melhorar as baterias está funcionando, isso nos impede de ajustar nossos esforços para melhorar ainda mais as coisas”.
Assim, os pesquisadores usaram um aditivo eletrolítico de nitrila comum, o ligante tridentado contendo 1,3,6-hexanotricarbonitrila (ou mais simplesmente HTCN) para tentar esclarecer qual é o mecanismo das nitrilas na estabilização de alta tensão de um LiCoO
2 cátodo.
Enquanto a bateria estava operando e superando em muito um equivalente sem os aditivos eletrolíticos HTCN, os pesquisadores usaram microscopia eletrônica para observar mais de perto o que estava acontecendo, combinado com uma análise do íon e da composição elementar do sistema. Eles descobriram que o aditivo HTCN estava inibindo muito efetivamente a geração de rachaduras e a dissolução de íons de cobalto.
Então, usando espectroscopia de fotoelétrons de raios-X combinada com uma série de cálculos teóricos, eles descobriram que as moléculas de HTCN estavam sendo eficientemente adsorvidas na superfície do LCO e incorporadas na interface entre o cátodo e o eletrólito, que em por sua vez, inibem grandemente uma reação de oxidação na superfície do LCO, evitando assim uma decomposição contínua do eletrólito.
Ao todo, isso equivale a uma interface muito mais estável entre o cátodo e o eletrólito, o que suprimiu significativamente a decomposição de componentes e a formação de rachaduras. É esta estrutura catodo-eletrólito estável e densa que aumenta a estabilidade da bateria através de muitos ciclos de carga e descarga.
Conhecendo essa compreensão em nível molecular de como os aditivos nitrílicos dão um impulso a essas baterias, os pesquisadores agora podem procurar outras formulações de aditivos eletrolíticos que produzam uma estrutura de interface semelhante ou melhor.
+ Explorar mais Os aditivos químicos melhoram a estabilidade das baterias de íons de lítio de alta densidade
