Catalisadores de nanocarbono monolítico inicializam a oxidação seletiva de sulfeto de dihidrogênio
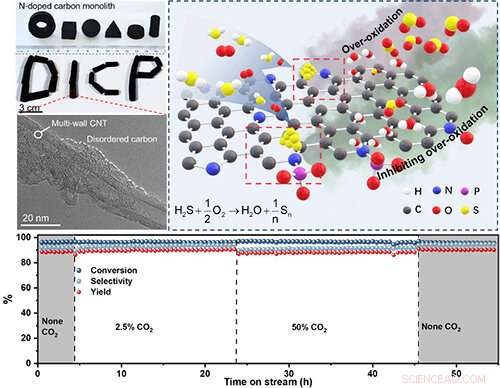 p O catalisador de nanocarbono monolítico apresenta desempenho catalítico superior para oxidação seletiva de H2S com seletividade de enxofre aprimorada e tolerância a impurezas. Crédito:XU Chi
p O catalisador de nanocarbono monolítico apresenta desempenho catalítico superior para oxidação seletiva de H2S com seletividade de enxofre aprimorada e tolerância a impurezas. Crédito:XU Chi
p Remoção ultra-profunda de H
2 S é importante no refino de petróleo, purificação de gás natural e indústria química de carvão. Contudo, os catalisadores industriais para H contínuo
2 A oxidação seletiva de S mostra baixa atividade e estabilidade, especialmente em gás de alimentação contendo vapor e gás de impureza. p Recentemente, Assoc. O grupo do Prof. Liu Yuefeng do Instituto de Física Química de Dalian (DICP) da Academia Chinesa de Ciências (CAS) fabricou compósitos monolíticos de nanocarbono para remoção contínua de alta concentração de H
2 S, apresentando maior seletividade e estabilidade do produto sob alta concentração de O
2 , CO
2 e vapor.
p Este trabalho foi publicado em
Catálise ACS em 30 de junho.
p Os materiais de nanocarbono possuem propriedades químicas de superfície únicas e excelente desempenho catalítico. Contudo, os locais hiperativos e as características exotérmicas da reação podem causar superoxidação do produto em SOX.
p Os pesquisadores alcançaram alta seletividade de enxofre para a oxidação seletiva de H
2 S sem perder a conversão por carbocatalisadores monolíticos mesoporosos 3D dopados com N dopados com fosfato (N-C / CNT), levando a uma alta taxa de formação de enxofre.
p O monólito N-C / CNT modificado por P exibiu alta estabilidade, mesmo em ambientes severos de reação com CO
2 , O
2 , Steam e SO
2 , indicando o potencial promissor para aplicação prática.
p Combinando métodos avançados de caracterização (XPS, TPD), análise cinética e cálculo teórico, os pesquisadores descobriram que a interação entre o grupo P e o local da piridina, que era o centro ativo, poderia moderar a adsorção e atividade de O
2 no site ativo, evitando assim a ocorrência de sobrexidação e melhorando a seletividade do produto.
