 p Crédito:Universidade de Tecnologia de Viena
p Crédito:Universidade de Tecnologia de Viena
p Se o CO
2 o conteúdo da atmosfera não deve aumentar mais, o dióxido de carbono deve ser convertido em outra coisa. Contudo, como CO
2 é uma molécula muito estável, isso só pode ser feito com a ajuda de catalisadores especiais. O principal problema com tais catalisadores até agora tem sido sua falta de estabilidade:depois de um certo tempo, muitos materiais perdem suas propriedades catalíticas. p Na TU Wien, a pesquisa está sendo conduzida em uma classe especial de minerais - os perovskitas, que até agora têm sido usados para células solares, como materiais anódicos ou componentes eletrônicos, e não por suas propriedades catalíticas. Agora, os cientistas da TU Wien conseguiram produzir uma perovskita especial que é perfeitamente adequada como um catalisador para a conversão de CO
2 em outras substâncias úteis, como os combustíveis sintéticos. O novo catalisador de perovskita é muito estável e também relativamente barato, portanto, seria adequado para uso industrial.
p
Como fechar o ciclo do carbono
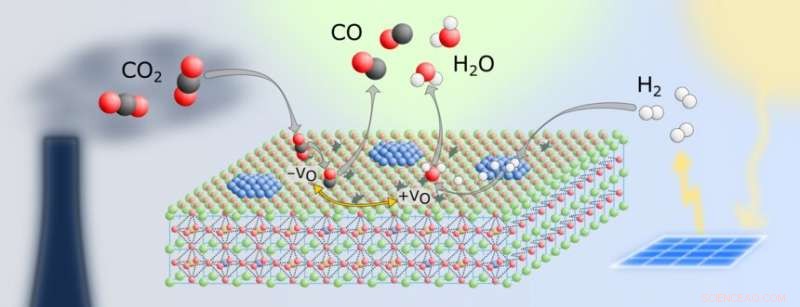
p "Estamos interessados na chamada reação reversa de deslocamento água-gás, "diz o Prof. Christoph Rameshan do Instituto de Química de Materiais da TU Wien." Neste processo, dióxido de carbono e hidrogênio são convertidos em água e monóxido de carbono. Você pode então processar o monóxido de carbono ainda mais, por exemplo em metanol, outros materiais de base química ou mesmo em combustível. "
p Esta reação não é nova, mas não foi realmente implementado em escala industrial para CO
2 utilização. Acontece em altas temperaturas, o que contribui para o fato de que os catalisadores se quebram rapidamente. Este é um problema particular quando se trata de materiais caros, como os que contêm metais raros.
p Christoph Rameshan e sua equipe investigaram como adaptar um material da classe de perovskitas especificamente para essa reação, e ele teve sucesso:"Nós tentamos algumas coisas e finalmente chegamos a uma perovskita feita de cobalto, ferro, cálcio e neodímio que tem excelentes propriedades, "diz Rameshan.
p
Átomos migrando através do cristal
p Por causa de sua estrutura cristalina, a perovskita permite que certos átomos migrem através dela. Por exemplo, durante a catálise, átomos de cobalto do interior do material viajam para a superfície e formam pequenas nanopartículas lá, que são particularmente quimicamente ativos. Ao mesmo tempo, os chamados vazios de oxigênio se formam - posições no cristal onde um átomo de oxigênio deveria realmente estar. É precisamente nessas posições vagas que o CO
2 moléculas podem se encaixar particularmente bem, para então ser dissociado em oxigênio e monóxido de carbono.
p "Pudemos mostrar que nossa perovskita é significativamente mais estável do que outros catalisadores, "diz Christoph Rameshan." Ele também tem a vantagem de poder ser regenerado:se sua atividade catalítica diminuir após um certo tempo, você pode simplesmente restaurá-lo ao seu estado original com a ajuda de oxigênio e continuar a usá-lo. "
p Avaliações iniciais mostram que o catalisador também é economicamente promissor. "É mais caro do que outros catalisadores, mas apenas por um fator de três, e é muito mais durável, "diz Rameshan." Gostaríamos agora de tentar substituir o neodímio por outra coisa, o que poderia reduzir ainda mais o custo. "
p
A planta industrial com produção de combustível embutida
p Teoricamente, você poderia usar essas tecnologias para obter CO
2 fora da atmosfera, mas para fazer isso você primeiro teria que concentrar o dióxido de carbono, e isso requer uma quantidade considerável de energia. Portanto, é mais eficiente primeiro converter CO
2 onde é produzido em grandes quantidades, como em plantas industriais. "Você poderia simplesmente adicionar um reator adicional às usinas existentes que atualmente emitem muito CO
2 , em que o CO
2 é primeiro convertido em CO e, em seguida, processado posteriormente, "diz Christoph Rameshan. Em vez de prejudicar o clima, tal planta industrial geraria então benefícios adicionais.
