
Usando química computacional, estudante de graduação Vindi M. Jayasinghe-Arachchige e Rajeev Prabhakar, professor de química, projetou uma nova molécula que poderia avançar significativamente no estudo e no uso de enzimas. Crédito:Jenny Hudak / Universidade de Miami
As enzimas são a força motriz da natureza. Encontrado nas células de todos os animais, plantas, e todos os outros organismos vivos, eles aceleram as reações químicas que desencadeiam milhares de funções biológicas - desde a formação de neurônios até a digestão dos alimentos.
Eles realizam seus trabalhos tão seletivamente e tão rapidamente - milhões de vezes mais rápido do que um piscar de olhos - que o campo da química biomimética surgiu nas últimas décadas com o objetivo de projetar enzimas artificiais que podem imitar os poderes das enzimas naturais em ambientes industriais. Enzimas artificiais podem, por exemplo, converter milho em etanol ou ajudar a criar novos medicamentos mais rapidamente, barato, e de forma eficaz.
Indo um passo mais perto de alcançar esse objetivo, Rajeev Prabhakar, um químico computacional da Universidade de Miami, e seus colaboradores da Universidade de Michigan criaram um romance, sintético, molécula de três fitas que funciona como uma metaloenzima natural, ou uma enzima que contém íons metálicos.
"Não estava claro se eles poderiam ser feitos, mas nós os fizemos. E, então nós os usamos para catalisar reações com sucesso, "disse Prabhakar, um professor de química que estuda reações enzimáticas na esperança de projetar seus análogos artificiais. "Este é um passo incremental, mas importante no desenvolvimento de enzimas artificiais, que há muito é considerado o Santo Graal da química. Infelizmente, tão boas quanto as enzimas naturais funcionam em nossos corpos e outras formas de vida, eles não toleram muito bem outras configurações. Eles também são muito caros e não são fáceis de preparar e purificar. "
Por seu estudo inovador publicado em Química da Natureza esta semana, Prabhakar e o estudante de graduação Vindi M. Jayasinghe-Arachchige uniram forças com Vincent L. Pecoraro, um professor de química da Universidade de Michigan, para melhorar o desempenho das enzimas artificiais em que o laboratório de Pecoraro foi pioneiro ao longo dos anos. Os pesquisadores de Michigan já haviam criado metaloenzimas sintéticas mais simples que catalisaram com sucesso uma série de reações químicas. Mas essas macromoléculas artificiais foram projetadas com três idênticas, ou fitas "homotriméricas" simétricas, que, Prabhakar disse, limitaram suas habilidades catalíticas.
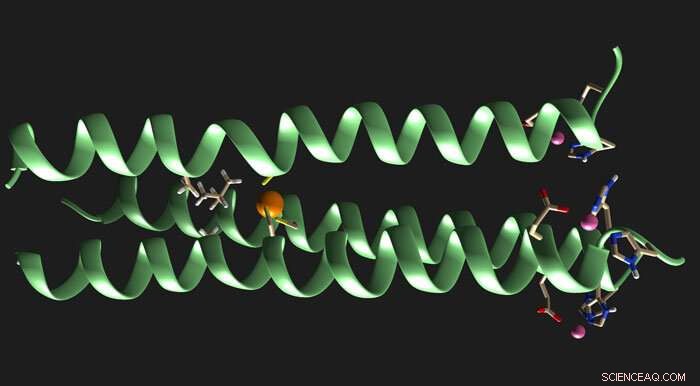
Crédito:Universidade de Miami
Na nova molécula, que Jayasinghe-Arachchige projetou no supercomputador da Universidade de Miami com a orientação de Prabhakar, a terceira fita difere em estrutura das outras duas fitas. Seus cálculos de mecânica quântica mostraram que quanto mais complexo, não simétrico, estrutura de três fios, conhecido como uma bobina "heterotrimérica", expandiu o desempenho catalítico de metaloenzimas artificiais homotriméricas - uma descoberta que Pecoraro e sua equipe confirmaram com experimentos em seu laboratório em Michigan.
"Nossas técnicas são diferentes, mas complementar, "Prabhakar disse." O que nós fazemos, o grupo Pecoraro não pode fazer, e o que eles fazem, não podemos fazer. Modelamos moléculas no computador para que possamos prever suas propriedades estruturais e o mecanismo de suas formações. Eles usam nossos modelos para construir a coisa real, e, neste caso, esse é o primeiro exemplo de uma molécula heterotrimérica natural. "
A maioria dos leigos provavelmente consideraria o estudo tão incompreensível quanto seu título:"Bobinas espiraladas de três fios heteroméricas projetadas usando uma estratégia mediada por modelo Pb (II) (Cys) 3." Mas o resultado final, Prabhakar disse, é que a pesquisa colaborativa conduzida em Miami e Michigan abre as portas para uma nova estratégia para alcançar a criação de enzimas artificiais que funcionam tão bem quanto as enzimas naturais.
Além do Pecocaro, Prabhakar, e Jayasinghe-Arachchige, outros co-autores do estudo incluem o ex-aluno de graduação de Prabhakar, Thomas J. Paul, agora na Universidade de Michigan; Audrey E. Tolbert, Catherine S. Ervin, e Kosh P. Neupane, também da Universidade de Michigan; e Leela Ruckthong, da King Mongkut's University of Technology, Na Tailândia.
Agora em seu último ano de estudo para seu doutorado em química, Jayasinghe-Arachchige disse que continua fascinada com os avanços nas técnicas de química computacional que lhe permitiram modelar as estruturas químicas e reações da nova molécula.
"Estou animado com o fato de que nossas descobertas criarão novos caminhos para o desenvolvimento de enzimas artificiais eficientes que podem ser usadas para melhorar a qualidade de vida, '' disse Jayasinghe-Arachchige, "e como uma mulher em um campo onde as mulheres estão sub-representadas, Espero que este estudo motive as mulheres a ingressar no fascinante mundo dos campos STEM. "