Crédito:RUDN University
Um químico da Universidade RUDN descobriu quatro novos compostos estáveis que podem ser obtidos na reação de iodo com iodeto de metilamônio - o uso dessas substâncias permitirá a produção de painéis solares de perovskita sem reagentes tóxicos e evitará subprodutos durante a fabricação. O artigo foi publicado no The Journal of Physical Chemistry Letters .
As perovskitas híbridas à base de chumbo são usadas em células solares modernas como uma camada de absorção de luz. Mas eles são instáveis à umidade, e as tecnologias existentes requerem o uso de soluções e solventes tóxicos. Isso complica a tecnologia e a torna potencialmente perigosa.
A solução para o problema pode ser métodos sem solvente, isso é, o uso de fundidos em vez de soluções - por exemplo, aplicar um poliiodeto fundido a uma fina película de chumbo metálico. Contudo, existem poucos estudos confiáveis sobre a química do poliiodeto. Os pesquisadores estudaram as propriedades do metilamônio (CH 3 NH 3 ) e compostos de iodo para encontrar variantes de compostos adequados para uso na produção de células solares de perovskita.
Os compostos do sistema iodeto de metilamônio (MA) e iodo derretem à temperatura ambiente e formam líquidos iônicos - fundidos que são compostos exclusivamente de íons. Esses líquidos precursores podem ser aplicados uniformemente em grandes superfícies, trazendo a produção industrial de células solares modulares baseadas em perovskitas híbridas para o mercado comercial.
Os líquidos à base de poliiodetos fundem à temperatura ambiente apenas na presença de grandes cátions orgânicos na composição. O químico Victor Khrustalev da Universidade RUDN explicou essa diferença pelo fato de o cátion metilamônio ter um grande momento de dipolo e ser capaz de formar um grande número de ligações de hidrogênio. Em pequenos tamanhos de cátions, isso leva a um aumento da entropia durante o derretimento, o que reduz a temperatura de fusão.
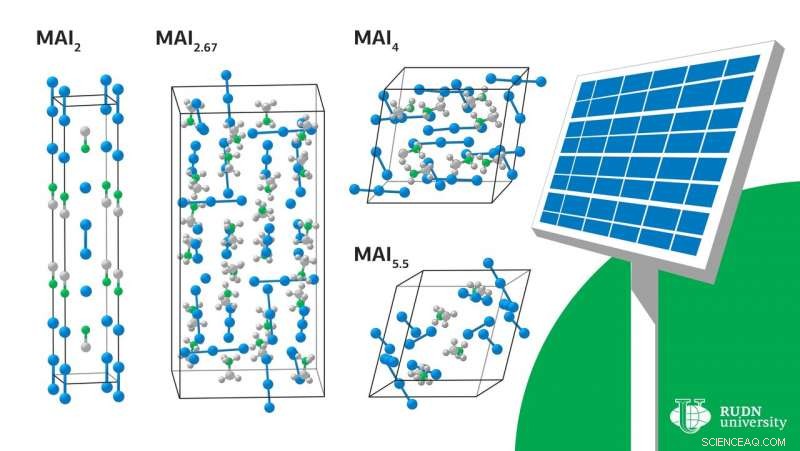
Sob certas condições, cristais de várias composições começam a evoluir do líquido - MAI 2 , MAI 2,67 , MAI 4 и MAI 5,5 . Para determinar as condições sob as quais existe um derretimento, os cientistas realizaram um cálculo teórico da entalpia e da entropia de formação desses cristais. Para todos os compostos, exceto MAI 2 , a reação de obtenção de um composto com menor teor de iodo dependia exclusivamente da contribuição da entropia. Os químicos explicaram que o aumento da entalpia durante a transição para compostos com maior teor de iodo é devido ao enfraquecimento da interação dos cátions com os ânions devido à distribuição de uma pequena carga negativa em um grande ânion poliiodeto. Um aumento semelhante na entropia é devido à complexidade dos poliânions e ao enfraquecimento das ligações entre eles.
Esses dados termodinâmicos nos permitiram definir e generalizar os valores experimentais dos limites em que o fundido pode existir.
Os químicos também descobriram que tais efeitos ocorrem em compostos semelhantes com o cátion formamidina (FA
+
=HC (NH 2 ) 2 ) e polibrometos. Além disso, a composição mista (MABr 3 ) 0,15 (FAI 3 ) 0,85 demonstra propriedades de líquido iônico de -40 a 80 ° C. Tal baixo ponto de fusão do precursor é favorável para a obtenção de filmes finos de perovskitas híbridas mistas que demonstram propriedades máximas de absorção de luz.