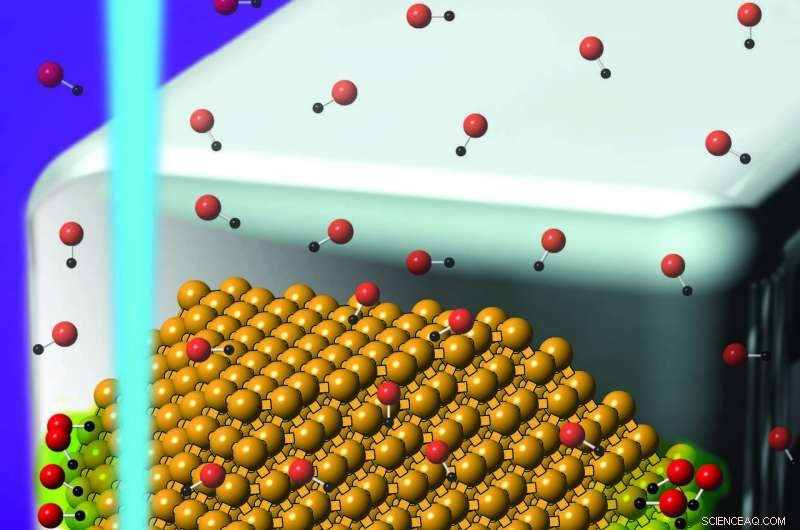
A ilustração mostra a localização de uma reação química em nanopartículas de ouro mediada por plasmons de superfície localizados - oscilações de grupos de elétrons na superfície da nanopartícula. Os plasmons (verdes) atuam como catalisadores que permitem a reação, em que pares de monóxido de carbono (linhas brancas) se transformam em átomos de carbono (vermelho) e oxigênio (preto) à temperatura ambiente. As bolas de ouro representam as nanopartículas de ouro. Crédito:K. Dill / NIST
Os pesquisadores do NIST exploraram com detalhes sem precedentes uma nova geração de catalisadores que permitem algumas reações químicas, que normalmente requerem alto calor, para prosseguir à temperatura ambiente. Os catalisadores de economia de energia usam luz solar ou outra fonte de luz para excitar plasmons de superfície localizados (LSPs) - oscilações de grupos de elétrons na superfície de certas nanopartículas de metal, como ouro, prata e alumínio. A energia derivada das oscilações LSP impulsiona reações químicas entre as moléculas que aderem às nanopartículas.
Os cientistas já haviam mostrado que o hidrogênio molecular pode ser dividido em seus átomos individuais pela energia gerada pelas oscilações LSP. A equipe do NIST descobriu agora uma segunda reação mediada por LSP que ocorre em temperatura ambiente. Nesta reação, LSPs excitados em nanopartículas de ouro transformam duas moléculas de monóxido de carbono em carbono e dióxido de carbono. A reação, que normalmente requer uma temperatura mínima de 400 graus C., desempenha um papel importante na conversão de monóxido de carbono em materiais amplamente utilizados à base de carbono, como nanotubos de carbono e grafite.
Sondar as nanopartículas com um feixe de elétrons e combinar os dados com simulações, os pesquisadores do NIST identificaram os locais nas nanopartículas de ouro onde ocorreram as reações. Eles também mediram a intensidade dos LSPs e mapearam como a energia associada às oscilações variava de um lugar para outro dentro das nanopartículas. As medições são etapas fundamentais para a compreensão do papel dos LSPs para iniciar reações em temperatura ambiente, mitigando a necessidade de aquecer as amostras.
Wei-Chang Yang do NIST e da University of Maryland NanoCenter, junto com Henri Lezec e Renu Sharma e outros colaboradores, descrever seu trabalho no dia 15 de abril Materiais da Natureza .
Os cientistas confiaram em depósitos de depósitos de carbono sólido - um dos produtos da reação de monóxido de carbono que estudaram - como marcadores para as localizações exatas nas nanopartículas de ouro onde a reação ocorreu. A equipe descobriu que a reação se concentrava na interseção onde as moléculas do gás monóxido de carbono aderem preferencialmente às nanopartículas de ouro e onde a amplitude do campo elétrico associado aos LSPs era mais alta. Embora muitos LSPs possam ser excitados com a luz do sol, a equipe escolheu um feixe de elétrons para disparar as oscilações e estudou a reação do monóxido de carbono em um microscópio eletrônico de transmissão de varredura que pode operar em um ambiente à temperatura ambiente.
As evidências, diz Sharma, lançar a base para a busca de outros sistemas que aproveitem diretamente a luz solar para gerar LSPs em nanopartículas para conduzir reações químicas em temperatura ambiente. Ao reduzir o consumo de energia, tais sistemas podem ter um enorme impacto na indústria e no meio ambiente.