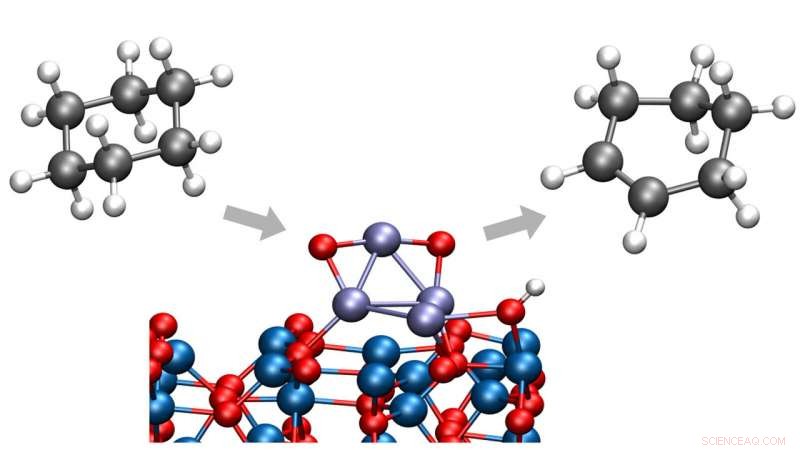
Os químicos de Argonne identificaram uma maneira de converter ciclohexano em ciclohexeno ou ciclohexadieno, ambos importantes produtos químicos em uma ampla gama de processos industriais. O novo processo ocorre em baixas temperaturas, eliminando a criação de subprodutos indesejados. Crédito:Laboratório Nacional de Argonne
Os químicos gastam muito tempo e energia tentando fazer com que as reações químicas comecem ou se acelerem - mas às vezes pode ser tão importante pará-las antes que vão longe demais.
Em um estudo recente do Laboratório Nacional de Argonne do Departamento de Energia dos EUA (DOE), químicos identificaram uma maneira de converter ciclohexano em ciclohexeno ou ciclohexadieno, produtos químicos importantes em uma ampla gama de processos industriais. Mais importante, este processo ocorre em baixas temperaturas, eliminando a criação de dióxido de carbono que teria resultado de uma quebra indesejada das ligações carbono-carbono.
O ciclohexano é uma molécula inicial importante em uma ampla gama de reações químicas, de acordo com o químico de Argonne Stefan Vajda, agora no J. Heyrovský Institute of Physical Chemistry em Praga. Contudo, sem um catalisador adequado para iniciar a reação, converter ciclohexano em produtos úteis normalmente requer temperaturas elevadas geradas por meio do gasto de uma grande quantidade de energia, e o processo também pode sofrer de baixa seletividade.
No estudo, O químico Larry Curtiss de Vajda e Argonne e sua equipe internacional de colaboradores examinaram um tipo de reação chamada desidrogenação oxidativa, em que as moléculas de hidrogênio são removidas de uma molécula maior. Cortando um número limitado de ligações hidrogênio-carbono, a reação pode produzir ciclohexeno e ciclohexadieno antes que a combustão para dióxido de carbono ocorra.
O trabalho melhorou os estudos anteriores da equipe de Argonne sobre a desidrogenação de ciclohexano e ciclohexeno, introduzindo dois componentes principais:um catalisador de óxido de cobalto de tamanho sub-nanômetro em um suporte de óxido de alumínio e um ambiente de oxigênio controlado.
Os pesquisadores empregaram técnicas de espalhamento de raios-X na Fonte Avançada de Fótons de Argonne (APS), um DOE Office of Science User Facility, para monitorar a natureza e estabilidade dos catalisadores durante o teste catalítico dos clusters em tempo real. Eles descobriram que os aglomerados realizavam a desidrogenação parcial do ciclohexano em temperaturas em torno de 100 graus Celsius - muito mais baixas do que havia sido observado anteriormente para este tipo de reação, e os aglomerados mantiveram sua natureza oxidada e estabilidade em temperaturas de reação de até 300 ° C.
"O fato de podermos fazer essa conversão acontecer em temperaturas mais baixas protege os produtos intermediários de desidrogenação ciclohexeno e ciclohexadieno de serem posteriormente convertidos em produtos indesejados, "Vajda disse.
Vajda e Curtiss observaram que o catalisador altamente seletivo tem vida longa e não é envenenado ou degradado pela reação. Na investigação teórica e experimental do tamanho do catalisador, os pesquisadores descobriram que os aglomerados de tamanho quatro e vinte e sete átomos eram quase igualmente eficientes na realização da reação. "Parece que, desde que o catalisador tenha menos de um nanômetro de tamanho, esta composição funciona bem - um fator importante para o aumento de escala potencial desta classe de catalisadores por mais tradicional, embora menos seletivo em relação ao tamanho, rotas de síntese. "Vajda disse.
Para entender melhor os mecanismos básicos por trás da atividade e seletividade dos catalisadores de cobalto, os pesquisadores usaram cálculos da teoria funcional da densidade para modelar as vias de reação. "O excelente desempenho dos aglomerados de cobalto pode ser explicado por cálculos teóricos, que revelam átomos de cobalto altamente ativos nos aglomerados e mostram que a natureza oxidada dos aglomerados causa a formação do produto a baixa temperatura, "Curtiss explicou.