Crédito:Angewandte Chemie
Ligar moléculas terapeuticamente ativas a anticorpos específicos pode ajudar a conduzi-los até seus alvos designados e minimizar os efeitos colaterais - especialmente no tratamento de tumores. No jornal Angewandte Chemie , os cientistas já descreveram novos conjugados feitos de anticorpos e um inibidor da proteína do fuso da cinesina. Alterar o ligante entre os dois componentes permite ajustar a atividade desta droga citostática, que é eficaz contra uma ampla gama de cânceres.
Os medicamentos precisam ser altamente eficazes, mas relativamente livre de efeitos colaterais. Isso é particularmente importante no tratamento do câncer, porque as drogas citostáticas usadas interferem nos mecanismos de regulação de todas as células do corpo, causando sintomas como comprometimento das defesas imunológicas, perda de cabelo, e náusea. Os tratamentos, portanto, visam introduzir drogas citostáticas diretamente nas células tumorais antes de desencadear seu efeito tóxico. Uma das maneiras de se conseguir isso é anexar essas pequenas moléculas de fármaco a um anticorpo para fazer um conjugado. O componente de ponte, chamado de linker, deve manter o conjugado junto enquanto ele circula no sangue. O anticorpo liga-se especificamente a locais de ligação (antígenos) que são especialmente numerosos nas superfícies das células tumorais alvo. A ancoragem do anticorpo desencadeia a captação do conjugado dentro das células cancerosas. Lá, a droga é liberada por enzimas para realizar sua tarefa destrutiva especificamente na célula cancerosa. As células saudáveis permanecem praticamente inalteradas.
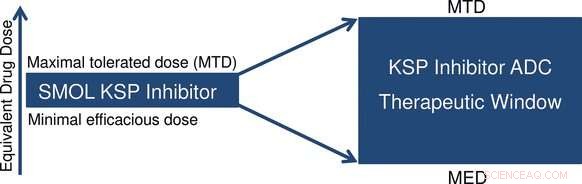
O número de drogas citostáticas que foram incorporadas com sucesso em tais conjugados de anticorpos tem sido limitado até agora. Pesquisadores liderados por Hans-Georg Lerchen (Bayer AG) agora tentaram isso com uma citotoxina que usa um mecanismo diferente dos medicamentos citostáticos clássicos para atacar o ciclo celular. É um novo inibidor da proteína do fuso da cinesina à base de pirrol (KSP). KSP desempenha um papel fundamental na separação do centrossoma durante a divisão celular. O bloqueio desta etapa causa um forte efeito antitumoral. Mesmo doses muito baixas do inibidor foram altamente eficazes contra uma ampla gama de linhas de células cancerosas. Lerchen e seus colegas de trabalho demonstraram que essa técnica pode ser usada para fazer conjugados de anticorpos altamente ativos. O uso de diferentes anticorpos permite que eles atinjam uma variedade de tipos de tumor.
Os pesquisadores foram capazes de conectar o inibidor em uma variedade de pontos de fixação por ligantes estáveis ao anticorpo, impedindo assim a divisão prematura. Apenas dentro das células tumorais, os conjugados são metabolizados por enzimas, liberando o inibidor. A variação do ligante permite a variação controlada das moléculas inibidoras resultantes, de modo que sua atividade pode ser adaptada aos requisitos específicos. Os inibidores que não podem ser expelidos das células se acumulam nas células tumorais, alongando seu período ativo. Os inibidores que podem ser expulsos podem entrar nas células tumorais vizinhas, que é especialmente útil no tratamento de tumores que contêm um padrão heterogêneo de locais de ligação de anticorpos.
Os novos conjugados são altamente eficazes in vitro e demonstraram ser eficazes em modelos de tumor para várias indicações in vivo. Em experimentos com ratos, eles levaram à remissão completa de um modelo de tumor de bexiga humana - com efeitos colaterais mínimos.