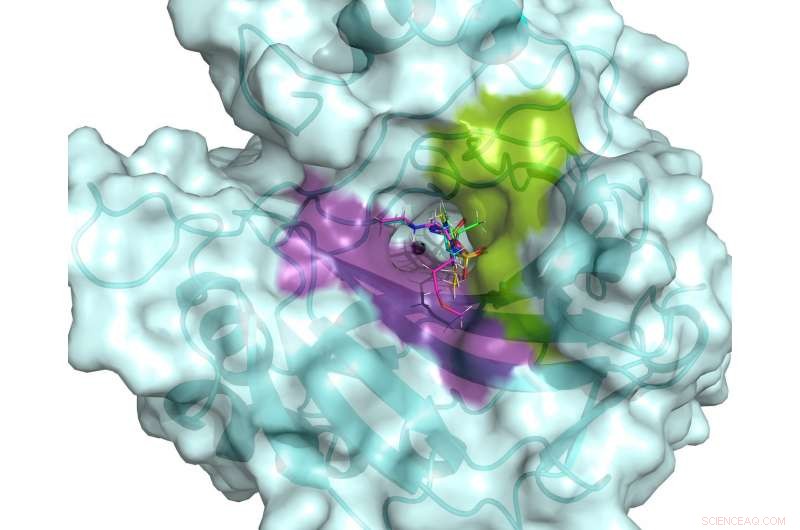
O sítio ativo do hCA II. O sítio ativo é flanqueado por bolsões de ligação hidrofílicos (violeta) e hidrofóbicos (verde) que podem ser usados para projetar drogas específicas visando hCAs associados ao câncer. Cinco medicamentos clínicos são mostrados sobrepostos no sítio ativo do hCA II, com base em estruturas de nêutrons à temperatura ambiente. Crédito:ORNL / Andrey Kovalevsky
Novos insights da análise de nêutrons de medicamentos para glaucoma e seu alvo enzimático podem ajudar os cientistas a desenvolver medicamentos que visem de forma mais eficaz os cânceres agressivos.
Uma equipe de pesquisadores liderada pelo Laboratório Nacional Oak Ridge do Departamento de Energia usou cristalografia macromolecular de nêutrons para investigar os diferentes estados de três medicamentos para glaucoma conforme eles interagem com a enzima alvo, anidrase carbônica humana II (hCA II).
"Nosso objetivo era observar as diferenças na apresentação de três medicamentos para glaucoma usados clinicamente enquanto eles estão ligados à enzima hCA II, "disse Andrey Kovalevsky, um cientista de instrumentos no ORNL e um co-autor sênior do estudo. "Ao observar o quão bem essas drogas são direcionadas ao hCA II em protonado, estados neutros e desprotonados, esperávamos obter insights que tornariam possível melhorar esses medicamentos para que eles possam direcionar melhor as enzimas ligadas ao câncer. "
Protonação se refere à presença, adição ou perda de um próton, que dá à droga um neutro, carga positiva ou negativa, respectivamente. Alterar a carga de uma droga pode alterar sua capacidade de reconhecer e se ligar à sua proteína-alvo e, consequentemente, sua eficácia.
O estudo, publicado no jornal Estrutura , encontrei essa temperatura, pH, e a carga elétrica dos três medicamentos para o glaucoma afetou sua capacidade de direcionar e se ligar à enzima hCA II.
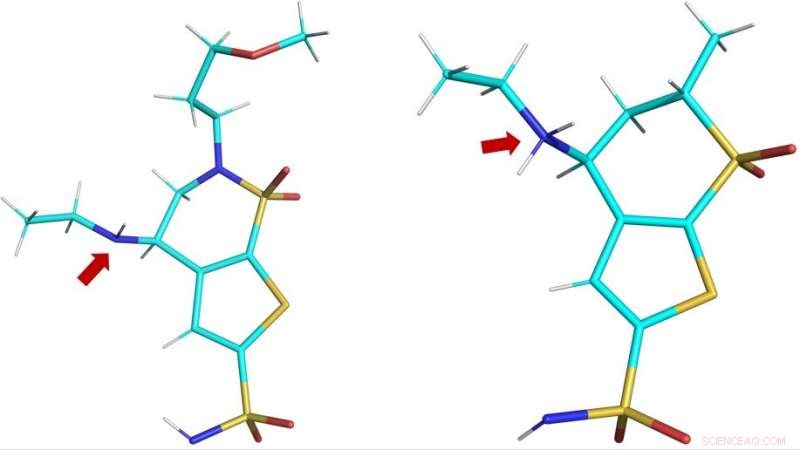
Estruturas tridimensionais das drogas clínicas brinzolamida (BZM, esquerda) anddorzolamida (DZM, direita) conforme observado no sítio ativo do hCA II. A seta vermelha mostra os grupos amino das drogas:em BZM, o átomo de nitrogênio (em azul) não é protonado e, portanto, não carregado; em DZM, o átomo de nitrogênio aceitou um próton extra e, portanto, está carregado positivamente. Crédito:ORNL / Andrey Kovalevsky
"Esta descoberta foi realmente uma prova de princípio para nós, "disse Robert McKenna, professor da Universidade da Flórida e co-autor sênior do estudo. "Isso abriu nossos olhos para como as mudanças na temperatura e no pH podem afetar o estado de protonação da droga, o que, por sua vez, o torna mais ou menos eficaz. "
Novas informações sobre as redes de ligações de hidrogênio que constituem o sítio ativo do hCA II podem ajudar outros cientistas a desenvolver novos e melhores medicamentos para o tratamento do câncer. A família de enzimas hCA contém proteínas semelhantes, como hCA IX e XII, que estão associados a cânceres de mama agressivos, como câncer de mama triplo negativo.
“Queremos explorar a diferença no comando, pH e temperatura para ver se podemos desenvolver drogas que sejam mais eficazes no direcionamento dessas enzimas, "disse Kovalevsky." Se pudermos entender a ligação em nível atômico, podemos redesenhar medicamentos e transformá-los em 'ímãs' mais fortes e seletivos que serão atraídos por enzimas associadas ao câncer. Essas drogas seriam muito mais eficazes em matar células cancerosas, deixando as células saudáveis ilesas, o que reduz significativamente os efeitos colaterais para os pacientes. "
Muitos cientistas usaram a cristalografia de raios-X para analisar as estruturas de hCA enymes, mas esses estudos carecem de informações atômicas completas sobre a ligação de drogas por causa da incapacidade dos raios-X de visualizar átomos de hidrogênio abundantes em proteínas e enzimas.
Os nêutrons são sensíveis aos elementos mais leves, portanto, eles fornecem informações muito mais detalhadas sobre a localização dos átomos de hidrogênio. Ver o hidrogênio é fundamental para estudar os estados de protonação de uma enzima e ligante - uma molécula que se liga a uma macromolécula biológica - e para analisar a arquitetura das redes de ligações de hidrogênio. Os nêutrons também oferecem outras vantagens experimentais.
"Quando você usa difração de nêutrons, você não tem danos de radiação, então você pode fazer seu estudo em temperatura ambiente, "disse McKenna." Além disso, cristais congelados podem alterar a droga e a enzima, introduzindo uma visão falsa no estudo, enquanto os estudos de temperatura ambiente se assemelham mais ao ambiente em que a droga será usada. "