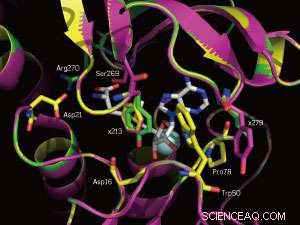
Um close-up dos locais de ligação de SAM da enzima nativa (amarelo) e dois mutantes (magenta e verde). As posições mutadas 213 e 279 são marcadas. Crédito:WILEY-VCH Verlag GmbH &Co. KGaA, Weinheim
Moléculas orgânicas contendo um átomo de flúor são amplamente utilizadas nos materiais, indústrias agroquímicas e farmacêuticas. Contudo, sintetizar a ligação carbono-flúor normalmente utiliza catalisadores de metal tóxicos e requer condições anidras e altas temperaturas. Agora, uma equipe internacional desenvolveu um sistema mais suave, abordagem baseada em enzimas mais eficiente para criar essa ligação.
Este método enzimático funciona em condições aquosas e em temperaturas amenas e foi desenvolvido por um consórcio que incluiu pesquisadores da A * STAR e outras instituições. "Essas condições são realmente muito atraentes, "explica o membro da equipe Yee Hwee Lim do Instituto A * STAR de Ciências Químicas e de Engenharia.
A equipe utilizou uma das enzimas fluorinase altamente específicas que são encontradas na natureza - FlA1. Essas enzimas catalisam a formação de uma ligação carbono-flúor em S-adenosilmetionina (SAM) usando fluoreto inorgânico por meio de um mecanismo de substituição.
A enzima, embora excelente em catalisar reações de fluoração com esta molécula natural, não funcionou bem em moléculas não naturais. Além disso, esforços para modificar as estruturas das enzimas e, portanto, função tinha sido uma luta - até agora.
"Mostramos pela primeira vez que a enzima fluorinase pode ser projetada, e que a engenharia pode melhorar sua atividade enzimática mesmo em moléculas não naturais, "Lim diz.
A equipe utilizou a técnica estabelecida conhecida como 'evolução direcionada', que imita a seleção natural para desenvolver enzimas para que possam reagir bem com moléculas não naturais.
"A evolução dirigida nunca foi aplicada com sucesso a esta enzima, até agora, "diz Lim." Esta é uma enzima difícil de trabalhar e enfrentamos muitos desafios, incluindo problemas com a degradação do produto. "
A equipe usou a radiomarcação de 5'-cloro-5'-desoxiadenosina (5'-CIDA) para mostrar suas capacidades. Nesta reação de duas etapas, 5'-CIDA radiomarcado é convertido em SAM, e então fluorado para formar 5'-fluoro-5'-desoxiadenosina (5'-FDA). Este produto 5'-FDA rotulado pode ser usado para um procedimento de diagnóstico médico conhecido como tomografia por emissão de pósitrons (PET).
"Nós mostramos que melhorar a atividade de uma enzima três vezes pode abrir mais aplicações, "diz Lim." As enzimas nativas foram usadas anteriormente para tentar rotular os agentes PET, mas os tempos de reação eram longos, às vezes horas. Usando nossa enzima, poderíamos fazer a reação em 30 minutos, um cronograma mais razoável, dado que a meia-vida do Fluorine-18 é de menos de duas horas. "
A equipe de Lim agora está explorando como a mutação da estrutura da enzima muda sua interação com 5'-CIDA e SAM. "Eu gostaria de envolver biólogos computacionais para entender melhor mais sobre as mutações que fizemos e como elas se correlacionam com nossas reações."