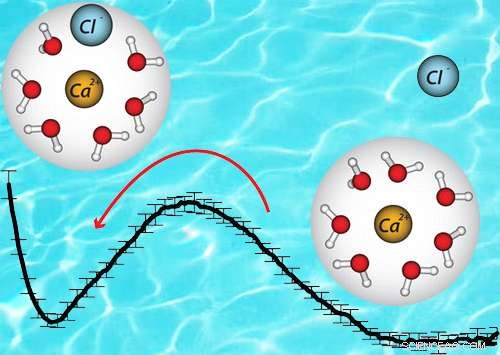
A energia livre é diferente entre o par de íons (esquerda) e o íon sozinho (direita). Não foi possível ver essa diferença com as abordagens anteriores. Crédito:American Chemical Society
De baterias a biologia, líquidos contendo sal são vitais para um desempenho contínuo. A compreensão precisa do comportamento desses líquidos depende da representação correta das estruturas moleculares que eles formam. Dr. Marcel Baer, Dr. Timothy Duignan, e o Dr. Christopher Mundy, do Pacific Northwest National Laboratory, determinou que a estrutura precisa de um par de íons isolados na água relata com precisão como uma solução inteira se comportará.
"Esta estrutura local precisa é a peça importante para relacionar o microscópico ao macroscópico, ou propriedades intrínsecas dos íons em solução para propriedades coletivas, "disse Mundy, que liderou os estudos no PNNL.
Ao integrar cálculos e experimentos em torno de dois íons que formam um par iônico de sal, a equipe pode compreender a natureza coletiva da solução. Nomeadamente, a equipe pode entender as estatísticas de agrupamento no que se refere ao comportamento específico dos íons em diferentes concentrações, que é medido pelo coeficiente osmótico. Especificamente, o eletrólito se forma em aglomerados ou permanece como íons isolados em diferentes concentrações?
O comportamento e a especiação dos eletrólitos influenciam tudo, desde seu uso como eletrólitos de bateria até seu comportamento em resíduos nucleares complexos. Ao compreender como as propriedades individuais dos íons informam seu comportamento coletivo, os cientistas podem determinar como adaptar a concentração e o tipo de eletrólito para aplicações específicas.
A equipe examinou como a estrutura molecular correta influencia a termodinâmica da solução. Eles determinaram a estrutura por meio de medições estendidas da estrutura fina de absorção de raios-X e simulação molecular com base na mecânica quântica. O trabalho da equipe demonstra que é possível prever o grau em que os íons estão emparelhados na solução (chamada de atividade) usando descrições precisas do íon-água local, e interações íon-íon.
Em um artigo de revisão simultâneo convidado com o Dr. Tim Duignan, a equipe demonstrou como acertar o emparelhamento com cálculos de alto nível. Os resultados fornecem os detalhes moleculares necessários para melhorar as teorias macroscópicas de solvatação de íons.