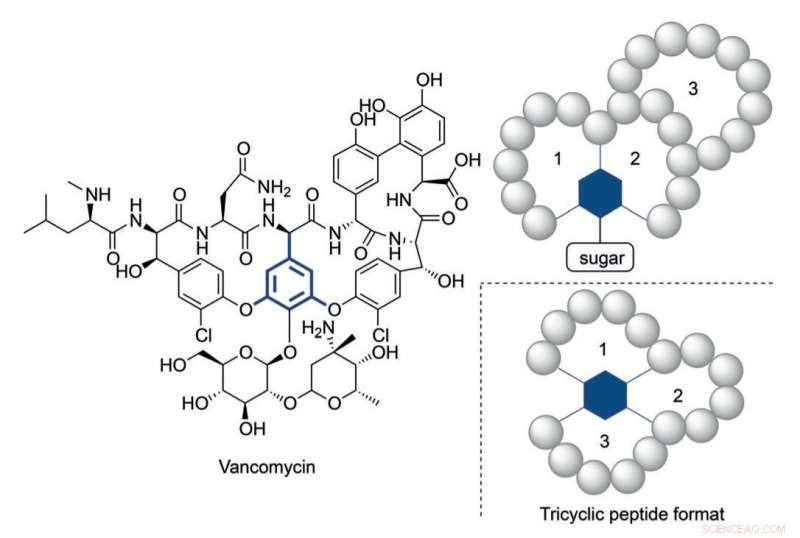
Estrutura da vancomicina e formato de um peptídeo tricíclico inspirado em sua estrutura multicíclica. Crédito:HIMS
Químicos do Instituto Van 't Hoff de Ciências Moleculares (HIMS) e Pepscan (Lelystad) da Universidade de Amsterdã desenvolveram uma nova metodologia para bloquear peptídeos lineares em estruturas tricíclicas altamente rígidas com potencial farmacêutico. Suas descobertas acabaram de ser relatadas em Angewandte Chemie .
A metodologia, desenvolvido por HIMS Ph.D. estudante Gaston Richelle, permite a síntese paralela de vários peptídeos tricíclicos em um formato de biblioteca. Isto permite o rastreio biológico subsequente de modo a identificar novos peptídeos terapêuticos.
Nível mais alto de complexidade estrutural
Ao longo da última década, os peptídeos cíclicos surgiram como uma classe promissora de terapêutica, mostrando uma ampla janela terapêutica que varia da antifertilidade às aplicações antivirais e anticâncer. Muitos peptídeos monocíclicos e bicíclicos foram identificados e o número de peptídeos cíclicos que entram em ensaios clínicos aumentou drasticamente.
Mesmo assim, tornou-se claro que, em alguns casos, são necessários peptídeos estruturalmente mais complexos para atingir níveis de atividade apropriados. Vancomicina, o peptídeo antibiótico tricíclico de 'último recurso', fornece um exemplo ilustrativo de tal construção complexa. O aumento alarmante da resistência das bactérias contra os antibióticos atualmente disponíveis exige construções complexas de peptídeos em analogia à vancomicina.
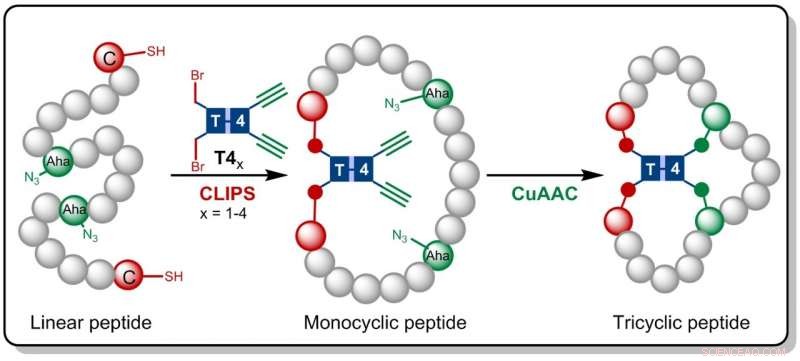
Crédito:HIMS
A busca por novas rotas sintéticas para peptídeos multicíclicos complexos, portanto, ganhou sério interesse. Metodologias anteriormente relatadas para a criação de peptídeos multicíclicos foram limitadas devido à formação de múltiplos isômeros, protocolos de reação trabalhosos ou diversidade estrutural limitada.
CLIPS combinados com CuAAC
Na pesquisa agora publicada em Angewandte Chemie , os químicos de Amsterdã se baseiam na tecnologia CLIPS desenvolvida anteriormente na Pepscan. Este método para 'Lincagem Química de Peptídeos em Scaffolds' produz peptídeos monocíclicos e bicíclicos que mostraram exibir seletividades e afinidades aumentadas contra proteínas alvo.
Gaston Richelle combinou agora o método CLIPS com a química 'click' CuAAC totalmente compatível, levando à formação de peptídeos tricíclicos complexos. Ao fazer uso de moléculas de estrutura flexível, os procurados péptidos tricíclicos são formados de uma forma isomericamente pura. A principal vantagem da nova metodologia é que as reações CLIPS e CuAAC podem ser realizadas em um procedimento de um único recipiente, sem limitações quanto à natureza e às quantidades de aminoácidos que são implementadas nas alças do peptídeo.
Como resultado, a metodologia pode ser aplicada em bibliotecas de peptídeos de alta diversidade para gerar uma ampla gama de topologias tricíclicas que podem ser rastreadas quanto à atividade biológica. Atualmente, vários exames de inibição são realizados, por exemplo. contra enzimas que são altamente abundantes nas células cancerosas de primeiro estágio. Também novos estudos de atividade antimicrobiana são realizados contra MRSA e Staphylococcus aureus. Somando a isso, a equipe de pesquisa está atualmente estudando o uso de andaimes T6 ainda mais complexos para criar peptídeos penta e hexacíclicos.