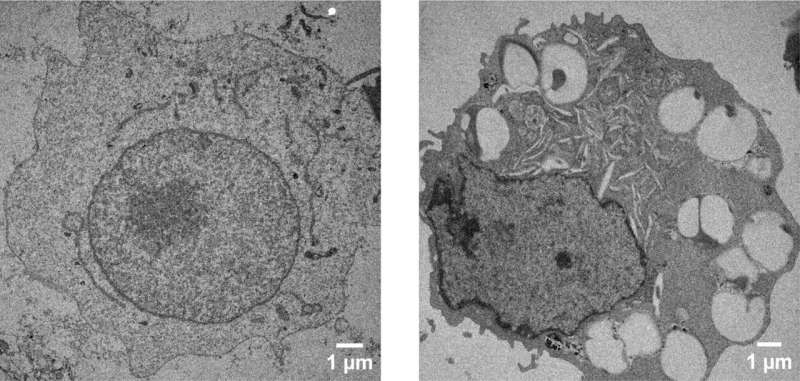
 Estrutura interna de uma célula saudável (esquerda) em comparação com uma célula que absorveu nanopartículas revestidas com DNA (direita). As grandes cavidades são os locais onde a nanopartícula foi internalizada, ajudando os pesquisadores a entender melhor quais receptores celulares estão sendo ativados. Crédito:Anais da Academia Nacional de Ciências (2024). DOI:10.1073/pnas.2319634121
Estrutura interna de uma célula saudável (esquerda) em comparação com uma célula que absorveu nanopartículas revestidas com DNA (direita). As grandes cavidades são os locais onde a nanopartícula foi internalizada, ajudando os pesquisadores a entender melhor quais receptores celulares estão sendo ativados. Crédito:Anais da Academia Nacional de Ciências (2024). DOI:10.1073/pnas.2319634121 As doenças autoimunes são misteriosas. Somente na década de 1950 é que os cientistas perceberam que o sistema imunológico poderia prejudicar os órgãos do seu próprio corpo. Ainda hoje, as causas fundamentais e o funcionamento interno da maioria das doenças autoimunes permanecem pouco compreendidos, limitando as opções de tratamento para muitas destas condições.
Nos últimos anos, no entanto, pesquisas encontraram pistas sobre como podem surgir doenças autoimunes. Esta pesquisa mostrou que o DNA ligado a pequenas partículas na corrente sanguínea é um provável culpado envolvido em muitas doenças autoimunes, especialmente o lúpus eritematoso sistêmico, ou simplesmente lúpus, que afeta principalmente mulheres jovens e pode causar danos renais.
No entanto, devido à grande variedade de tamanhos das partículas e do ADN no sangue, tem sido extremamente difícil testar até que ponto e em que circunstâncias estas combinações de partículas de ADN desempenham um papel na doença.
Pesquisadores da Duke University desenvolveram agora uma maneira de testar sistematicamente como essas partículas ligadas ao DNA interagem com o sistema imunológico. Ao utilizar pequenas partículas de tamanhos específicos, anexar cadeias de ADN de determinados comprimentos e expor os complexos resultantes às células imunitárias numa placa de laboratório, os investigadores mostram que pode ser possível uma melhor compreensão fundamental destas doenças.
Os resultados foram publicados no Proceedings of the National Academy of Sciences .
"Nossa abordagem identificou a via celular que causa a resposta prejudicial a essas partículas híbridas e mostrou que o DNA ligado às superfícies das nanopartículas está protegido contra degradação por enzimas", disse Christine Payne, professora de Engenharia Mecânica e Ciência de Materiais da Família Yoh. . “Acreditamos que estes são resultados extremamente importantes que formarão a base para estudos futuros com o nosso novo sistema”.
Embora o DNA geralmente esteja trancado dentro do núcleo de uma célula, ele geralmente entra na corrente sanguínea quando as células morrem ou são atacadas por vírus e bactérias. Embora a maior parte do chamado “DNA livre de células” dure apenas alguns minutos antes de ser decomposto pelo corpo, em algumas pessoas e situações ele pode persistir por muito mais tempo. Em trabalhos recentes, elevados níveis de ADN livre de células têm sido intimamente relacionados com a gravidade dos sintomas do lúpus, e muitos médicos estão agora a testar formas de o utilizar para monitorizar a actividade da doença.
O DNA livre de células pode escapar da eliminação em grande parte formando complexos com outras moléculas ou ligando-se a partículas que ocorrem naturalmente. Dependendo da origem do DNA, seu comprimento pode variar de algumas centenas de pares de bases a vários milhares. E as partículas às quais ele pode se fixar variam de 100 a 1.000 nanômetros de diâmetro.
“Experimentar as partículas realmente encontradas no sangue é difícil porque elas vêm em muitos tamanhos e combinações diferentes”, disse o Dr. David Pisetsky, professor de medicina e imunobiologia integrativa na Faculdade de Medicina da Universidade Duke.
"Onde trabalhos anteriores se concentraram no uso de nanopartículas para terapia, aqui estamos explorando o uso de particípios para compreender os mecanismos das doenças, o que pode ser muito informativo para questões médicas importantes." Payne trabalhou com membros de seu laboratório para fabricar partículas sintéticas rigidamente controladas em ambas as extremidades do espectro de tamanho que ocorre naturalmente.
Eles então anexaram fitas de DNA de E. Coli, com algumas centenas de pares de bases ou 10.000 pares de bases, a partículas grandes e pequenas. Com uma ampla gama de complexos sintéticos de partículas de DNA em mãos, eles misturaram diversas combinações com macrófagos humanos, um tipo de glóbulo branco que envolve e mata microrganismos, remove células mortas e estimula a ação de outras células do sistema imunológico.
"Entrei no laboratório há mais de um ano e tenho trabalhado na caracterização das coroas de nanopartículas para entender seu tamanho, quantidade de DNA e como o DNA se degrada", disse Diego Montoya, estudante do terceiro ano que trabalha no laboratório de Payne e pesquisador. coautor do artigo. "Tem sido muito divertido e um privilégio trabalhar com todos nesta pesquisa."
A primeira observação importante que a equipe fez foi que o DNA ligado às nanopartículas estava protegido de enzimas degradantes e que nanopartículas maiores forneciam mais proteção.
“Achamos que as enzimas podem não ser capazes de acessar o DNA para destruí-lo devido à forma que o DNA assume na superfície da nanopartícula”, disse Faisal Anees, Ph.D. estudante no laboratório de Payne. “Mas pode haver outros efeitos, então essa é uma questão que estamos tentando responder de forma mais definitiva agora”.
Os resultados mostraram que os macrófagos responderam a todos os tipos de complexos de partículas de DNA, produzindo sinais inflamatórios para outras células seguirem, uma marca registrada de muitas doenças autoimunes. Eles também demonstraram que esta resposta é criada através de uma via de sinalização específica chamada cGAS-STING.
Os investigadores sublinham que os resultados combinados ainda não fornecem uma prova definitiva da causa do lúpus ou de outras doenças autoimunes, que são provavelmente variadas e matizadas.
“Todas as formas como o sistema imunológico ataca a si mesmo são realmente complexas, difíceis de entender e difíceis de tratar”, disse Payne. "Essa abordagem dá aos pesquisadores uma maneira de detalhar e identificar fatores que não seriam capazes de fazer com um sistema puramente biológico."
“Temos agora um sistema modelo bem definido que nos dá a capacidade de fazer estas perguntas sobre causalidade versus correlação”, acrescentou Pisetsky, que investiga doenças autoimunes há quase meio século. "Isso também nos dá um novo método para explorar terapias potenciais."
