Pesquisas revelam um novo mecanismo para transferir quiralidade entre moléculas no campo de nanoescala
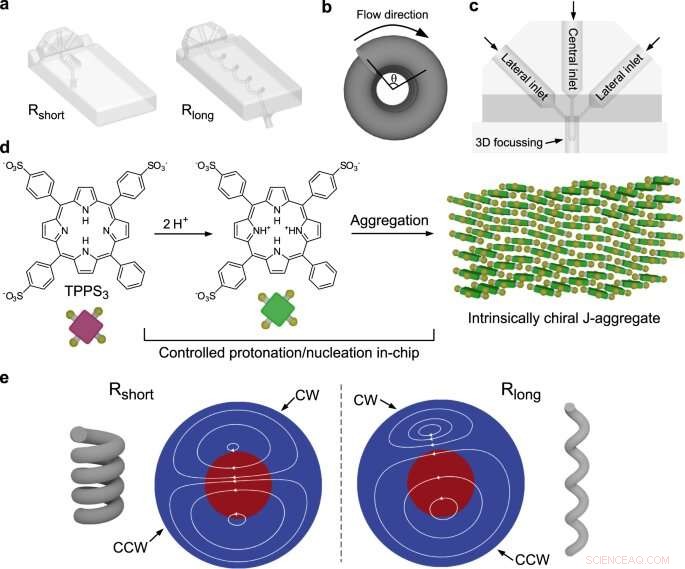
a Ilustrações de dispositivos Rshort e Rlong. b Definição do ângulo de rotação θ. c Detalhe da porção de entrada dos dispositivos fluídicos. Para obter uma focagem 3D hidrodinâmica concêntrica, uma agulha concêntrica de 2 mm de comprimento foi projetada para fornecer a solução injetada através da entrada central no centro do canal principal, enquanto cercada pela bainha gerada pelas soluções alimentadas pelas entradas laterais. d Esquema da agregação induzida por protonação de TPPS3 para dar agregados J intrinsecamente quirais (nota:no desenho da porfirina as bolas amarelas representam os anéis fenil contendo ou não o grupo sulfonato). e Representação 2D das trajetórias do fluxo secundário formado dentro dos dispositivos Rcurto (esquerda) e Rlongo (direita), mostrando diferentes magnitudes relativas dos vórtices CW e CCW contra-rotativos em hélices de passo curto e longo. A porfirina é injetada no meio do canal (cor vermelha) cercada por uma bainha da solução ácida (região azul). Condições de contorno:15 µM TPPS3 na entrada central, 10 mM HCl nas entradas laterais. Crédito:Sevim et al, Nature Communications (2022)
Se compararmos a mão direita com a esquerda, podemos ver que são imagens especulares - isto é, como formas simétricas refletidas em um espelho - e elas não podem se sobrepor. Essa propriedade é a quiralidade, uma característica da matéria que brinca com a simetria das estruturas biológicas em diferentes escalas, desde a molécula de DNA até os tecidos do músculo cardíaco.
Agora, um novo artigo publicado na revista
Nature Communications revela um novo mecanismo para transferir a quiralidade entre moléculas no campo da nanoescala, de acordo com um estudo liderado pelo professor da UB Josep Puigmartí-Luis, da Faculdade de Química e do Instituto de Química Teórica e Computacional (IQTC) da Universidade de Barcelona .
Quiralidade:de partículas fundamentais a biomoléculas A quiralidade é uma propriedade intrínseca da matéria que determina a atividade biológica das biomoléculas. "A natureza é assimétrica, tem uma esquerda e uma direita e sabe a diferença entre elas. As biomoléculas que formam a matéria viva - aminoácidos, açúcares e lipídios - são quirais:são formadas por moléculas quimicamente idênticas que são as moléculas especulares. imagens entre si (enantiômeros), um recurso que fornece propriedades diferentes como compostos ativos (atividade óptica, ação farmacológica, etc.)", observa Josep Puigmartí-Luis, pesquisador do ICREA e membro do Departamento de Ciência dos Materiais e Físico-Química.
"Os enantiômeros são quimicamente idênticos até que sejam colocados em um ambiente quiral que possa diferenciá-los (como o sapato direito 'reconhece' o pé direito). Sistemas vivos, feitos de moléculas homoquirais, são ambientes quirais (com o mesmo enantiômero), são quirais ambientes para que possam 'reconhecer' e responder de forma diferente às espécies enantioméricas. Além disso, podem controlar facilmente o sinal quiral em processos bioquímicos dando transformações estereoespecíficas."
Como obter moléculas quirais através de reações químicas O controle da quiralidade é decisivo na produção de medicamentos, agrotóxicos, aromas, sabores e outros compostos químicos. Cada enantiômero (molécula com certa simetria) tem uma certa atividade que é diferente do outro composto quimicamente idêntico (sua imagem especular). Em muitos casos, a atividade farmacológica de um enantiômero pode ser escassa e, na pior das hipóteses, pode ser muito tóxica. "Portanto, os químicos precisam ser capazes de fazer compostos como enantiômeros únicos, o que é chamado de síntese assimétrica", diz Puigmartí-Luis.
Existem várias estratégias para controlar o sinal de quiralidade em processos químicos. Por exemplo, usando compostos enantiopuros naturais conhecidos como pool quiral (por exemplo, aminoácidos, hidroxiácidos, açúcares) como precursores ou reagentes que podem se tornar um composto de interesse após uma série de modificações químicas. A resolução quiral é outra opção que permite separar enantiômeros através do uso de um agente de resolução enantiômero puro, e recuperar os compostos de interesse como enantiômeros puros. O uso de auxiliares quirais que auxiliam um substrato a reagir de forma diastereosseletiva é outra metodologia eficiente para obter um produto enantiomericamente puro. Por último, a catálise assimétrica – baseada no uso de catalisadores assimétricos – é o procedimento principal para se chegar à síntese assimétrica.
"Cada método descrito acima tem seus prós e contras", observa Alessandro Sorrenti, membro da Seção de Química Orgânica da Universidade de Barcelona e colaborador do estudo. "Por exemplo, a resolução quiral - o método mais difundido para a produção industrial de produtos enantiomericamente puros - é intrinsecamente limitada a 50% de rendimento. O pool quiral é a fonte mais abundante de compostos enantiómeros, mas geralmente há apenas um enantiômero disponível. O método auxiliar quiral pode oferecer altos excessos enantioméricos, mas requer fases sintéticas adicionais para adicionar e remover o composto auxiliar, bem como etapas de purificação. pequeno número de reações."
"Todos os métodos mencionados fazem uso de compostos enantiomericamente puros - na forma de agentes de resolução, auxiliares ou ligantes para catalisadores metálicos - que, em última análise, derivam direta ou indiretamente de fontes naturais. Em outras palavras, a natureza é a forma última de assimetria."
Controlando o sinal de quiralidade através da dinâmica de fluidos O novo artigo descreve como a modulação da geometria de um reator helicoidal em nível macroscópico permite controlar o sinal de quiralidade de um processo em escala nanométrica, uma descoberta inédita até o momento na literatura científica.
Além disso, a quiralidade é transferida de cima para baixo, com a manipulação do tubo helicoidal ao nível molecular, através da interação da hidrodinâmica dos fluxos secundários assimétricos e do controle espaço-temporal dos gradientes de concentração dos reagentes.
"Para que isso funcione, precisamos entender e caracterizar os fenômenos de transporte que ocorrem dentro do reator, ou seja, a dinâmica dos fluidos e o transporte de massa, que determinam a formação de frentes de concentração de reagentes e o posicionamento da zona de reação em regiões de quiralidade específica. ”, observa Puigmartí-Luis.
Em um canal helicoidal, o escoamento é mais complexo do que em um canal reto, pois as paredes curvas geram forças centrífugas que resultam na formação de escoamentos secundários no plano perpendicular à direção do fluido (fluxo principal). Esses fluxos secundários (vórtices) têm uma dupla função:são regiões de quiralidade oposta e constroem o ambiente quiral necessário para a enantiosseleção. Além disso, por advecção dentro do dispositivo e para o desenvolvimento de gradientes de concentração de reagentes.
Ao modular a geometria do reator helicoidal em nível macroscópico, "é possível controlar a assimetria dos fluxos secundários de tal forma que a zona de reação - a região onde os reagentes se encontram em uma concentração adequada para reagir - fique exposta exclusivamente a um dos dois vórtices e, portanto, a uma quiralidade específica. Este mecanismo de transferência de quiralidade, baseado no controle racional do fluxo de fluido e transporte de massa, permite, em última análise, controlar a enantiosseleção dependendo da quiralidade macroscópica do reator helicoidal, onde a lateralidade do a hélice determina o sentido da enantiosseleção", diz Puigmartí-Luis.
As descobertas lançam luz sobre novas fronteiras para alcançar a enantiosseleção em nível molecular – sem o uso de compostos enantiopuros – apenas combinando a geometria e as condições de trabalho dos reatores de fluido. “Além disso, nosso estudo fornece uma nova visão fundamental dos mecanismos subjacentes à transferência de quiralidade, demonstrando que essa propriedade intrínseca da matéria viva é baseada na interação de restrições físicas e químicas que atuam sinergicamente em várias escalas de comprimento”, conclui Josep Puigmartí-Luis .
+ Explorar mais Observando mudanças na quiralidade das moléculas em tempo real
