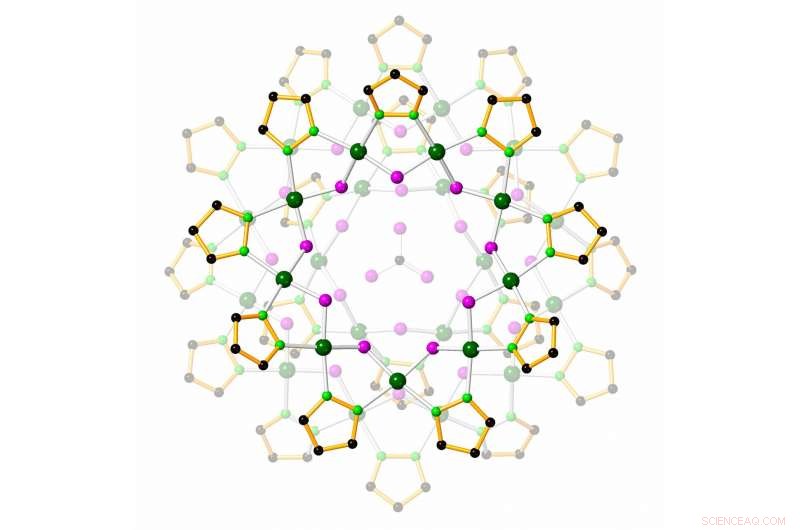
Um nanojar captura um íon carbonato (centro) para removê-lo da água. Crédito:Gellert Mezei
O dióxido de carbono da atmosfera pode se dissolver nos oceanos, lagos e lagoas, formando íons de bicarbonato e outros compostos que mudam a química da água, com possíveis efeitos nocivos para os organismos aquáticos. Além disso, o bicarbonato pode reentrar na atmosfera como dióxido de carbono mais tarde, contribuindo para a mudança climática. Agora, pesquisadores desenvolveram minúsculos "nanojares, "muito menor do que a largura de um cabelo humano, que divide o bicarbonato em carbonato e o captura, bem como certos ânions tóxicos, para que os íons possam ser removidos e potencialmente reciclados.
Os pesquisadores apresentarão seus resultados hoje na reunião de outono da American Chemical Society (ACS).
"Nós originalmente desenvolvemos nanojars para extrair íons nocivos carregados negativamente, como cromato e arseniato, da água, "diz Gellert Mezei, Ph.D., quem está apresentando o trabalho na reunião. "Mas acontece que eles também se ligam fortemente ao carbonato." Carbonato ou outros íons capturados nos nanojars podem mais tarde ser descartados ou reciclados em produtos úteis, ele diz.
Nanojars são pequenos recipientes feitos de várias unidades repetidas de um íon de cobre, um grupo pirazol e um hidróxido. Os frascos só se formam quando um íon com carga -2, como cromato, arseniato, fosfato ou carbonato, é presente. Quando os ingredientes adequados são adicionados a um solvente orgânico, as unidades repetidas se formam e montam em nanojars, com o ânion –2 carregado fortemente preso ao centro.
Para remover ânions da água, os pesquisadores adicionaram o solvente contendo os componentes de nanojar, que formou uma camada orgânica em cima da água. "O solvente não se mistura com a água, mas os ânions da água podem entrar nesta camada orgânica, "explica Mezei, que está na Western Michigan University. "Então, os nanojars se formam e envolvem os íons, prendendo-os na fase orgânica. "Como a água e as camadas orgânicas não se misturam, eles podem ser facilmente separados. O tratamento da camada orgânica com um ácido fraco faz com que os nanojars se desfaçam, liberando os ânions para descarte ou reciclagem.
Os pesquisadores usaram nanojars para remover ânions tóxicos da água. "Nós mostramos que podemos extrair cromato e arseniato abaixo dos níveis permitidos pela Agência de Proteção Ambiental dos EUA para água potável - realmente, níveis realmente baixos, "Mezei diz. Os nanojars têm uma afinidade ainda maior com o carbonato, e adicionar uma molécula chamada 1, A 10-fenantrolina à mistura produz nanojars que ligam dois íons carbonato cada, em vez de um.
A equipe também fez nanojares que são seletivos para determinados ânions. "O bloco de construção do pirazol original faz nanojars que são totalmente seletivos para –2 íons carregados, mas eles não podem discriminar entre esses íons, "Mezei diz. Usando dois pirazoles amarrados por um ligante de etileno como um bloco de construção, os pesquisadores fizeram nanojares que se ligam preferencialmente ao carbonato. Mais recentemente, eles mostraram que o uso de dois pirazóis com um ligante de propileno produz nanojares seletivos para sulfato. Esses nanojares seletivos para ânions serão importantes para aplicações nas quais apenas alguns íons carregados –2 devem ser removidos.
Os pesquisadores também têm trabalhado para tornar o processo mais adequado para aplicações do mundo real. Por exemplo, eles trocaram uma base fraca, trioctilamina, para a base forte, hidróxido de sódio, originalmente usado para fazer nanojars. "Trioctilamina, ao contrário do hidróxido de sódio, é solúvel na fase orgânica e torna a formação dos nanojares muito mais eficiente, "Mezei diz. Curiosamente, trioctilamina faz com que nanojars se formem com estruturas ligeiramente diferentes, que ele chama de nanojares "limitados", mas eles parecem se ligar ao carbonato com a mesma firmeza.
Até aqui, todos os experimentos foram conduzidos em escala de laboratório. Desenvolvendo um sistema para tratar grandes volumes de água, como em um lago, exigirá colaboração com engenheiros, Mezei diz. Contudo, ele imagina que a água contaminada do lago poderia ser bombeada para uma estação de tratamento e depois devolvida ao lago. Alguns íons, como fosfato, pode ser reciclado para fins úteis, como fertilizantes. O carbonato pode ser reciclado para fazer solventes "verdes", chamados de ésteres de carbonato, para a própria extração de nanojar. "Seja este processo de remoção de dióxido de carbono da água - e indiretamente, a atmosfera –– seria competitiva com outras tecnologias, que eu não sei ainda, "Mezei diz." Há muitos aspectos que devem ser levados em consideração, e isso é um negócio complicado. "