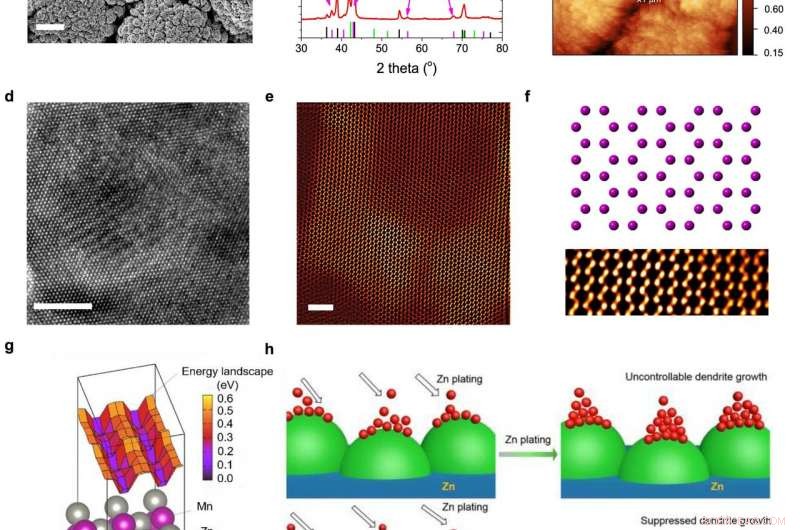
uma imagem SEM. A barra de escala:10 μm. b Padrão XRD. c Imagem AFM. d Imagem HRTEM de Zn3Mn vista ao longo da direção [001]. A barra de escala:10 nm. e, f Imagem HAADF-STEM e a estrutura cristalina atômica correspondente. As barras de escala:2 nm. As bolas roxas no modelo de estrutura de cristal representam os átomos de Zn / Mn co-ocupados. g Estrutura atômica e a paisagem de energia do átomo-ad de superfície de Zn3Mn. h Ilustração esquemática dos processos de galvanização de Zn no ânodo Zn (parte superior) e ânodo Zn-Mn (parte inferior). De:Estável, alta performance, livre de dendritos, baterias aquosas à base de água do mar
Pesquisadores da Faculdade de Engenharia da Universidade Estadual do Oregon desenvolveram um ânodo de bateria baseado em uma nova liga nanoestruturada que pode revolucionar a maneira como os dispositivos de armazenamento de energia são projetados e fabricados.
A liga à base de zinco e manganês abre ainda mais a porta para a substituição de solventes comumente usados em eletrólitos de bateria por algo muito mais seguro e barato, bem como abundante:água do mar.
As descobertas foram publicadas em Nature Communications .
"As necessidades mundiais de energia estão aumentando, mas o desenvolvimento de sistemas de armazenamento de energia eletroquímica de próxima geração com alta densidade de energia e longa vida útil continua sendo um desafio técnico, "disse Zhenxing Feng, pesquisador de engenharia química na OSU. "Baterias aquosas, que usam soluções condutoras à base de água como eletrólitos, são uma alternativa emergente e muito mais segura às baterias de íon de lítio. Mas a densidade de energia dos sistemas aquosos tem sido comparativamente baixa, e também a água vai reagir com o lítio, o que tem dificultado ainda mais o uso generalizado das baterias aquosas. "
Uma bateria armazena energia na forma de energia química e, por meio de reações, a converte na energia elétrica necessária para alimentar veículos, celulares, laptops e muitos outros dispositivos e máquinas. Uma bateria consiste em dois terminais - o ânodo e o cátodo, normalmente feito de materiais diferentes, bem como um separador e eletrólito, um meio químico que permite o fluxo de carga elétrica.
Em uma bateria de íon de lítio, como o nome sugere, uma carga é transportada por meio de íons de lítio conforme eles se movem através do eletrólito do ânodo para o cátodo durante a descarga, e de volta durante a recarga.
"Eletrólitos em baterias de íon-lítio são comumente dissolvidos em solventes orgânicos, que são inflamáveis e muitas vezes se decompõem em altas tensões de operação, "Feng disse." Portanto, há obviamente preocupações de segurança, incluindo com crescimento de dendrito de lítio na interface eletrodo-eletrólito; que pode causar um curto entre os eletrodos. "
Os dendritos se assemelham a pequenas árvores que crescem dentro de uma bateria de íon-lítio e podem perfurar o separador como cardos que crescem por rachaduras em uma calçada; o resultado são reações químicas indesejáveis e às vezes inseguras.
Incidentes de combustão envolvendo baterias de íon-lítio nos últimos anos incluem um incêndio em um jato Boeing 787 estacionado em 2013, explosões em smartphones Galaxy Note 7 em 2016 e disparos do Tesla Model S em 2019.
As baterias aquosas são uma alternativa promissora para armazenamento seguro e escalonável de energia, Feng disse. Eletrólitos aquosos são competitivos em termos de custos, ambientalmente benigno, capaz de carregamento rápido e densidades de alta potência e altamente tolerante a manuseio incorreto.
Seu uso em larga escala, Contudo, foi prejudicada por uma tensão de saída limitada e baixa densidade de energia (baterias com uma densidade de energia mais alta podem armazenar grandes quantidades de energia, enquanto as baterias com uma densidade de potência mais alta podem liberar grandes quantidades de energia mais rapidamente).
Mas pesquisadores da Oregon State, a University of Central Florida e a University of Houston projetaram um ânodo feito de uma "liga de zinco-M" tridimensional como o ânodo da bateria - onde M se refere ao manganês e outros metais.
"O uso da liga com sua nanoestrutura especial não apenas suprime a formação de dendritos, controlando a termodinâmica da reação de superfície e a cinética da reação, também demonstra estabilidade superelevada ao longo de milhares de ciclos sob condições eletroquímicas severas, "Feng disse." O uso de zinco pode transferir duas vezes mais cargas do que o lítio, melhorando assim a densidade de energia da bateria.
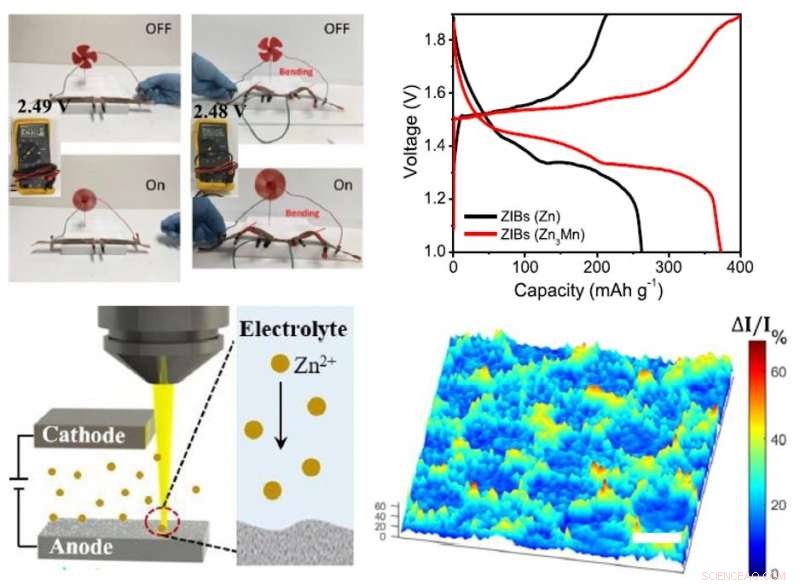
Um ventilador elétrico (canto superior esquerdo) é alimentado pela bateria de zinco proposta; perfis típicos de carga / descarga de ZIBs a 0,5 ° C (canto superior direito); configuração do microscópio in-situ para gerar imagens da dinâmica de deposição de zinco (canto inferior esquerdo); e a mudança morfológica causada pela deposição de zinco (embaixo à direita). Crédito:Universidade de Houston
"Também testamos nossa bateria aquosa usando água do mar, em vez de água desionizada de alta pureza, como o eletrólito, "Ele acrescentou." Nosso trabalho mostra o potencial comercial para a fabricação em larga escala dessas baterias. "
Feng e Ph.D. o aluno Maoyu Wang usou espectroscopia de absorção de raios-X e imagens para rastrear as mudanças atômicas e químicas do ânodo em diferentes estágios de operação, que confirmou como a liga 3-D estava funcionando na bateria.
"Nossos estudos teóricos e experimentais provaram que o ânodo de liga 3-D tem estabilidade interfacial sem precedentes, alcançado por um canal de difusão favorável de zinco na superfície da liga, "Feng disse." O conceito demonstrado neste trabalho colaborativo provavelmente trará uma mudança de paradigma no projeto de ânodos de liga de alto desempenho para baterias aquosas e não aquosas, revolucionando a indústria de baterias. "