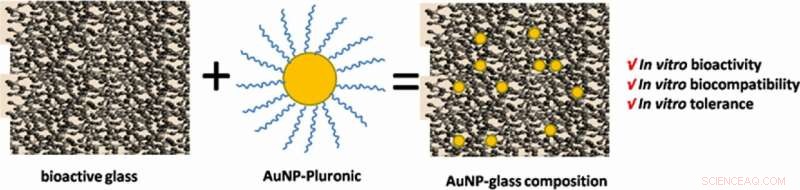
Nanopartículas de ouro incorporadas em vidros bioativos de silicato preparados pelo método sol-gel. Crédito da imagem:Ciência e Engenharia de Materiais:C, Crédito:Materiais Biomédicos, doi:https://doi.org/10.1088/1748-605X/aafd7d
A cura é um processo complexo nas deficiências da pele em adultos, exigindo processos bioquímicos colaborativos para reparo no local. Diversos tipos de células (macrófagos, leucócitos, mastócitos) contribuem para as fases de proliferação associadas, migração, síntese e contração da matriz, juntamente com fatores de crescimento e sinais de matriz no local da ferida. Compreender o controle de sinal e a atividade celular no local pode ajudar a explicar o processo de reparo da pele adulta, além de mero remendo e mais como regeneração, avaliar a biomecânica e implementar estratégias para o reparo acelerado de feridas em medicina regenerativa.
Bioengenheiros, cientistas de materiais e cientistas da vida que estudam a interseção de materiais e medicamentos desenvolveram autoenxertos, aloenxertos e xenoenxertos para cicatrização parcial e total de feridas. As limitações desses procedimentos podem atrasar a cicatrização de grandes áreas de defeitos da pele e é um problema clínico significativo na área de saúde, devido ao risco potencial de antigenicidade e transmissão de doenças. Estratégias de engenharia de tecidos para regeneração da pele é uma abordagem prática que envolve o uso de biomateriais bioativos para angiogênese assistida e revascularização mais rápida.
Em um estudo recente, Sorin Marza e colegas de trabalho nos institutos de pesquisa interdisciplinar e faculdades de física, bio-nanociências, farmácia e remédios, desenvolveu nanopartículas de vidro-ouro bioativas (BG-AuNPs) para promover o crescimento do tecido de granulação e induzir a cicatrização de feridas. No estudo, os cientistas investigaram o impacto dos compósitos BG-AuNP como uma pomada tópica por 14 dias na cicatrização de feridas na pele usando um modelo experimental de rato. Marza et al. desenvolveu um sol-gel de compósitos BGs e BG-AuNP misturados com vaselina em concentrações de 6, 12 e 18 por cento em peso (% em peso) para compreender a resposta de reparo da pele. Os cientistas observaram reações granulomatosas durante o processo de cicatrização nas feridas tratadas com a pomada BG-vaselina. Os resultados agora são publicados em Materiais Biomédicos , Publicação do IOP.
Angiogênese, ou a formação de novos vasos sanguíneos a partir dos vasos existentes é um processo importante durante a regeneração da pele. O vidro bioativo é responsável pelas respostas celulares locais devido à degradação in vivo, estimular a liberação de fatores de crescimento como VEGF (fator de crescimento endotelial vascular) e bFGF (fator de crescimento de fibroblasto básico) para causar um efeito angiogênico. Uma variedade de estudos sobre engenharia de tecidos demonstraram os benefícios do vidro bioativo na cicatrização de feridas, com base em resultados em modelos animais in vivo. Em seu princípio de ação, os cientistas relataram que o vidro bioativo estimulou o processo, controlando a resposta à inflamação para aumentar o efeito parácrino entre macrófagos e células reparadoras.
Nanopartículas de ouro (AuNPs) também estão se tornando importantes na medicina devido às suas propriedades químicas e físicas de biocompatibilidade, modificação de superfície, estabilidade e propriedades ópticas. Apesar de sua tradução inicial desafiadora em abordagens de engenharia de tecidos, uma baixa concentração de AuNPs pode estimular a proliferação celular durante o reparo de feridas. Estudos anteriores da mesma equipe de pesquisa mostraram que o vidro bioativo com AuNPs pode estimular a proliferação de células de queratinócitos humanos (HaCaT), que constituem 95 por cento a 97 por cento da epiderme na superfície da pele. No presente estudo, Marza et al. investigou o potencial de regeneração do tecido dérmico in vivo. No dia 14, eles observaram que as pomadas de vaselina BG e BG-AuNP podem estimular a regeneração completa da pele em modelos experimentais de ratos, substanciado com análises histopatológicas padrão ouro.
Marza et al. AuNPs esféricos recentemente preparados variando de tamanhos de 15 nm a 30 nm, confirmado usando micrografias de microscópio eletrônico de transmissão (TEM) para incorporar na matriz de vidro. Usando padrões de difração de pó de raios-X (XRD) das amostras de vidro, os cientistas investigaram as estruturas amorfas para identificar os centros de cristalização e a assinatura de ouro. Os estudos de caracterização das amostras compostas também incluíram espectroscopia de infravermelho com transformada de Fourier (FTIR), que forneceu espectros típicos para uma rede de silicato. Para desenvolver a pomada de composição de vidro, os cientistas dispersaram os materiais compósitos em pó na vaselina. Eles então usaram espalhamento dinâmico de luz (DLS) para medir as distribuições de tamanho de partícula e corroborar a diferença de tamanhos entre as estruturas de amostra de BG-Vaselina e BG-AuNP-Vaselina.
Após extensa caracterização de materiais, os cientistas conduziram estudos de biofuncionalização in vitro com culturas de células de queratinócitos para verificar a biocompatibilidade antes de realizar procedimentos cirúrgicos em um modelo animal translacional. Como antes, Marza et al. investigou a proliferação de células HaCaT em BG-AuNPs e obteve resultados comparáveis de boa tolerância in vitro durante a proliferação de queratinócitos em ambos os materiais (BG e BG-AuNPs). Os resultados comprovaram os compostos para uso como pomadas para investigações in vivo.
Para avaliar o potencial de cura de BG e BG-AuNPs nas pomadas de vaselina, Mayer et al. compósitos formados de 6, Concentração de 12 e 18 por cento em peso. Para comparação, os cientistas usaram vaselina como controle positivo. Nos modelos de ratos, os cientistas criaram cuidadosamente quatro feridas de excisão de pele ao replicar com sucesso um protocolo de cirurgia de pequenos animais publicado anteriormente. Eles usaram um método específico em cada rato ao aplicar a pomada; (1) a excisão superior esquerda foi mantida como controle sem pomada, (2) na excisão inferior esquerda, os cientistas aplicaram a pomada BG-vaselina, (3) na excisão superior direita, eles aplicaram vaselina sozinha e (4) na excisão inferior direita, eles aplicaram a pomada BG-AuNP-Vaselina.
Os cientistas usaram 30 ratos no estudo com 10 ratos atribuídos a grupos separados (6% BG-vaselina e BG-AuNPs-vaselina pomada; 12% BG / BG-AuNPs-vaselina; 18% BG / BG-AuNPs-vaselina). O protocolo de trabalho foi o mesmo para cada grupo. Após a aplicação da pomada, os cientistas adicionaram bandagens esterilizadas aos locais das feridas em ratos para prevenir a infecção da ferida no pós-operatório e administraram Tramadol por via subcutânea como analgésico. No dia 13, as feridas foram fechadas em todos os animais. Após 14 dias, eles sacrificaram os animais humanamente e conduziram exames histológicos para revelar reações inflamatórias leves e respostas de cicatrização de feridas nos respectivos grupos de animais. Em todos os grupos, a proliferação vascular foi leve a moderada.
Mayer et al. observou especificamente a cura amplamente completa com epiderme intacta, derme e apêndices da pele no grupo de 18 por cento BG-AuNPs-vaselina. Eles também observaram uma falta de proliferação vascular para este grupo, que eles atribuíram à cicatrização avançada e à remodelação vascular tardia. Desta maneira, Mayer et al. extensivamente caracterizou e estabeleceu pomadas de vaselina com base em nanopartículas de ouro e vidro bioativas como materiais promissores para a cicatrização de feridas. A equipe de pesquisa conduzirá estudos adicionais para otimizar a pomada de cicatrização de feridas para investigações em tradução de bancada para cabeceira.
© 2019 Science X Network