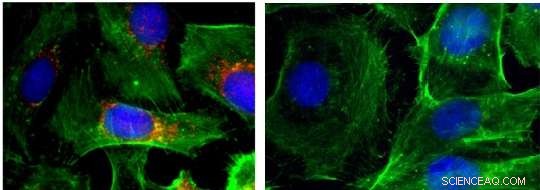
Imagens de imunofluorescência de células (núcleos mostrados em azul; actina mostrado em verde; BRAF mostrado em vermelho). Controle esquerdo; direita:após tratamento com nanopartículas que silenciam o BRAF. Crédito:Jinjun Shi, Hospital Brigham and Women's
Câncer anaplásico de tireoide (ATC), a forma mais agressiva de câncer de tireoide, tem uma taxa de mortalidade de quase 100 por cento e um tempo médio de sobrevivência de três a cinco meses. Uma estratégia promissora para o tratamento desses tumores sólidos e outros é a nanotecnologia de RNA de interferência (RNAi), mas a entrega de agentes de RNAi aos locais dos tumores provou ser um desafio. Investigadores do Hospital Brigham and Women's, junto com colaboradores do Massachusetts General Hospital, desenvolveram uma nanoplataforma inovadora que lhes permite entregar efetivamente agentes de RNAi aos locais do câncer e suprimir o crescimento do tumor e reduzir a metástase em modelos pré-clínicos de ATC. Seus resultados aparecem esta semana em Proceedings of the National Academy of Sciences .
"Chamamos isso de plataforma 'teranóstica' porque reúne uma terapia e um diagnóstico em uma nanopartícula funcional, "disse o co-autor sênior Jinjun Shi, PhD, professora assistente de Anestesia do Departamento de Anestesia. "Esperamos que este estudo abra caminho para o desenvolvimento de plataformas teranósticas para entrega de RNAi guiada por imagem para cânceres avançados."
RNAi, cuja descoberta ganhou o Prêmio Nobel de Fisiologia ou Medicina há 10 anos, permite aos pesquisadores silenciar genes mutantes, incluindo aqueles dos quais os cânceres dependem para crescer, sobreviver e formar metástases. Muitos ATCs dependem de mutações no gene BRAF, comumente mutado. Ao entregar agentes de RNAi que visam especificamente e silenciam este gene mutado, os investigadores esperavam impedir o crescimento e a disseminação do ATC, que muitas vezes metastatiza para os pulmões e outros órgãos.
Quando o RNAi é entregue por conta própria, geralmente é decomposto por enzimas ou filtrado pelos rins antes de atingir as células tumorais. Mesmo quando os agentes de RNAi chegam até o tumor, muitas vezes são incapazes de penetrar ou são rejeitados pelas células cancerosas. Para superar essas barreiras, os pesquisadores usaram nanopartículas para entregar as moléculas de RNAi aos tumores ATC. Além disso, eles acoplaram as nanopartículas com um polímero fluorescente infravermelho próximo, o que lhes permitiu ver onde as nanopartículas se acumulavam em um modelo de rato de ATC.
Ao medir o brilho do polímero fluorescente infravermelho próximo, a equipe verificou que as nanopartículas atingiram o local primário de ATC na tireóide. A equipe descobriu que as nanopartículas circulavam por longos períodos na corrente sanguínea e se acumulavam em altas concentrações nos tumores.
Além disso, a equipe relata evidências de que o BRAF foi silenciado com sucesso nesses locais. Eles descobriram que, para células cultivadas em um prato e tratadas com as nanopartículas contendo agentes de RNAi, o crescimento celular foi drasticamente reduzido e o número de células cancerosas que conseguiram migrar diminuiu em até 15 vezes. Em modelos de mouse, o crescimento do tumor também foi retardado e menos metástases se formaram.
Para traduzir a nova plataforma em aplicações clínicas, a equipe de pesquisa observa a importância de ter um diagnóstico por imagem que lhes permita avaliar rapidamente quais pacientes têm maior probabilidade de se beneficiar da nanoterapêutica de RNAi.
"A maioria dos pacientes que se apresentam a cirurgiões com câncer anaplásico de tireoide está sem opções e esta nova pesquisa dá a esses pacientes algumas opções. Ter uma abordagem que nos permite visualizar rapidamente e, simultaneamente, administrar uma terapia direcionada pode ser fundamental para o tratamento eficiente desta doença e outros cânceres letais com um prognóstico ruim, "disse o co-autor sênior, Sareh Parangi, MD, professor associado do Departamento de Cirurgia do MGH.