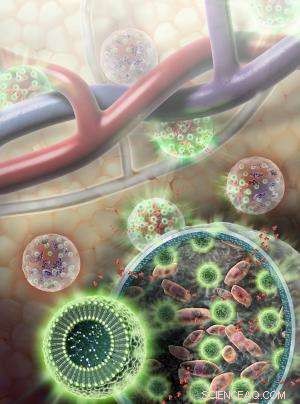
 p Os nanossensores (esferas verdes) são compostos de moléculas de gordura e L-arginina, bem como moléculas indicadoras separadas que emitem sinais detectáveis por ressonância magnética e sinais luminosos quando as células estão vivas. Os nanossensores são colocados em uma membrana de hidrogel junto com as células do fígado (rosa). Nutrientes e outras moléculas relativamente pequenas (vermelhas) são capazes de viajar através da membrana de hidrogel de e para a corrente sanguínea. Crédito:Sayo Studios
p Os nanossensores (esferas verdes) são compostos de moléculas de gordura e L-arginina, bem como moléculas indicadoras separadas que emitem sinais detectáveis por ressonância magnética e sinais luminosos quando as células estão vivas. Os nanossensores são colocados em uma membrana de hidrogel junto com as células do fígado (rosa). Nutrientes e outras moléculas relativamente pequenas (vermelhas) são capazes de viajar através da membrana de hidrogel de e para a corrente sanguínea. Crédito:Sayo Studios
p Os pesquisadores da Johns Hopkins descobriram uma maneira de detectar se as células previamente transplantadas para um animal vivo estão vivas ou mortas, uma inovação, segundo eles, provavelmente acelerará o desenvolvimento de terapias de substituição de células para doenças como insuficiência hepática e diabetes tipo 1. Conforme relatado na edição de março de
Materiais da Natureza , o estudo usou sensores de pH em nanoescala e máquinas de ressonância magnética (MRI) para dizer se as células do fígado injetadas em camundongos sobreviveram ao longo do tempo. p "Esta tecnologia tem o potencial de transformar o corpo humano em menos de uma caixa preta e nos dizer se as células transplantadas ainda estão vivas, "diz Mike McMahon, Ph.D., um professor associado de radiologia da Escola de Medicina da Universidade Johns Hopkins que supervisionou o estudo. "Essa informação será inestimável em terapias de ajuste fino."
p Os avanços da medicina regenerativa dependem de meios confiáveis de substituir células danificadas ou ausentes, como a injeção de células pancreáticas em pessoas com diabetes cujas próprias células não produzem insulina suficiente. Para proteger as células transplantadas do sistema imunológico, ao mesmo tempo que permite o fluxo livre de nutrientes e insulina entre as células e o corpo, eles podem ser envolvidos em membranas de hidrogel antes do transplante. Mas, explica McMahon, "depois de colocar as células, você realmente não tem ideia de quanto tempo eles sobrevivem. "Essas células transplantadas eventualmente param de funcionar na maioria dos pacientes, quem deve retomar o uso de insulina. Nesse ponto, os médicos só podem presumir que as células morreram, mas eles não sabem quando ou por que, diz McMahon.
p Com esse problema em mente, O grupo de McMahon, que é especializada em métodos de detecção de alterações químicas, colaborou com o grupo de pesquisa liderado por Jeff Bulte, Ph.D., o diretor de imagem celular do Hopkins 'Institute for Cell Engineering. O grupo de Bulte inventa maneiras de rastrear células implantadas pelo corpo usando ressonância magnética. Liderado pelo pesquisador Kannie Chan, Ph.D., a equipe desenvolveu um extremamente pequeno, ou nanoescala, sensor preenchido com L-arginina, um suplemento nutricional que responde quimicamente a pequenas mudanças na acidez (pH) causadas pela morte de células próximas. Mudanças na acidez, por sua vez, desencadeariam mudanças nas moléculas do sensor embutidas na fina camada de gordura que compõe a parte externa da nanopartícula, emitindo um sinal que poderia ser detectado por ressonância magnética.
p Para testar como esses nanosensores funcionariam em um corpo vivo, a equipe os carregou em esferas de hidrogel junto com as células do fígado - uma terapia potencial para pacientes com insuficiência hepática - e outro sensor que emite luz bioluminescente apenas enquanto as células estão vivas. As esferas foram injetadas logo abaixo da pele de camundongos. Conforme confirmado pelo sinal de luz, a ressonância magnética detectou com precisão onde as células estavam no corpo e qual proporção ainda estava viva. (Esses indicadores de luz não podem ser usados para rastrear células em humanos porque nossos corpos são muito grandes para os sinais visíveis passarem, mas esses indicadores permitiram à equipe verificar se os nanossensores de ressonância magnética estavam funcionando corretamente nos ratos.)
p "Foi emocionante ver que isso funciona tão bem em um corpo vivo, "Chan diz. A equipe espera que, porque os componentes do sistema - membrana de hidrogel, moléculas de gordura, e L-arginina - são seguros para humanos, adaptar sua descoberta para uso clínico será relativamente simples. "Isso deve eliminar muitas suposições do transplante de células, permitindo que os médicos vejam se as células sobrevivem, e se não, quando eles morrem, "Diz Chan." Dessa forma, eles podem descobrir o que está matando as células, e como evitá-lo. "
p As aplicações potenciais dos sensores não se limitam a células dentro de cápsulas de hidrogel, Notas de Bulte. "Essas nanopartículas funcionariam fora das cápsulas, e eles podem ser emparelhados com muitos tipos diferentes de células. Por exemplo, eles podem ser usados para ver se as células tumorais estão morrendo em resposta à quimioterapia, " ele diz.
