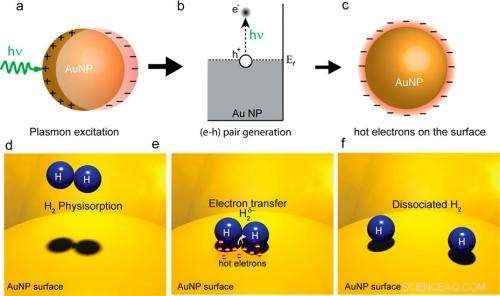
 p Em um), (b), e C), plasmons de superfície excitados por um laser geram elétrons quentes em uma superfície de nanopartícula de ouro. Em (d), (e), e (f), elétrons quentes se transferem para as moléculas de H2 e fazem com que elas se dissociem. Uma vez que a dissociação é a etapa limitante da taxa em muitas reações químicas, este processo de elétron quente pode aumentar a eficiência da reação. Crédito da imagem:Shaunak Mukherjee, et al. © 2012 American Chemical Society
p Em um), (b), e C), plasmons de superfície excitados por um laser geram elétrons quentes em uma superfície de nanopartícula de ouro. Em (d), (e), e (f), elétrons quentes se transferem para as moléculas de H2 e fazem com que elas se dissociem. Uma vez que a dissociação é a etapa limitante da taxa em muitas reações químicas, este processo de elétron quente pode aumentar a eficiência da reação. Crédito da imagem:Shaunak Mukherjee, et al. © 2012 American Chemical Society
p (Phys.org) - Do refino de petróleo ao processamento de alimentos, a grande maioria das aplicações químicas comerciais envolve catalisadores para controlar a taxa de reações químicas. Qualquer coisa que possa aumentar a eficiência dos catalisadores pode ter um impacto generalizado nessas áreas. Em um novo estudo, cientistas mostraram que uma melhoria de eficiência pode ser possível criando elétrons "quentes" (aqueles com uma energia muito alta) de uma superfície metálica na qual ocorre a reação química, e usar os elétrons para controlar a reação química e torná-la mais eficiente. p Os pesquisadores, liderado pelos professores Peter Nordlander e Naomi J. Halas da Rice University em Houston, Texas, e a Professora Emily A. Carter, da Princeton University, Nova Jersey, publicaram seu estudo sobre a técnica para melhorar a química catalítica em uma edição recente da
Nano Letras .
p Em seu método, os pesquisadores usaram um laser de luz visível para iluminar a superfície de uma nanopartícula de ouro (a superfície do catalisador) em temperatura ambiente. A luz do laser que entra excita opticamente os plasmons de superfície na superfície do metal, e os plasmons então decaem em elétrons quentes. Por causa de suas altas energias, os elétrons quentes se estendem mais longe das nanopartículas do que os elétrons com energias mais baixas. Se outro átomo ou molécula que pode aceitar o elétron estiver próximo, o elétron quente pode ser transferido para os estados eletrônicos desse receptor.
p Nestes experimentos, os pesquisadores adsorveram H
2 moléculas na superfície das nanopartículas de ouro, um procedimento que é comumente realizado em catálise heterogênea, em que as moléculas adsorvidas atuam como reagentes. Os pesquisadores descobriram, como resultado principal de seu estudo, que alguns dos elétrons quentes poderiam ser transferidos para as camadas fechadas do H
2 moléculas e fazer com que os dois átomos de hidrogênio se separem, ou dissociar. Este processo, chamado de "dissociação induzida por plasmon de H
2 em Au, "poderia melhorar a eficiência de certas reações químicas.
p "Em muitas reações químicas importantes, a etapa de limitação de taxa é a dissociação de moléculas de invólucro fechado, como uma molécula de hidrogênio, "Nordlander disse
Phys.org . "Se esta etapa de reação puder ser 'tratada' (usando nosso processo de elétrons quentes demonstrado), a reação pode ocorrer muito mais rápido e exigir menos energia. "
p Para medir a dissociação, os pesquisadores expuseram o substrato de nanopartículas a H
2 e D
2 (dois átomos de deutério, um isótopo de hidrogênio contendo um nêutron). Se os elétrons quentes dissociarem essas moléculas, isso resultaria na formação de moléculas de HD. Os pesquisadores descobriram que, assim que ligaram o laser, a taxa de formação de HD na superfície das nanopartículas aumentou em um fator de 6. Eles também mediram que a taxa era fortemente dependente da concentração e do tamanho das nanopartículas de ouro. Os pesquisadores explicaram que, num sentido, os elétrons "fazem o impossível" porque não haveria dissociação sem eles.
p "Uma molécula de hidrogênio adsorvida em uma superfície macroscópica de ouro não se dissocia espontaneamente, mesmo em temperaturas elevadas, "Nordlander disse." É uma reação química impossível. A energia para a dissociação é simplesmente muito grande. Escolhemos o sistema hidrogênio-ouro exatamente por esse motivo. Queríamos um sistema em que a interpretação do efeito fosse direta. Em outros metais, como metais de transição, uma molécula de hidrogênio pode se dissociar espontaneamente, em particular perto de defeitos e a temperaturas elevadas. Mas não em ouro. "
p Esses resultados demonstram como o campo da plasmônica - que envolve interações entre fótons e nanoestruturas - pode ter aplicações no campo da química catalítica, particularmente fotocatálise, Os pesquisadores esperam que esta demonstração da capacidade de controlar reações químicas usando a luz possa ser estendida para usos específicos. Ao usar a frequência do laser para sintonizar as ressonâncias de plasmon de superfície, pode ser possível criar elétrons quentes com energias específicas que povoam estados eletrônicos específicos de moléculas adsorvidas na superfície das nanopartículas.
p "A aplicação imediata é melhorar a eficiência dos catalisadores metálicos, iluminando-os com luz, "Nordlander disse." Nossos grupos têm uma 'agenda verde' e nossa intenção é projetar novos tipos de catalisadores que são movidos pela luz solar. Isso é algo que temos em abundância aqui em Houston.
p "Outra aplicação importante é investigar até que ponto podemos direcionar e controlar reações químicas, transferindo elétrons quentes de determinadas energias para orbitais moleculares específicos. Este é um tópico de pesquisa relativamente inexplorado. Elétrons normais têm energias positivas e são muito mais 'quentes' que nossos elétrons quentes. Esses elétrons de alta energia normalmente não permanecem em uma molécula por tempo suficiente para que os átomos comecem a se mover. " p
Copyright 2012 Phys.org
Todos os direitos reservados. Este material não pode ser publicado, transmissão, reescrito ou redistribuído no todo ou em parte sem a permissão expressa por escrito do Phys.org.
