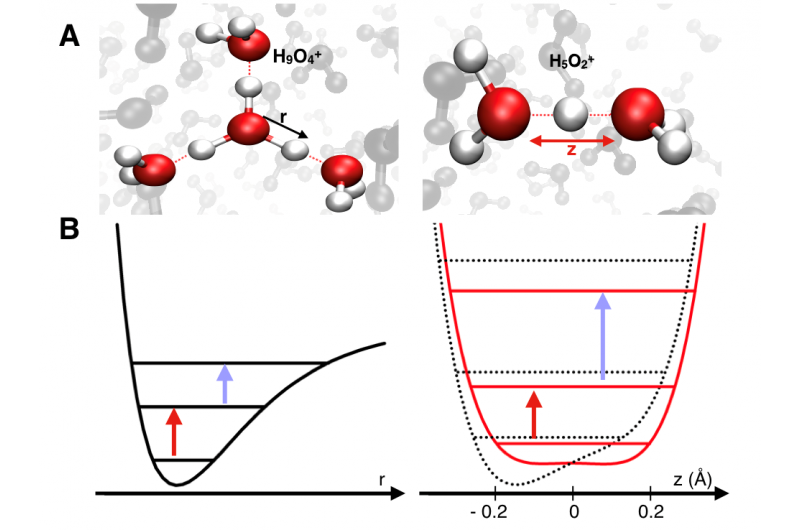
[A] Esquema do cátion Eigen H9O4 + (à esquerda) e do cátion Zundel H5O2 + (à direita). As setas indicam a coordenada de ligação O-H r e a coordenada de transferência de próton (O ... H + ... O) z. No cátion Eigen, uma ligação O-H covalente localiza o próton, enquanto no cátion Zundel o próton é deslocado entre duas moléculas de água. [B] Potencial vibracional anarmônico (esquerda) e potencial mínimo duplo do cátion Zundel ao longo de z (direita, vermelho). Distorções pelo solvente ao redor impõem uma modulação do potencial mínimo duplo (direita, linha pontilhada). Setas vermelhas e azuis indicam transições entre estados quânticos específicos do movimento do próton, ou seja, a transição do estado fundamental para o primeiro estado excitado (vermelho) e a transição do primeiro estado excitado para o segundo estado excitado (azul). A modulação dos potenciais leva a mudanças espectrais das transições vibracionais que são mapeadas por espectroscopia infravermelha bidimensional. Crédito:MBI Berlin
Os processos básicos em química e biologia envolvem prótons em um ambiente aquático. Estruturas aquáticas que acomodam prótons e seus movimentos permaneceram indefinidos até agora. Aplicando espectroscopia vibracional ultrarrápida, pesquisadores mapearam movimentos flutuantes de transferência de prótons e forneceram evidências diretas de que os prótons na água líquida são predominantemente compartilhados por duas moléculas de água. Alongamentos de prótons de femtossegundos dentro de um local de hidratação são de 10 a 50 vezes mais rápidos do que o salto de prótons para um novo local, a etapa elementar de transferência de prótons na química.
O próton, o núcleo carregado positivamente H + de um átomo de hidrogênio e menor espécie química, é um ator chave em química e biologia. Os ácidos liberam prótons em um ambiente de água líquida, onde são altamente móveis e dominam o transporte de carga elétrica. Em biologia, o gradiente de concentração de prótons através das membranas celulares é o mecanismo que conduz a respiração e o armazenamento de energia das células. Mesmo depois de décadas de pesquisa, Contudo, as geometrias moleculares nas quais os prótons são acomodados na água e as etapas elementares da dinâmica dos prótons permaneceram altamente controversas.
Os prótons na água são comumente descritos com a ajuda de duas estruturas limitantes (Fig. 1A). No complexo Eigen (H9O4 +) (à esquerda), o próton é parte do íon H3O + central rodeado por três moléculas de água. No cátion Zundel (H5O2 +) (direita), o próton forma fortes ligações de hidrogênio com duas moléculas de água flanqueadoras. Uma descrição no nível molecular emprega a superfície de energia potencial do próton (Fig. 1B), que é marcadamente diferente para as duas geometrias limitantes. Conforme mostrado na Fig. 1B, espera-se um potencial mínimo único anarmônico para as espécies Eigen e um potencial mínimo duplo para as espécies Zundel. Em água líquida, esses potenciais são altamente dinâmicos por natureza e sofrem flutuações muito rápidas devido aos movimentos térmicos das moléculas de água circundantes e do próton.
Pesquisadores do Instituto Max Born em Berlim, Alemanha, e a Universidade Ben Gurion do Negev em Beer-Sheva, Israel, já elucidaram os movimentos ultrarrápidos e as características estruturais dos prótons na água sob as condições ambientais. Eles relatam resultados experimentais e teóricos em Ciência que identificam o cátion Zundel como uma espécie predominante em água líquida. O femtossegundo (1 fs =10 -15 s) a dinâmica dos movimentos do próton foi mapeada por meio de transições vibracionais entre os estados quânticos do próton (setas vermelhas e azuis na Fig. 1B). O método sofisticado de espectroscopia vibracional bidimensional fornece os contornos amarelo-vermelho e azul na Fig. 2A que marcam a faixa de energia coberta pelas duas transições. O contorno azul ocorre em frequências de detecção mais altas do que o vermelho, dando a primeira evidência direta para o caráter de mínimo duplo do potencial de prótons no ambiente aquoso nativo. Em contraste, espera-se que o contorno azul apareça em frequências de detecção menores do que o vermelho.
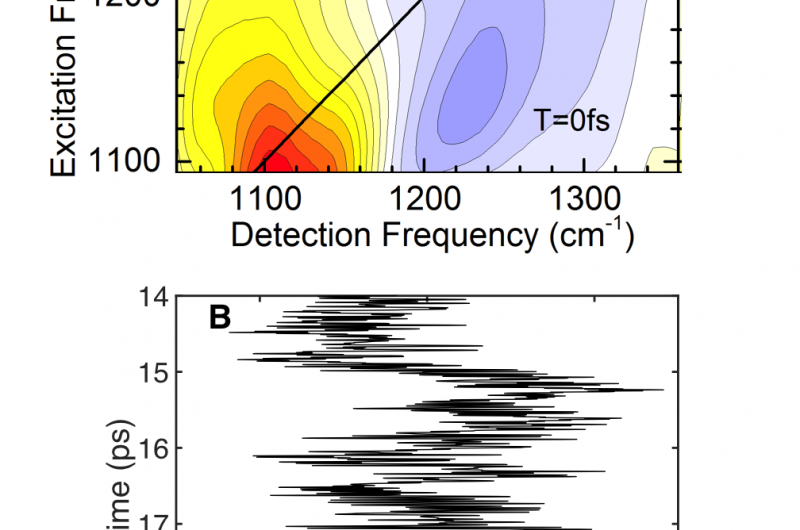
[A] Espectros vibracionais bidimensionais com a transição do estado fundamental para o primeiro estado excitado (vermelho) na frequência de detecção mais baixa do que a transição do primeiro estado excitado para o segundo estado excitado (azul). A orientação de ambos os contornos paralelos ao eixo da frequência de excitação se deve às flutuações de frequência ultrarrápidas e à perda de memória na posição do próton. [B] Dinâmica simulada em tempo real dos movimentos do próton no cátion Zundel. Em menos de 100 fs, o próton exibe grandes excursões de amplitude ao longo de z, a coordenada que liga as duas moléculas de água no cátion Zundel. Devido à modulação ultrarrápida da forma do potencial do próton pelas moléculas de solvente circundantes, o próton explora todos os locais entre as duas moléculas de água. Crédito:MBI Berlin
A orientação dos dois contornos paralelos ao eixo de frequência vertical demonstra que as duas transições vibracionais exploram uma enorme faixa de frequência em menos de 100 fs, uma marca registrada das modulações ultrarrápidas da forma do potencial de prótons. Em outras palavras, o próton explora todos os locais entre as duas moléculas de água em menos de 100 fs e rapidamente perde a memória de onde esteve antes. A modulação do potencial do próton é causada pelo forte campo elétrico imposto pelas moléculas de água no meio ambiente. Seu movimento térmico rápido resulta em fortes flutuações de campo e, portanto, modulações de energia potencial em uma escala de tempo abaixo de 100 fs. Esta imagem é apoiada por experimentos de referência com cátions Zundel seletivamente preparados em outro solvente e por simulações teóricas detalhadas da dinâmica de prótons (Fig. 2B).
Um cátion Zundel específico na água se transforma em novas geometrias de acomodação de prótons pela quebra e reforma das ligações de hidrogênio. Esses processos são muito mais lentos do que o movimento do próton oscilante e ocorrem em uma escala de tempo de alguns picossegundos. Esta nova imagem da dinâmica do próton é altamente relevante para o transporte de prótons pelo conhecido mecanismo de von Grotthuss, e para mecanismos de translocação de prótons em sistemas biológicos.