 p (Esquerda) Módulo experimental japonês KIBO na Estação Espacial Internacional. Os experimentos foram conduzidos em sua cabine pressurizada de novembro de 2013 a junho de 2014 (Foto cedida pela NASA). (À direita) Astronauta japonês Koichi Wakata com Ice Crystal Cell 2 durante sua instalação. Crédito:NASA / JAXA
p (Esquerda) Módulo experimental japonês KIBO na Estação Espacial Internacional. Os experimentos foram conduzidos em sua cabine pressurizada de novembro de 2013 a junho de 2014 (Foto cedida pela NASA). (À direita) Astronauta japonês Koichi Wakata com Ice Crystal Cell 2 durante sua instalação. Crédito:NASA / JAXA
p Nos experimentos de microgravidade na Estação Espacial Internacional (ISS), os cientistas revelaram que a água super-resfriada contendo glicoproteínas anticongelantes acelera e oscila sua taxa de crescimento de cristal de gelo. Esse resultado aparentemente contraditório pode levar a uma melhor compreensão do misterioso efeito anticongelante nos organismos vivos. p Os peixes podem sobreviver mesmo em ambientes abaixo de zero, como sob blocos de gelo. Os pesquisadores levantaram a hipótese de que, quando as glicoproteínas contidas no sangue dos peixes são absorvidas na superfície dos cristais de gelo, ele restringe o crescimento de cristais de gelo. A verificação das funções dessas glicoproteínas requer medições precisas das taxas normais de crescimento dos cristais ao longo do tempo. No entanto, é difícil fazer isso na Terra por causa do fluxo convectivo natural em torno do cristal em crescimento, induzido pela gravidade.
p Os pesquisadores, liderado pelo professor emérito Yoshinori Furukawa da Universidade de Hokkaido, esperava usar as condições de microgravidade do espaço para medir com precisão as taxas de crescimento normais das faces do cristal, como fluxo convectivo não ocorre neste ambiente.
p Para realizar os experimentos na ISS, O Instituto de Ciência de Baixa Temperatura da Universidade de Hokkaido e a JAXA desenvolveram em conjunto o Ice Crystal Cell 2, um dispositivo para medir a velocidade de crescimento do cristal de gelo no espaço. Uma vez instalado no módulo experimental japonês KIBO, experimentos foram realizados controlando o dispositivo usando sinais do solo.
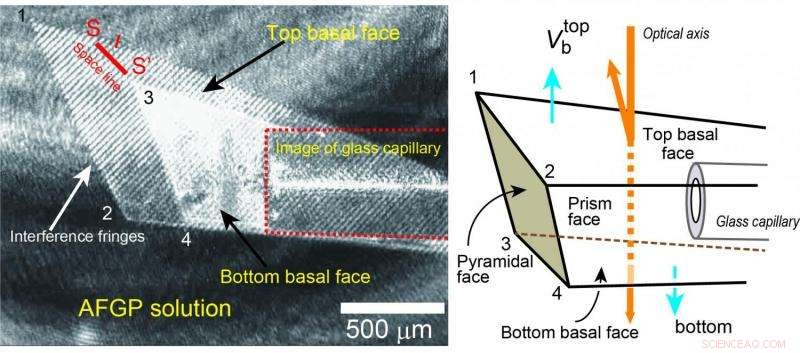 p (Esquerda) Um instantâneo de um vídeo do crescimento de cristais de gelo. Os padrões listrados no centro mostram as faces basais inferiores. Esses padrões são franjas de interferência produzidas pela luz refletida na face basal. A velocidade com que esses movimentos se movem foi usada para calcular a velocidade de crescimento da face basal inferior. (À direita) Uma ilustração que mostra a geometria tridimensional do cristal de gelo. Crédito:Universidade de Hokkaido
p (Esquerda) Um instantâneo de um vídeo do crescimento de cristais de gelo. Os padrões listrados no centro mostram as faces basais inferiores. Esses padrões são franjas de interferência produzidas pela luz refletida na face basal. A velocidade com que esses movimentos se movem foi usada para calcular a velocidade de crescimento da face basal inferior. (À direita) Uma ilustração que mostra a geometria tridimensional do cristal de gelo. Crédito:Universidade de Hokkaido
p Os pesquisadores conduziram 124 experimentos, dos quais 22 foram considerados como tendo medido com precisão as taxas de crescimento de cristais de gelo em água super-resfriada contendo uma impureza de glicoproteína. Os resultados mostraram que as faces basais do fundo dos cristais de gelo cresceram três a cinco vezes mais rápido do que na água pura. Os cristais de gelo também exibiam oscilações periódicas à medida que cresciam. “Os resultados foram contrários ao que se esperava, como a glicoproteína realmente facilitou o crescimento de cristais de gelo, ao invés de restringi-lo, "diz Ken Nagashima da equipe de pesquisa.
p O que, então, explica o efeito anticongelante da glicoproteína? Os pesquisadores descobriram o processo complicado no qual faces planas de cristal com altas taxas de crescimento eram truncadas por faces com taxas de crescimento mais lentas, fazendo com que o cristal poliédrico seja cercado apenas por faces planas com as taxas de crescimento mais baixas. Isso resultou em uma grande desaceleração do crescimento dos cristais de gelo.
p "Nossos resultados sugerem que a prevenção do congelamento em organismos vivos não pode ser explicada apenas pelo efeito de depressão do crescimento das glicoproteínas. Em outras palavras, o novo mecanismo que observamos é essencial para evitar que os organismos vivos congelem, "diz Nagashima." A função das glicoproteínas no crescimento do cristal de gelo está intimamente ligada à forma como os biopolímeros regulam o crescimento de vários cristais inorgânicos. Uma melhor compreensão disso pode levar à criação de novos materiais, " ele adicionou.

