Cientistas identificam classe de moléculas de ligação que podem ser usadas para degradação proteica direcionada
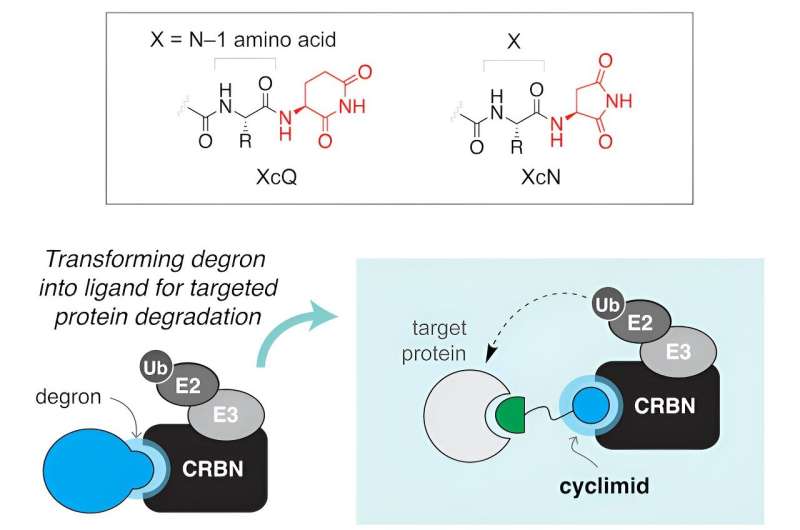 Resumo gráfico. Crédito:Biologia Química Celular (2024). DOI:10.1016/j.chembiol.2024.01.003
Resumo gráfico. Crédito:Biologia Química Celular (2024). DOI:10.1016/j.chembiol.2024.01.003 Na batalha contra o cancro e outras doenças, os cientistas estão a desenvolver armas moleculares que podem ser usadas para impedir o crescimento celular incontrolável.
Uma equipe de cientistas do Hospital Geral de Harvard e Massachusetts descobriu que as "ciclimidas", uma classe de moléculas de ligação conhecidas como ligantes, oferecem uma abordagem promissora e eficiente para remover proteínas causadoras de doenças ou com mau funcionamento. Suas propriedades distintas permitem aos cientistas atacar proteínas errantes em suas raízes moleculares.
"Por mais de um ano, abordamos a questão de quais são os ligantes naturais reconhecidos pelo cereblon, uma proteína crucial para a degradação direcionada", disse a coautora sênior Christina Woo, professora associada de Química e Biologia Química de Morris Kahn. "Este estudo caracteriza de forma abrangente esses ligantes para fornecer novos insights para a biologia do cereblon e como sequestrá-lo."
Nos últimos anos, os cientistas desenvolveram pequenas moléculas para atingir especificamente proteínas associadas a doenças. Estas moléculas têm duas funções:fixam-se à proteína alvo que precisa de ser removida e a sua “ogiva” interage com parte do sistema de limpeza celular, muitas vezes ligando-se a uma proteína chamada cereblon. Juntas, essas moléculas especializadas formam o que os cientistas chamam de complexo ternário. Uma vez estabelecido este complexo, a proteína alvo é efetivamente marcada para eliminação pelo proteassoma da célula, que atua como um sistema de reciclagem celular.
O sucesso deste processo – remoção de proteínas específicas – depende do desenho e da eficiência da ogiva molecular, tornando-as elementos cruciais no desenvolvimento de terapias para diversas doenças, incluindo o cancro.
 Cristina Woo (centro) em seu laboratório com os coautores do estudo Nandini Vallavoju (da esquerda), Wenqing Xu, Ralph Mazitschek e Connor Payne. Crédito:Kris Snibbe/fotógrafo da equipe de Harvard
Cristina Woo (centro) em seu laboratório com os coautores do estudo Nandini Vallavoju (da esquerda), Wenqing Xu, Ralph Mazitschek e Connor Payne. Crédito:Kris Snibbe/fotógrafo da equipe de Harvard
No artigo dos pesquisadores publicado na Cell Chemical Biology , eles descobriram que pequenas alterações estruturais no ligante cereblon podem alterar dramaticamente as atividades biológicas nas células. Em colaboração com o Laboratório Mazitschek, que realizou extensas pesquisas sobre a identificação de alvos moleculares relevantes para doenças, os pesquisadores introduziram uma abordagem bioquímica sistemática para quantificar a formação de complexos ternários. Este método permite aos pesquisadores prever a atividade de degradação celular dos ciclídeos de forma mais eficaz, agilizando o processo de desenvolvimento.
“Demos à comunidade um microscópio poderoso e acessível com nosso método”, disse Ralph Mazitschek, co-autor sênior. "Estabelecemos uma plataforma de criação de perfil abrangente, confiável, robusta e sensível que é aplicável a praticamente qualquer um desses degradadores de moléculas pequenas e degradadores de cola molecular."
“Esta foi uma colaboração no verdadeiro sentido da palavra”, disse Connor Payne, pós-doutorado no laboratório de Mazitschek. "Tínhamos conhecimentos diferentes e tecnologias diferentes que estávamos desenvolvendo, então a sinergia entre eles era muito, muito bonita de se ver concretizada."
No futuro, Woo e Mazitschek estão optimistas de que os cilimídeos e as suas plataformas de rastreio serão incorporados em estratégias de degradação de proteínas, o que poderá ser útil no desenvolvimento de medicamentos e no tratamento do cancro.
"Acho que nossa pesquisa acabará por facilitar o perfil de muito mais moléculas contra os alvos desejados e chegar mais rapidamente a moléculas mais seletivas e eficazes", disse Woo. "Há muitas direções diferentes que isso pode nos levar."

