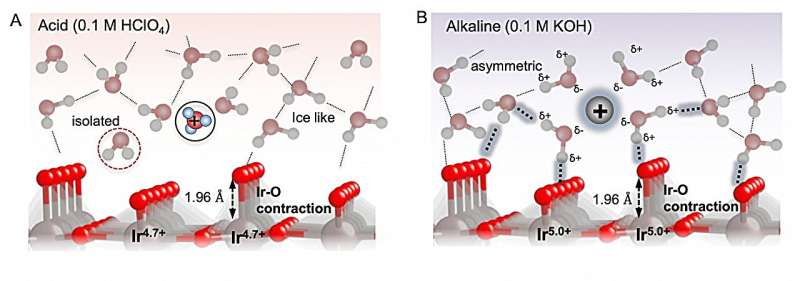
 Esquema da interface eletroquímica sob ácido 0,1 M HClO4 eletrólito (A) e eletrólito alcalino 0,1 M KOH (B) durante a oxidação da água a ~ 1,5 VRHE. Crédito:Journal of the American Chemical Society (2024). DOI:10.1021/jacs.3c12011
Esquema da interface eletroquímica sob ácido 0,1 M HClO4 eletrólito (A) e eletrólito alcalino 0,1 M KOH (B) durante a oxidação da água a ~ 1,5 VRHE. Crédito:Journal of the American Chemical Society (2024). DOI:10.1021/jacs.3c12011 Os catalisadores de óxido de irídio são eficazes para a oxidação da água, tornando-os muito atraentes para tecnologias verdes. Uma equipe que inclui pesquisadores do SANKEN (Instituto de Pesquisa Científica e Industrial) da Universidade de Osaka analisou mais de perto como eles funcionam.
Em um estudo publicado no Journal of the American Chemical Society a equipe usou espectroscopia para revelar como as espécies químicas envolvidas na reação de evolução de oxigênio (OER) catalisada por óxido de irídio interagem com a solução ao seu redor.
Os REA são importantes em muitos processos de energia limpa, como a transformação de dióxido de carbono em combustíveis líquidos utilizáveis e a geração de hidrogênio verde a partir da eletrólise da água. Ambos os processos serão cruciais num futuro sem combustíveis fósseis. Portanto, compreender completamente os REA é um importante foco de pesquisa.
Os processos catalíticos podem ser complexos com várias espécies intermediárias envolvidas na passagem do material de partida ao produto desejado. As técnicas Operando permitem que esses intermediários sejam investigados usando espectroscopia durante a reação, fornecendo uma janela para o que realmente está acontecendo.
Usando um eletrodo com superfície de óxido de irídio, os pesquisadores investigaram a oxidação de moléculas de água em soluções com diferentes valores de pH.
"A interação entre a superfície do eletrodo e os intermediários oxigenados é fundamental para a eficiência do REA, portanto, a otimização do material catalisador geralmente tem sido o foco", explica a autora sênior Reshma R. Rao, do Imperial College London.
"No entanto, as observações até o momento deixaram questões sem resposta, por isso analisamos mais de perto o lado da solução da interface usando espectroscopia operando UV-Vis, espectroscopia de absorção de raios X e espectroscopia infravermelha de superfície aprimorada."
Para obter uma reação eficiente, a ligação dos intermediários da reação ao eletrodo deve ser correta para permitir que os intermediários interajam com o eletrodo, mas não tão forte a ponto de ficarem presos ao eletrodo e não conseguirem reagir. Os pesquisadores descobriram que a ligação era controlada por interações de longo alcance entre os intermediários através da solução e isso dependia do pH.
Em condições alcalinas, a água próxima ao eletrodo influenciou as interações de longo alcance entre as espécies oxigenadas, o que afetou sua ligação à superfície. Assim, embora os intermediários se liguem mais fortemente a pH mais elevado, as interações facilitadas pela água interfacial desestabilizam as espécies oxigenadas e permitem que a reação ocorra.
"O uso de espectroscopia operando e técnicas complementares para obter uma visão direta das espécies envolvidas nos permitiu ampliar a compreensão do desempenho do catalisador além da ligação do eletrodo", diz o autor sênior Yu Katayama. "Acreditamos que tal percepção será a chave para otimizar a cinética dos REA."
As descobertas contribuirão para aumentar a eficiência da oxidação da água para a produção de hidrogênio verde. Além disso, combinar a espectroscopia operando com técnicas complementares pode ser útil para a compreensão da catálise de muitos outros processos.
