Catalisadores de Mn baratos e reutilizáveis proporcionam alquilação eficiente de cetonas com álcoois
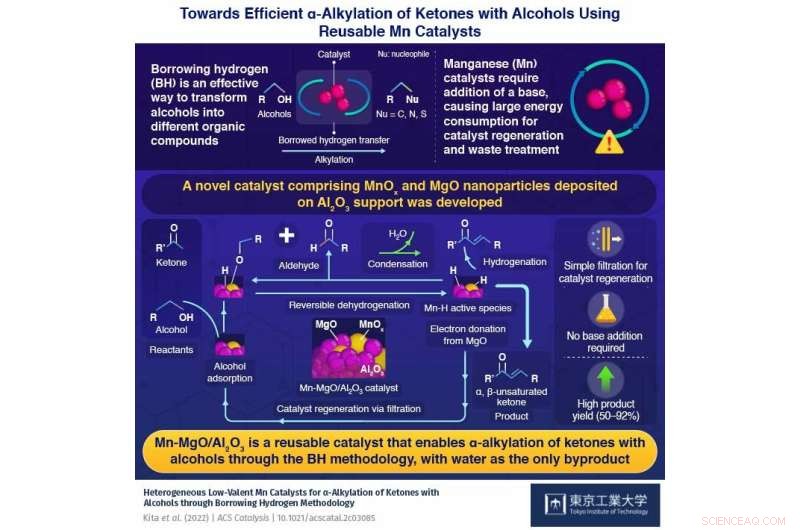
Resumo gráfico. Crédito:Tokyo Tech
Ao sintetizar novos compostos, é vantajoso ter reagentes amplamente disponíveis e um método simples que produza um alto rendimento de produtos com pouco desperdício (subprodutos indesejáveis). Nesse sentido, a alquilação de álcoois por meio de um método conhecido como "empréstimo de hidrogênio" (BH) pode transformar álcoois em uma gama diversificada de produtos, tendo a água como único subproduto.
A reação é centrada em torno de um catalisador e começa com um catalisador removendo os átomos de hidrogênio do álcool para oxidá-lo em um composto carbonílico. Este intermediário altamente reativo sofre então uma reação de condensação com diferentes compostos orgânicos para produzir água e recebe o hidrogênio de volta do catalisador para formar o produto final.
Assim, por "emprestar" átomos de hidrogênio, os grupos alquil do álcool podem ser facilmente transferidos para uma nova molécula orgânica contendo diferentes substituintes. Esforços têm sido feitos para fazer essa reação funcionar com catalisadores de manganês (Mn) biocompatíveis e baratos. No entanto, os catalisadores de Mn atualmente disponíveis requerem a adição de bases fortes, que geram mais resíduos e complicam o processo de regeneração do catalisador.
Agora, em um novo estudo publicado na
ACS catálise , pesquisadores do Instituto de Tecnologia de Tóquio (Tokyo Tech) sintetizaram um catalisador de Mn reutilizável que pode realizar reações de alquilação de álcoois de forma eficiente sem a necessidade de uma base. A equipe de pesquisa, liderada pelo professor assistente Yusuke Kita, havia experimentado anteriormente com catalisadores de rutênio de metal precioso para realizar a alquilação de álcoois pelo método BH.
Eles descobriram que a adição de óxido de magnésio (MgO) ao catalisador melhorou sua capacidade de hidrogenação. Imaginando se o MgO teria o mesmo efeito em catalisadores à base de Mn, eles co-depositaram óxido de Mn (MnO
x ) e nanopartículas de MgO em um óxido de alumínio (Al
2 O
3 ) Apoio, suporte.
Para seu deleite, o novo catalisador facilitou com sucesso a reação de alquilação para uma ampla variedade de cetonas com álcoois, atingindo rendimentos de 50 a 92%. Além disso, ao contrário dos catalisadores de Mn convencionais, ele foi capaz de alquilar substratos contendo cetona, como grupos ciano, que de outra forma reagiriam com água na presença de uma base.
Mais importante ainda, como a reação não produziu nenhum subproduto além da água, o catalisador pode ser facilmente regenerado com um método de filtração simples. "O catalisador atual não exigiu a adição de bases fortes homogêneas que são normalmente indispensáveis para essas reações e exigem grande consumo de energia para separação, reciclagem e tratamento de resíduos", diz o Dr. Kita.
A equipe atribuiu a alta atividade catalítica observada ao contato próximo entre o MnO
x e as nanopartículas de MgO. Usando a espectroscopia de infravermelho com transformada de Fourier, um método que pode identificar compostos químicos medindo a quantidade de luz que eles absorvem, os pesquisadores identificaram, pela primeira vez, uma espécie de hidreto de Mn (Mn-H) na superfície do catalisador, sugerindo que o MgO facilita a transferência eficiente de hidrogênio.
"A catálise é devido a partículas de MgO que coexistem com o MnO
x espécies no Al
2 O
3 apoio e a doação de elétrons de MgO para MnO
x aumenta a reatividade das espécies de Mn-H", explica o Dr. Kita.
Como um catalisador econômico e facilmente reutilizável, o Mn-MgO/Al
2 O
3 poderia, portanto, acelerar a adoção de reações de alquilação via BH e ajudar a produzir diversos compostos orgânicos de maneira ecologicamente correta.
+ Explorar mais Nova abordagem sinérgica de catalisador de átomo único quebra a limitação de atividade dos predecessores
