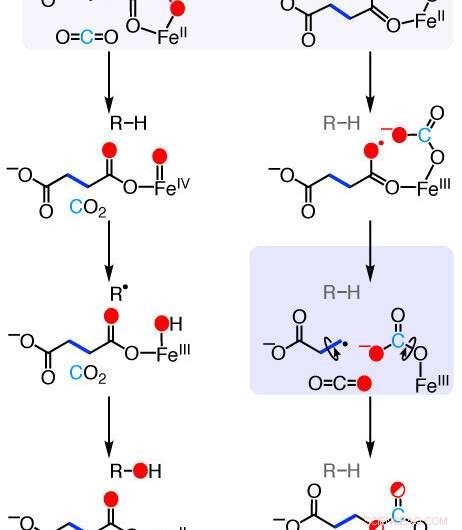
Mecanismos das reações da enzima formadora de etileno (EFE). Uma nova pesquisa apresenta as etapas químicas usadas por essa enzima que ocorre naturalmente para converter um composto químico comum em etileno - um hormônio vegetal importante para o amadurecimento de frutas e um produto químico industrial usado na produção de plásticos e têxteis. Crédito:Rachelle Copeland, Estado de Penn
Uma nova pesquisa apresenta as etapas químicas usadas por uma enzima que ocorre naturalmente para converter um composto químico comum em etileno - um hormônio vegetal importante para o amadurecimento de frutas e um produto químico industrial usado na produção de plásticos e têxteis. Um artigo que descreve a pesquisa de cientistas da Penn State aparece online em 12 de agosto no jornal Ciência .
"Como o etileno é tão importante na indústria de manufatura para fazer plásticos, solventes e têxteis, é um dos compostos mais abundantemente produzidos na Terra, "disse Rachelle Copeland, recém-graduado em doutorado pela Penn State e primeiro e co-autor do artigo. "Atualmente, o petróleo é nossa principal fonte de eteno para esses usos. Contudo, as plantas e alguns micróbios produzem etileno naturalmente. Entender o processo químico passo a passo usado por essas plantas e micróbios pode nos ajudar a abandonar a produção de etileno à base de petróleo. "
A apropriadamente chamada "enzima formadora de etileno (EFE)" é capaz de transformar um composto químico comum - 2-oxoglutarato, que é encontrado em quase todos os organismos onde desempenha um papel no metabolismo - em etileno, mas os pesquisadores não conseguiram caracterizar com precisão o mecanismo empregado pela enzima. A reação necessária para essa transformação é fundamentalmente diferente das reações conduzidas por enzimas intimamente relacionadas ao EFE.
As enzimas são proteínas que iniciam ou aceleram as reações químicas necessárias para sustentar a vida, a maioria dos quais requer átomos, aglomerados de átomos, ou pequenas moléculas - conhecidas coletivamente como cofatores - para fazer essas reações acontecerem. EFE pertence a uma classe de enzimas que promovem reações de vários tipos de moléculas com oxigênio, habilitado por um cofator de ferro e co-substrato de 2-oxoglutarato.
"Nosso grupo de laboratório tem estudado enzimas relacionadas ao EFE por quase 20 anos, "disse Carsten Krebs, professor de química e de bioquímica e biologia molecular na Penn State e autor do artigo. "O EFE é único nesta família de enzimas porque decompõe o 2-oxoglutarato de duas maneiras diferentes. A primeira é bem caracterizada, mas o segundo, aquele que produz etileno, tem sido um mistério até agora. "
A equipe de pesquisa dissecou a via química para a formação de etileno por EFE inserindo isótopos - átomos que diferem em peso atômico e podem ser rastreados conforme a reação está em andamento - em vários produtos. Dessa forma, a equipe poderia rastrear átomos individuais para ver onde eles vão no decorrer da reação. Separadamente, eles também fizeram modificações químicas na enzima e no 2-oxoglutarato para ver como a reação e os produtos foram alterados.
"Usando essas técnicas, pudemos ver que o EFE inicia a reação entre o 2-oxoglutarato e o oxigênio de uma maneira muito diferente de outras enzimas relacionadas, "disse Copeland." Ele insere o oxigênio entre dois átomos de carbono do 2-oxoglutarato, que produz um composto intermediário único que a enzima então decompõe em etileno. "
A localização do átomo de oxigênio inserido havia sido prevista computacionalmente, mas não havia sido mostrada experimentalmente até agora.
"Vários mecanismos foram propostos ao longo dos anos para explicar como o EFE converte 2-oxoglutarato em etileno, mas não houve dados experimentais para distingui-los, "disse J. Martin Bollinger Jr., professor de química e de bioquímica e biologia molecular na Penn State e autor do artigo. "Rachelle projetou esses experimentos para examinar os aspectos mais fundamentais da reação. Para onde vão os átomos individuais? E traça um mecanismo inequivocamente claro."