A troca dependente de potencial auxilia na separação da água usando catalisadores de óxido de cobalto
 p Um interruptor dependente de potencial auxilia na separação da água usando catalisadores de óxido de cobalto, Pesquisadores do Boston College e da Yale University relatam na revista Chem. Uma pequena carga elétrica conduz uma reação de evolução de oxigênio que usa água para produzir gás hidrogênio. Crédito: Chem
p Um interruptor dependente de potencial auxilia na separação da água usando catalisadores de óxido de cobalto, Pesquisadores do Boston College e da Yale University relatam na revista Chem. Uma pequena carga elétrica conduz uma reação de evolução de oxigênio que usa água para produzir gás hidrogênio. Crédito: Chem
p Usando cobalto abundante e uma abordagem experimental única para investigar maneiras de acelerar uma reação catalítica lenta para coletar hidrogênio da água, pesquisadores do Boston College e da Yale University descobriram uma mudança mecanística na reação de evolução do oxigênio, um passo significativo para otimizar eletrocatalisadores para separação de água para produzir energia limpa. p O mecanismo muda variando a quantidade de voltagem, ou potencial aplicado, a equipe relata no jornal
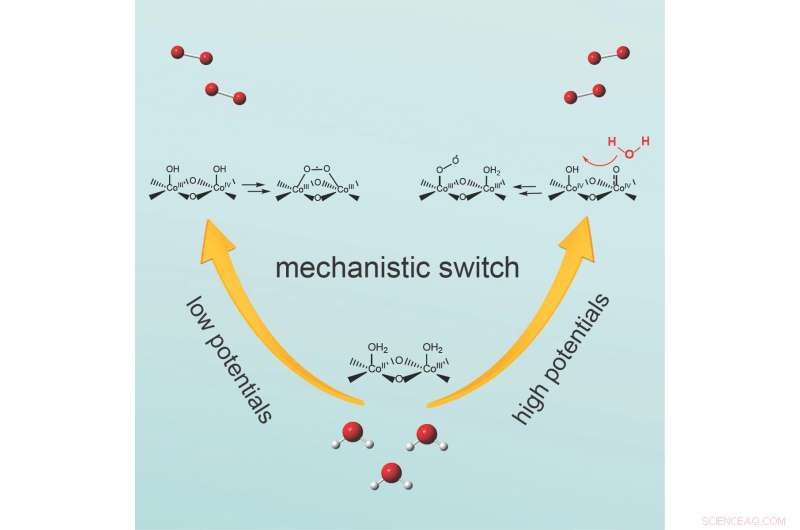
Chem . Em potencial moderado, dois átomos de oxigênio ligados à superfície do catalisador reagem para formar a ligação oxigênio-oxigênio. Por contraste, em potenciais mais elevados, a ligação oxigênio-oxigênio é formada por uma molécula de água que ataca uma espécie de oxigênio ligada à superfície.
p Os resultados mostram que nesta classe de materiais, um eletrocatalisador para esta reação deve ser escolhido, ou otimizado, dependendo do regime potencial em que se espera operar em um reator. Em outras palavras, um determinado catalisador pode ser particularmente eficiente na promoção de um mecanismo, mas não o outro.
p "O que nos surpreendeu foi o quão abruptamente ocorre a mudança de um regime mecanicista para outro com potencial aplicado, "disse o professor de química do Boston College, Dunwei Wang, um dos principais autores do relatório. “Apenas cerca de 100 mV são necessários para alternar entre os dois mecanismos. É um lembrete de como os mecanismos de reação são sensíveis. a troca fácil pode ser outra indicação de como a fotossíntese pode se adaptar às mudanças no ambiente de reação para um desempenho otimizado. "
p Os pesquisadores têm trabalhado para dividir a água em hidrogênio e oxigênio molecular em um esforço para fornecer energia renovável abundante na forma de gás hidrogênio transportável e armazenável. A divisão pode ser realizada com eletrocatálise, um processo no qual as reações de evolução de hidrogênio e oxigênio ocorrem em compartimentos separados espacialmente nos eletrodos. Isso torna a eletrocatálise um meio altamente promissor para a produção de gás hidrogênio limpo.
p Contudo, a reação de evolução de oxigênio (OER) é lenta, disse Wang. Como resultado, a taxa da reação geral de divisão da água é limitada pelo lento OER. A reação precisa ser facilitada por catalisadores, isso é, materiais que promovem a reação sem serem eles próprios consumidos no processo. A data, eletrocatalisadores economicamente viáveis para a promoção da reação de evolução de oxigênio ainda não foram desenvolvidos. Wang e seus colegas se concentraram no OER em eletrocatalisadores promissores em um esforço para entender melhor os processos de reação e usar esses conhecimentos para projetar eletrocatalisadores mais eficientes e estáveis para essa reação.
p Eles se concentraram na reação em uma classe de eletrocatalisadores que são baseados em óxidos de cobalto, um material barato e abundante em terra, atributos que seriam traduzidos de forma eficiente para uso em escala industrial, Disse Wang.
p Na última década, vários eletrocatalisadores à base de óxido de cobalto surgiram como candidatos promissores para promover o REA. Em colaboração com colegas da Universidade de Yale, Wang e sua equipe estudaram o REA em dois tipos de eletrocatalisadores de óxido de cobalto com técnicas eletroquímicas, espectroscopia infravermelha, e teoria do funcional da densidade.
p Wang disse que a equipe controlou a concentração de água usando eletrólitos de água em sal, que apresentam uma concentração de sal cerca de dez vezes superior à da água do mar. Como resultado, os pesquisadores conseguiram controlar a atividade da água ajustando a quantidade de sal no eletrólito. Eles monitoraram como a taxa de reação respondeu a diferentes concentrações de água. Isso revelou o mecanismo do OER em eletrocatalisadores à base de cobalto, Disse Wang. O co-autor e professor associado de química da BC Matthias Waegele e sua equipe de pesquisa usaram a espectroscopia infravermelha, que depende da interação da luz infravermelha com as moléculas, para detectar intermediários de reação do OER sob condições operacionais.
p Eles foram capazes de detectar um intermediário de reação chave, que foi previsto pelos cálculos do químico de Yale Victor Batista e seu grupo de pesquisa. Gary Brudvig, um químico inorgânico em Yale, também assessorou a equipe durante o projeto.
p Wang disse que a equipe queria observar de perto a reação de evolução do oxigênio, particularmente a característica de ser um processo passo a passo, nem um único evento. A água contém apenas um átomo de oxigênio. O produto do REA é o oxigênio molecular, que contém dois átomos de oxigênio. Portanto, durante o OER, uma ligação oxigênio-oxigênio é formada, ele notou.
p Wang disse que os pesquisadores neste campo se concentraram em duas questões centrais:como essa ligação de oxigênio se forma e em que etapa? Dois mecanismos principais foram propostos em estudos anteriores, no entanto, os pesquisadores ainda não tinham resolvido sob quais condições experimentais - temperatura, ou potencial de eletrodo aplicado, por exemplo - as formas de ligação oxigênio-oxigênio e qual dos mecanismos é o dominante.
p Wang e seus colegas decidiram observar de perto como o potencial do eletrodo aplicado dita o mecanismo da etapa de formação da ligação oxigênio-oxigênio, uma vez que as reações na eletrocatálise são acionadas por um potencial elétrico que é aplicado ao catalisador.
p Os resultados sugerem que a chave mecanística pode ser geral para eletrocatalisadores à base de óxido, Disse Wang.
p "Estamos muito interessados em saber se esta observação também se aplica a outros eletrocatalisadores promissores, "disse ele." Em particular, estamos trabalhando atualmente em catalisadores com centros ativos atomicamente definidos. Em contraste com os eletrocatalisadores à base de cobalto, cuja estrutura atômica no centro ativo permanece não resolvida, nossa nova plataforma de estudo contém centros catalíticos que são atomicamente bem definidos. Será muito interessante ver se a troca mecanística induzida por potencial também ocorre nesses catalisadores. "
