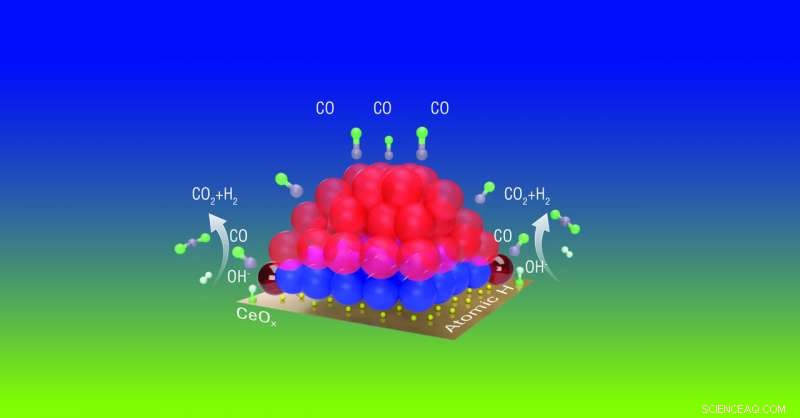
Cientistas estudando um catalisador de reação de deslocamento de gás água feito de átomos de platina (vermelho e azul) em um óxido de cério (C e O x ) superfície descobriu que apenas alguns átomos de platina ao redor da periferia da nanopartícula (vermelho escuro brilhante) são ativados para participar da reação. Esses átomos de platina ativados transferem oxigênio dos grupos OH (originalmente das moléculas de água) para o monóxido de carbono (CO), transformando-o em CO 2 , deixando o H se combinar com o hidrogênio atômico para formar H 2 . Compreender essas dinâmicas pode ajudar os cientistas a projetar catalisadores que requerem menos átomos de platina. Crédito:Laboratório Nacional de Brookhaven
Cientistas do Laboratório Nacional Brookhaven do Departamento de Energia dos EUA, Stony Brook University (SBU), e outras instituições colaboradoras descobriram dinâmicas, detalhes em nível atômico de como um importante catalisador à base de platina funciona na reação de deslocamento de gás água. Esta reação transforma o monóxido de carbono (CO) e água (H 2 O) em dióxido de carbono (CO 2 ) e gás hidrogênio (H 2 ) - uma etapa importante na produção e purificação de hidrogênio para múltiplas aplicações, incluindo o uso como combustível limpo em veículos com células de combustível, e na produção de hidrocarbonetos.
Mas como a platina é rara e cara, os cientistas têm buscado maneiras de criar catalisadores que usem menos desse metal precioso. Entender exatamente o que a platina faz é uma etapa essencial.
O novo estudo, publicado em Nature Communications , identifica os átomos envolvidos no sítio ativo do catalisador, resolver relatórios conflitantes anteriores sobre como o catalisador opera. Os experimentos fornecem evidências definitivas de que apenas certos átomos de platina desempenham um papel importante na conversão química.
"Parte do desafio é que o próprio catalisador tem uma estrutura complexa, "explicou o autor principal Yuanyuan Li, um cientista pesquisador do Departamento de Ciência de Materiais e Engenharia Química da SBU, que tem uma nomeação como convidado na Divisão de Química do Laboratório de Brookhaven e trabalha sob a orientação de Anatoly Frenkel, nomeado em conjunto pela Brookhaven / SBU.
"O catalisador é feito de nanopartículas de platina (aglomerados de átomos de platina) assentados em uma superfície de óxido de cério (céria). Alguns desses átomos de platina estão na superfície das nanopartículas, alguns estão no centro; alguns estão na interface com ceria, e alguns deles estão no perímetro - as bordas externas - dessa interface, "Li disse." Essas posições e como você coloca as partículas na superfície podem influenciar quais átomos irão interagir com o suporte ou com as moléculas de gás, porque alguns estão expostos e outros não. "
Experimentos anteriores produziram resultados conflitantes sobre se as reações ocorrem nas nanopartículas ou em átomos de platina isolados, e se os locais ativos são carregados positiva ou negativamente ou neutros. Detalhes de como o suporte de céria interage com a platina para ativá-la para atividade catalítica também não eram claros.
"Queríamos responder a essas questões, "disse Li." Para identificar o site ativo e determinar o que realmente está acontecendo neste site, é melhor se pudermos investigar este tipo de catalisador em nível atômico, "ela notou.
O time, que incluiu cientistas do Centro de Nanomateriais Funcionais de Brookhaven (CFN) e outras instituições nos EUA e na Suécia, usou uma série de técnicas para fazer exatamente isso. Eles estudaram o catalisador sob condições de reação e, inesperadamente, capturou um efeito peculiar que ocorreu quando os catalisadores atingiram seu estado ativo em condições de reação.
"Os átomos de platina no perímetro das partículas estavam 'dançando' dentro e fora de foco em um experimento de microscopia eletrônica realizado por nossos colaboradores, enquanto o resto dos átomos eram muito mais estáveis, "Frenkel disse. Tal comportamento dinâmico não foi observado quando alguns dos reagentes (CO ou água) foram removidos da corrente de moléculas reagentes.
"Descobrimos que apenas os átomos de platina no perímetro da interface entre as nanopartículas e o suporte de céria fornecem a atividade catalítica, "Li disse." As propriedades dinâmicas nesses locais de perímetro permitem que o CO obtenha oxigênio da água para que possa se tornar CO 2 , e a água (H 2 O) perde oxigênio para se tornar hidrogênio. "
Agora que os cientistas sabem quais átomos de platina desempenham um papel ativo no catalisador, eles podem ser capazes de projetar catalisadores que contenham apenas aqueles átomos de platina ativos.

Autor principal Yuanyuan Li, um cientista pesquisador do Departamento de Ciência de Materiais e Engenharia Química da Stony Brook University, que tem uma nomeação como convidado na Divisão de Química do Laboratório Brookhaven, realiza uma análise em uma amostra usando um espectrômetro infravermelho. Crédito:Laboratório Nacional de Brookhaven
"Podemos supor que todos os átomos de platina da superfície estão funcionando, mas eles não são, "Li disse." Não precisamos de todos eles, apenas os ativos. Isso poderia nos ajudar a tornar o catalisador mais barato, removendo os átomos que não estão envolvidos na reação. Acreditamos que este mecanismo pode ser generalizado para outros sistemas catalíticos e reações, " ela adicionou.
Detalhes experimentais
Os "instantâneos" da microscopia eletrônica no CFN e no Instituto Nacional de Padrões e Tecnologia revelaram a natureza dinâmica dos átomos de platina do perímetro. "Em algumas imagens, o site do perímetro está lá, você pode ver isso, mas em algumas imagens não está lá. Esta é uma evidência de que esses átomos são muito dinâmicos, com alta mobilidade, "Li disse.
Estudos de espectroscopia de infravermelho (IV) na Divisão de Química de Brookhaven revelaram que a aparência dos locais do perímetro coincidia com "lacunas de oxigênio" - um tipo de defeito na superfície do óxido de cério. Esses estudos também mostraram que o CO tendia a migrar através da superfície das nanopartículas de platina em direção aos átomos do perímetro, e que os grupos hidroxi (OH) permaneceram no suporte de céria perto dos átomos de platina do perímetro.
"Então, parece que os átomos de platina do perímetro trazem os dois reagentes, CO e OH (das moléculas de água) juntos, "Li disse.
Estudos de espectroscopia de fotoelétrons de raios-X em Química revelaram que átomos de platina de perímetro também foram ativados - mudaram de um estado não metálico para um estado metálico que poderia capturar átomos de oxigênio dos grupos OH e entregar esse oxigênio ao CO. "Isso realmente mostra que esses átomos de platina de perímetro ativados sites permitem que a reação aconteça, "Li disse.
Um conjunto final de experimentos - estudos de espectroscopia de absorção de raios-X conduzidos na Advanced Photon Source (APS) no Argonne National Laboratory do DOE - mostrou as mudanças estruturais dinâmicas do catalisador.
"Vemos que a estrutura está mudando sob as condições de reação, "Li disse.
Esses estudos também revelaram uma ligação excepcionalmente longa entre os átomos de platina e o oxigênio no suporte de céria, sugerindo que algo invisível aos raios X estava ocupando espaço entre os dois.
"Achamos que há algum hidrogênio atômico entre a nanopartícula e o suporte. Os raios X não podem ver átomos leves como o hidrogênio. Em condições de reação, esses hidrogênios atômicos irão se recombinar para formar H 2 , " ela adicionou.
As características estruturais e os detalhes de como as mudanças dinâmicas estão conectadas à reatividade ajudarão os cientistas a entender o mecanismo de funcionamento desse catalisador em particular e, potencialmente, projetar outros com melhor atividade e menor custo. As mesmas técnicas também podem ser aplicadas a estudos de outros catalisadores.