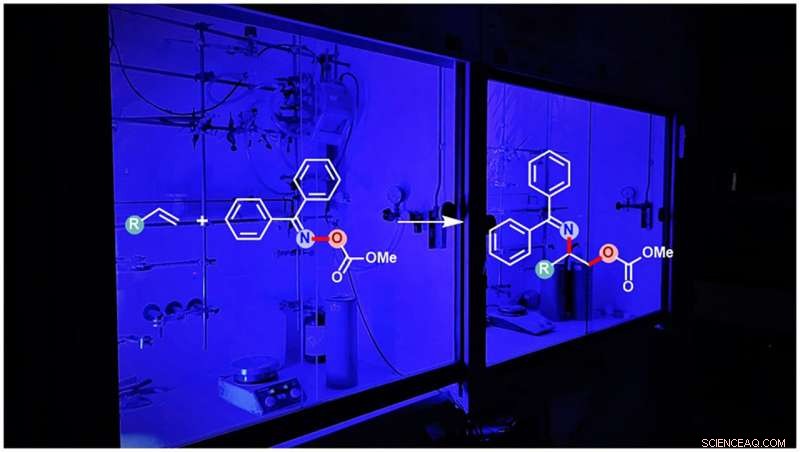
 p Síntese fotossensibilizada de aminoálcoois protegidos. Crédito:WWU - Grupo Glorius
p Síntese fotossensibilizada de aminoálcoois protegidos. Crédito:WWU - Grupo Glorius
p Seja em betabloqueadores para tratar a hipertensão ou em produtos naturais, os chamados aminoálcoois vicinais são compostos orgânicos de alta qualidade encontrados em muitos itens do dia-a-dia. Contudo, sua produção é difícil, e por muito tempo, os químicos têm tentado desenvolver métodos eficientes de sintetizá-los. Em seu estudo recente publicado na revista
Catálise Natural , cientistas liderados pelo Prof. Dr. Frank Glorius, da Universidade de Münster, encontraram uma solução para a produção de uma variante especial de aminoálcoois. “O novo método ajuda a estudar as propriedades da substância e a encontrar aplicações para esses novos compostos no futuro, "enfatiza Glorius do Instituto de Química Orgânica da Universidade de Münster. p Os aminoálcoois vicinais podem ocorrer em duas variantes diferentes - chamadas regioisômeros - nas quais os grupos funcionais amina e álcool trocam de posição. Embora sejam muito semelhantes, eles geralmente têm propriedades bioquímicas diferentes. A instalação de grupos amina e álcool em uma etapa representa um grande desafio. A descoberta da Reação de Amino Hidroxilação Assimétrica, com a qual um dos regioisômeros pode ser produzido, até resultou em um Prêmio Nobel para o químico Barry Sharpless em 2001. No entanto, o outro regioisômero não pode ser sintetizado por um método semelhante e permaneceu um problema de longa data - até agora. Com a ajuda do novo método de reação fotoiniciada dos químicos, a síntese do outro regioisômero agora também se tornou eficientemente possível.
p Alcenos não ativados contendo uma ligação dupla carbono-carbono são conhecidos como produtos químicos de matéria-prima para processos de reação devido à sua boa disponibilidade. Em geral, a instalação de grupos amina e álcool em uma etapa através desta ligação dupla carbono-carbono de alqueno não ativado é sempre iniciada pelo grupo amina, seguido pela adição do grupo álcool. Como resultado, um regioisômero particular do aminoálcool vicinal é sempre formado. Agora os cientistas identificaram uma classe particular de compostos semelhantes a aminas que são reativos, mas estáveis o suficiente para permitir primeiro a adição do grupo álcool à ligação dupla carbono-carbono, seguido pela adição do grupo amina para gerar o regioisômero oposto anteriormente inacessível dos aminoálcoois vicinais.
p "Assim como as plantas usam clorofila para converter luz em energia, usamos o que é chamado de fotocatalisador, "explica o Dr. Tuhin Patra, primeiro autor deste estudo. "Esta espécie pode absorver a luz dos LEDs azuis e transferir sua energia para uma molécula diretamente envolvida na reação. Isso libera simultaneamente os grupos amina e álcool." Este processo, em que as moléculas transferem elétrons umas para as outras, é chamado de transferência de energia, o cientista explica.
p Fascinantemente, o novo método gera o regioisômero menos acessível dos aminoálcoois vicinais de tal maneira que ambos os grupos álcool e amina são protegidos de futuras reações. Dependendo das necessidades do usuário, um dos dois grupos de álcool ou amina agora pode ser reativado sem afetar o outro. Contudo, mesmo ambos os grupos podem ser habilitados para reagir mais ao mesmo tempo, se isso for necessário para a síntese de outros requisitos. "Projetos anteriores geralmente instalam apenas um grupo por vez em um processo geral complexo de várias etapas. Nosso projeto não só permite a instalação de dois grupos diferentes em uma etapa com a proteção desejada, mas também gera de forma confiável o regioisômero menos acessível, oferecendo a chance de investigar futuras aplicações deste composto, "conclui Glorius.
