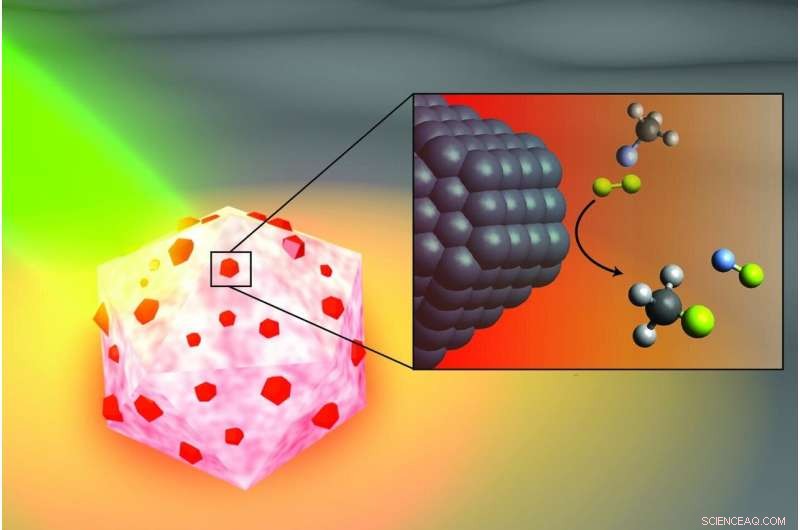
Uma ilustração artística do catalisador reator-antena ativado por luz dos engenheiros da Rice University, projetado para quebrar as ligações carbono-flúor em fluorocarbonos. A porção de alumínio da partícula (branca e rosa) captura a energia da luz (verde), ativando ilhas de catalisadores de paládio (vermelho). Na inserção, moléculas de fluorometano (topo) compostas por um átomo de carbono (preto), três átomos de hidrogênio (cinza) e um átomo de flúor (azul claro) reagem com moléculas de deutério (amarelo) perto da superfície do paládio (preto), clivando a ligação carbono-flúor para produzir fluoreto de deutério (direita) e metano monodeuterado (abaixo). Crédito:H. Robatjazi / Rice University
Os engenheiros da Rice University criaram um catalisador movido a luz que pode quebrar as fortes ligações químicas dos fluorocarbonos, um grupo de materiais sintéticos que inclui poluentes ambientais persistentes.
Em um estudo publicado este mês em Catálise Natural , Naomi Halas, pioneira da nanofotônica de arroz, e colaboradores da Universidade da Califórnia, Santa Bárbara (UCSB) e a Universidade de Princeton mostraram que minúsculas esferas de alumínio pontilhadas com partículas de paládio podem quebrar as ligações carbono-flúor (C-F) por meio de um processo catalítico conhecido como hidrodefluoração, no qual um átomo de flúor é substituído por um átomo de hidrogênio.
A força e a estabilidade das ligações C-F estão por trás de algumas das marcas químicas mais reconhecidas do século 20, incluindo Teflon, Freon e Scotchgard. Mas a força dessas ligações pode ser problemática quando os fluorocarbonos vão para o ar, solo e água. Clorofluorcarbonos, ou CFCs, por exemplo, foram banidos por um tratado internacional na década de 1980, depois que se descobriu que estavam destruindo a camada protetora de ozônio da Terra, e outros fluorcarbonos estavam na lista de "produtos químicos eternos" visados por um tratado de 2001.
"A parte mais difícil de remediar qualquer um dos compostos que contêm flúor é quebrar a ligação C-F; isso requer muita energia, "disse Halas, um engenheiro e químico cujo Laboratório de Nanofotônica (LANP) é especializado na criação e estudo de nanopartículas que interagem com a luz.
Nos últimos cinco anos, Halas e seus colegas foram pioneiros em métodos para fazer catalisadores "antenas-reatores" que estimulam ou aceleram as reações químicas. Embora os catalisadores sejam amplamente usados na indústria, eles são normalmente usados em processos de uso intensivo de energia que requerem alta temperatura, alta pressão ou ambos. Por exemplo, uma malha de material catalítico é inserida em um vaso de alta pressão em uma fábrica de produtos químicos, e gás natural ou outro combustível fóssil é queimado para aquecer o gás ou líquido que flui através da malha. Os reatores de antena do LANP melhoram drasticamente a eficiência energética, capturando a energia da luz e inserindo-a diretamente no ponto da reação catalítica.
No Catálise Natural estude, a antena de captura de energia é uma partícula de alumínio menor do que uma célula viva, e os reatores são ilhas de paládio espalhadas pela superfície do alumínio. O recurso de economia de energia dos catalisadores de antena-reator talvez seja mais bem ilustrado por outro sucesso anterior da Halas:o vapor solar. Em 2012, sua equipe mostrou que suas partículas de captação de energia podem vaporizar instantaneamente moléculas de água perto de sua superfície, significando que Halas e seus colegas poderiam fazer vapor sem ferver água. Para esclarecer o ponto, eles mostraram que podiam fazer vapor com água gelada.
O projeto do catalisador antena-reator permite que a equipe da Halas misture e combine metais que são mais adequados para capturar luz e catalisar reações em um determinado contexto. O trabalho faz parte do movimento da química verde em direção a produtos mais limpos, processos químicos mais eficientes, e a LANP já demonstrou catalisadores para a produção de etileno e gás de síntese e para a divisão de amônia para produzir hidrogênio combustível.
O autor principal do estudo, Hossein Robatjazi, um Beckman Postdoctoral Fellow na UCSB que obteve seu Ph.D. da Rice em 2019, conduziu a maior parte da pesquisa durante seus estudos de graduação no laboratório da Halas. Segundo ele, o projeto também mostra a importância da colaboração interdisciplinar.
"Eu terminei os experimentos no ano passado, mas nossos resultados experimentais tinham algumas características interessantes, mudanças na cinética de reação sob iluminação, isso levantou uma questão importante, mas interessante:que papel a luz desempenha para promover a química de quebra de C-F? ", disse ele.
As respostas vieram depois que Robatjazi chegou para sua experiência de pós-doutorado na UCSB. Ele foi encarregado de desenvolver um modelo de microcinética, e uma combinação de percepções do modelo e de cálculos teóricos realizados por colaboradores em Princeton ajudou a explicar os resultados intrigantes.
"Com este modelo, usamos a perspectiva da ciência da superfície na catálise tradicional para unir os resultados experimentais às mudanças na via de reação e reatividade sob a luz, " ele disse.
Os experimentos de demonstração com fluorometano podem ser apenas o começo para o catalisador de quebra de C-F.
"Esta reação geral pode ser útil para remediar muitos outros tipos de moléculas fluoradas, "Halas disse.