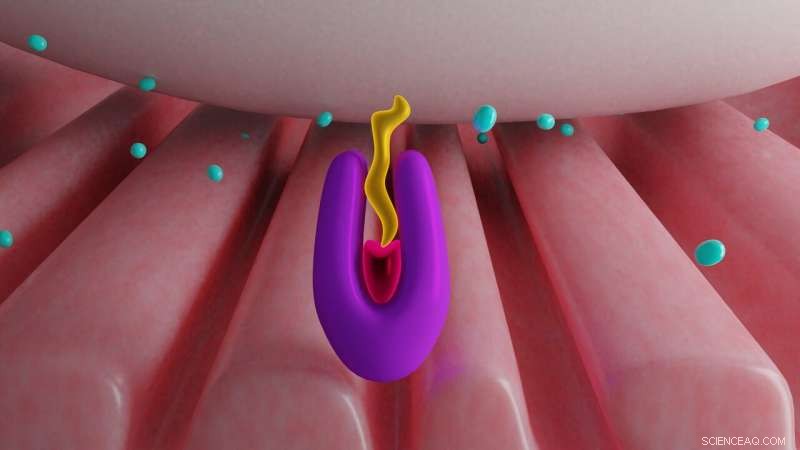
Um antídoto de ação rápida para mitigar os efeitos do envenenamento por organofosforados requer um reativador que possa cruzar a barreira hematoencefálica de forma eficaz e eficiente, ligam-se frouxamente à enzima, pegue quimicamente o veneno e saia rapidamente. O Oak Ridge National Laboratory está usando dados de difração de nêutrons para melhorar um novo projeto de reativador. Crédito:Michelle Lehman e Jill Hemman / ORNL, Departamento de Energia dos EUA
Escolha o seu veneno. Pode ser mortal por bons motivos, como proteger as plantações de insetos prejudiciais ou combater a infecção do parasita como remédio - ou pelo mal como arma para o bioterrorismo. Ou, em quantidades extremamente diluídas, pode ser usado para realçar a beleza.
Embora ataques químicos direcionados a civis tendam a ser manchetes, os relatos de envenenamento mais comuns nos Estados Unidos são de exposição acidental a produtos químicos domésticos, como sprays de insetos, soluções de limpeza ou frutas ou vegetais mal lavados. Em todo o caso, o remédio é uma ação rápida, composto de drogas perseguidoras de veneno, e o Oak Ridge National Laboratory está na vanguarda, desenvolvendo uma nova geração de antídotos que salvam vidas.
Simplificando, "um veneno é algo que degrada gravemente a sua saúde, ou seu estado de saúde, "disse Andrey Kovalevsky, cristalógrafo e bioquímico do ORNL. Ele é um especialista em compreensão da função enzimática em nível atômico, ligação e resistência aos medicamentos. Usando nêutrons e raios-X, ele estuda como as enzimas funcionam no corpo e, dependendo das especificidades, como inibi-los ou reativá-los usando pequenas moléculas orgânicas.
"Dependendo do veneno e da quantidade, o efeito pode ser muito rápido - em segundos - ou pode ser lento, ", acrescentou. O corpo aciona suas próprias defesas para neutralizar uma substância venenosa; no entanto, geralmente não é suficiente. Qualquer nível de exposição pode ser mortal, especialmente se o tipo de veneno não for conhecido imediatamente pelo primeiro socorrista ou pela equipe médica que atende o paciente afetado.
Um antídoto deve agir rápido - antes que o veneno cause danos irreversíveis - para ser eficaz e salvar vidas.
Espelhe o veneno
Kovalevsky faz parte de uma equipe liderada por Zoran Radić, da Universidade da Califórnia, San Diego, desenvolver uma nova família de antídotos para venenos chamados organofosforados, que incluem agentes nervosos. A pesquisa de Radić visa exclusivamente a causa raiz do envenenamento por organofosforados, indo além de apenas tratar os sintomas como os remédios existentes.
Seu foco está nos complexos mecanismos bioquímicos que controlam e mantêm o sistema nervoso do corpo. Eles começam com acetilcolina, ou ACh, que é um composto encontrado na junção de músculos e nervos e também no cérebro. A ACh funciona como um neurotransmissor que mantém a comunicação normal entre os nervos e os músculos. Mas ACh não age sozinho.
A enzima chamada acetilcolinesterase, ou AChE, é também onde os músculos e os nervos se encontram. Seu trabalho é fornecer controle específico dos níveis do composto ACh, degradando-o, o que garante que os nervos estão funcionando corretamente.
Quando uma pessoa é exposta a um agente nervoso, ou a grandes quantidades de um spray de inseto, por exemplo, o veneno passa rapidamente dos pulmões ou da pele para a corrente sanguínea e corre para o sistema nervoso. À medida que atinge as junções músculo-nervo, o veneno domina e inibe o trabalho da enzima AChE.
Como a enzima AChE está sob ataque e é incapaz de degradar a ACh, os níveis do composto ACh aumentam, perturbando o equilíbrio entre músculos e nervos. Isso causa estragos no corpo.
"Em vez de ser muito pouco, há muito deste neurotransmissor. Então, os receptores dos nervos estão superexcitados, e as pessoas podem entrar em choque, têm tremores e convulsões e começam a suar porque suas glândulas estão trabalhando demais, "Kovalevsky explicou. No final, a pessoa afetada provavelmente morrerá porque parou de respirar.
Radić disse que o antídoto deve refletir a atividade do veneno sem atuar como um inibidor, também.
"Esses venenos, normalmente composto de moléculas sem carga ou neutras, atravessam as membranas biológicas muito rapidamente para o sangue e são então distribuídas do sangue para o tecido, incluindo o sistema nervoso central. E tudo isso acontece em minutos após a exposição, " ele disse.
"O veneno chega ao seu alvo rapidamente, então, para tratar esse alvo e recuperar a atividade da enzima, temos que ter um antídoto que faça o mesmo. "
Se bem feito, o antídoto vai aliviar a enzima AChE do ataque do veneno, essencialmente extirpando a molécula do veneno ligada à enzima, e permitindo que ele comece a nivelar os neurotransmissores ACh e, finalmente, acalmar todo o sistema nervoso. O truque é garantir que o antídoto seja projetado para não durar muito tempo ou se apegar demais à enzima - e se tornar parte do problema.
Para o resgate
Em um estudo financiado pelo Programa CounterACT, National Institutes of Health Office of the Director e do National Institute of Neurological Disorders and Stroke e publicado no Journal of Biological Chemistry , A equipe de Radić projetou e testou medicamentos de ação rápida chamados reativadores em três agentes nervosos diferentes e um pesticida com resultados iniciais positivos.
A equipe começou com um composto de medicamento existente (nome de código RS194B), que foi desenvolvido por Radić e o professor Palmer Taylor da UC San Diego cerca de 15 anos antes, porque já havia se mostrado promissor ao atravessar a barreira hematoencefálica quando testado em primatas expostos ao envenenamento por organofosforados.
Contudo, os reativadores recém-projetados tiveram melhor desempenho in vitro, ou fora de um organismo vivo, do que RS194B, e a equipe de pesquisa descobriu o porquê.
No nível atômico, O RS194B não conseguiu atingir o local da atividade do veneno dentro da molécula de AChE com a mesma eficiência dos novos reativadores.
Para este estudo, a equipe usou análise cristalográfica de raios-X para observar o complexo RS194B com a enzima AChE sozinha e, em seguida, introduziu um análogo de um agente químico nervoso chamado VX - um dos produtos químicos mais mortíferos já produzidos. Enquanto RS194B não ligou como esperado, o experimento promoveu ideias sobre como redesenhar "uma espécie de composto de elite, "Kovalevsky disse.
"Precisamos melhorar a capacidade do reativador de cruzar a barreira hematoencefálica, ligam-se frouxamente à enzima, pegue quimicamente o veneno e saia rapidamente, "Kovalevsky disse." Não queremos que permaneça após a reativação, como fazemos com muitos medicamentos padrão que normalmente inibem a função de uma enzima. "
"Esse é o nosso objetivo. É por isso que projetar reativadores é um esforço completamente diferente e muitas regras do projeto de medicamentos convencionais não se aplicam, " ele adicionou.
Depois de alguns ajustes no design do medicamento, a equipe surgiu com um novo paradigma que pode mudar completamente a forma como os pesquisadores pensam sobre o projeto de um reativador. Eles executaram simulações de computador e mais tarde sintetizaram vários compostos mais promissores das opções de design alteradas, que forneceu detalhes sobre suas propriedades e dicas sobre como cada composto pode funcionar.
Eles analisaram o impacto de cada variação de design de medicamento, mais o RS194B original, com agentes nervosos Sarin, Ciclosarina, VX e um pesticida Paraoxon. Também, a equipe incluiu 2PAM (também chamado de pralidoxima) - o único antídoto para envenenamento por organofosforado que é aprovado pela U.S. Federal Drug Administration para uso em adultos e crianças - que serviu como um controle para os experimentos.
"Queríamos que nossos projetos de reativadores fossem tão bons quanto, ou melhor do que, 2PAM nestes estudos, "disse Kovalevsky. No entanto, 2PAM não é capaz de cruzar a barreira hematoencefálica. Ele pode viajar para outras áreas do corpo afetadas pelo veneno para atuar no sistema nervoso periférico, mas não é reativado no sistema nervoso central.
Com base nos resultados iniciais do estudo, várias variações de design de drogas da equipe funcionaram melhor do que RS194B e 2PAM, que Kovalevsky disse ser um resultado muito encorajador para suas novas idéias de design de reativador.
"Uma das distinções do nosso antídoto é que eles podem envolver diferentes venenos organofosforados de forma mais eficaz, porque suas estruturas de reativação podem mudar com sua protonação, "Radić disse." Ao contrário dos raios X, difração de nêutrons é uma técnica experimental que pode nos dizer sobre a posição dos prótons no antídoto e na enzima envenenada. "
Grande, cristais minúsculos
Para obter uma imagem melhor do novo design do reativador, a equipe usou cristalografia de nêutrons no High Flux Isotope Reactor de ORNL, uma instalação de usuário do Departamento de Energia do Escritório de Ciências. Kovalevsky opera o instrumento chamado IMAGINE, que usa técnicas de difração de nêutrons para observar a estrutura de um único cristal em escala atômica.
A estrutura molecular da proteína é complexa, que requer o crescimento de grandes cristais únicos - uma força dos ORNLs - para difração de nêutrons. Os nêutrons são altamente sensíveis aos elementos leves, como o hidrogênio, e eles são particularmente adequados para encontrar átomos de hidrogênio individuais em cristais de proteína que os raios X não podem detectar. Os dados coletados do IMAGINE, junto com informações de um experimento de nêutrons realizado no Institut Laue-Langevin na França, confirmou que é possível identificar a localização e distribuição de cada átomo de hidrogênio na proteína.
A equipe continuará crescendo cristais maiores para análise, que deve produzir conjuntos de dados de maior resolução e informar os ajustes para o prometido, novos designs de drogas. Sua pesquisa contínua poderia, em última análise, confirmar uma nova classe de ação rápida, antídotos que salvam vidas para envenenamento por organofosforados.