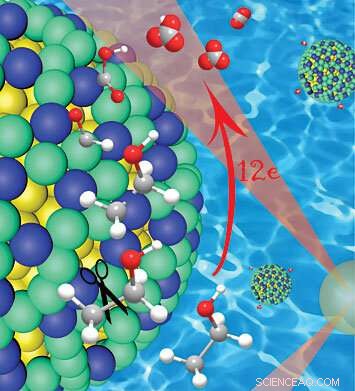
Um close-up da casca de platina / irídio (verde / azul) sobre um núcleo de nanopartícula de ouro (amarelo), mostrando como este catalisador cliva as ligações carbono-carbono (cinza) em etanol, deixando inicialmente átomos de hidrogênio ligados. O hidrogênio protege o carbono nos estágios iniciais da reação, prevenir a formação de monóxido de carbono envenenado por catalisador, que permite a oxidação completa e a liberação de 12 elétrons. Crédito:Laboratório Nacional de Brookhaven
Cientistas do Laboratório Nacional de Brookhaven e da Universidade de Arkansas desenvolveram um catalisador altamente eficiente para extrair energia elétrica do etanol, um combustível líquido fácil de armazenar que pode ser gerado a partir de recursos renováveis. O catalisador, descrito no Jornal da American Chemical Society , direciona a eletro-oxidação do etanol por um caminho químico ideal que libera todo o potencial de energia armazenada do combustível líquido.
"Este catalisador é uma virada de jogo que permitirá o uso de células a combustível de etanol como uma fonte promissora de alta densidade de energia de energia elétrica 'fora da rede', "disse Jia Wang, o químico do Laboratório Brookhaven que liderou o trabalho. Uma aplicação particularmente promissora:drones movidos a células de combustível líquido.
"As células de combustível de etanol são leves em comparação com as baterias. Elas forneceriam energia suficiente para operar drones usando um combustível líquido fácil de reabastecer entre os voos, mesmo em locais remotos, "Wang observou.
Muito do poder potencial do etanol está preso nas ligações carbono-carbono que formam a espinha dorsal da molécula. O catalisador desenvolvido pelo grupo de Wang revela que quebrar esses laços no momento certo é a chave para desbloquear essa energia armazenada.
"A eletro-oxidação do etanol pode produzir 12 elétrons por molécula, "Disse Wang." Mas a reação pode progredir seguindo muitos caminhos diferentes. "
A maioria dessas vias resulta em oxidação incompleta:os catalisadores deixam as ligações carbono-carbono intactas, liberando menos elétrons. Eles também retiram os átomos de hidrogênio no início do processo, expor átomos de carbono à formação de monóxido de carbono, que "envenena" a capacidade dos catalisadores de funcionar ao longo do tempo.

Membros do Brookhaven Lab da equipe de pesquisa que desenvolveu e caracterizou um novo catalisador core-shell para eletro-oxidação completa de etanol (l a r):Radoslav Adzic, Zhixiu Liang, Jia Wang, Eli Stavitski, e Liang Song. Crédito:Laboratório Nacional de Brookhaven
"A oxidação completa de 12 elétrons do etanol requer a quebra da ligação carbono-carbono no início do processo, enquanto os átomos de hidrogênio ainda estão ligados, porque o hidrogênio protege o carbono e evita a formação de monóxido de carbono, "Disse Wang. Então, várias etapas de desidrogenação e oxidação são necessárias para concluir o processo.
O novo catalisador - que combina elementos reativos em uma estrutura única de núcleo-concha que os cientistas de Brookhaven vêm explorando para uma série de reações catalíticas - acelera todas essas etapas.
Para fazer o catalisador, Jingyi Chen, da Universidade de Arkansas, que foi um cientista visitante em Brookhaven durante parte deste projeto, desenvolveu um método de síntese para co-depositar platina e irídio em nanopartículas de ouro. A platina e o irídio formam "ilhas monoatômicas" na superfície das nanopartículas de ouro. Esse arranjo, Chen observou, é a chave que explica o excelente desempenho do catalisador.
"Os núcleos de nanopartículas de ouro induzem tensão de tração nas ilhas monoatômicas de platina-irídio, o que aumenta a capacidade desses elementos de clivar as ligações carbono-carbono, e, em seguida, remover seus átomos de hidrogênio, " ela disse.
Zhixiu Liang, um estudante de pós-graduação da Stony Brook University e o primeiro autor do artigo, realizou estudos no laboratório de Wang para entender como o catalisador atinge sua eficiência recorde de conversão de energia. Ele usou "espectroscopia de absorção de reflexão infravermelha in situ" para identificar os produtos e produtos intermediários da reação, comparar aqueles produzidos pelo novo catalisador com reações usando um catalisador de núcleo de ouro / casca de platina e também um catalisador de liga de platina-irídio.

Um esquema que mostra como as "ilhas monoatômicas" de platina (verde) e irídio (azul) na superfície das nanopartículas de ouro (amarelo) permitem uma oxidação completa de 12 elétrons do etanol sem envenenamento por monóxido de carbono. O gráfico ilustra a corrente de pico dramaticamente mais alta produzida pelo novo catalisador (Au @ PtIr) em comparação com três outros catalisadores:núcleo de ouro / camada de irídio (Au @ Ir); liga de irídio / platina (IrPt); e núcleo de ouro / casca de platina (Au @ Pt). Crédito:Laboratório Nacional de Brookhaven
"Medindo os espectros produzidos quando a luz infravermelha é absorvida em diferentes etapas da reação, este método nos permite rastrear, em cada etapa, quais espécies foram formadas e quanto de cada produto, "Disse Liang." O espectro revelou que o novo catalisador conduz o etanol em direção à via de oxidação completa de 12 elétrons, liberando todo o potencial de energia armazenada do combustível. "
O próximo passo, Wang observou, é projetar dispositivos que incorporem o novo catalisador.
Os detalhes mecanísticos revelados por este estudo também podem ajudar a orientar o projeto racional de futuros catalisadores multicomponentes para outras aplicações.