
Sooyeon Hwang (sentado), Dong Su (à esquerda, de pé, e Shuang Li no Brookhaven Lab's Center for Functional Nanomaterials, onde eles usaram microscópios eletrônicos para ver como a estrutura cristalina e a natureza química de um eletrodo de bateria feito de um material de óxido de ferro chamado magnetita evoluiu quando o lítio foi inserido e extraído em 100 ciclos de carga e descarga. Crédito:Laboratório Nacional de Brookhaven
Por causa de sua alta densidade de armazenamento de energia, materiais como óxidos de metal, sulfetos, e os fluoretos são materiais promissores para eletrodos para baterias de íon-lítio em veículos elétricos e outras tecnologias. Contudo, sua capacidade diminui muito rapidamente. Agora, cientistas que estudam um eletrodo feito de um material barato e não tóxico de óxido de ferro chamado magnetita propuseram um cenário - descrito na edição online de 20 de maio da Nature Communications —Isso explica o porquê.
"Magnetita, entre outros materiais de eletrodo de tipo de conversão (isto é, materiais que são convertidos em produtos totalmente novos quando reagem com o lítio), podem armazenar mais energia do que os materiais de eletrodo de hoje porque podem acomodar mais íons de lítio, "disse o líder do estudo Dong Su, líder do Grupo de Microscopia Eletrônica no Center for Functional Nanomaterials (CFN) - um Office of Science User Facility do Departamento de Energia dos EUA (DOE) no Brookhaven National Laboratory. "Contudo, a capacidade desses materiais se degrada muito rapidamente e depende da densidade da corrente. Por exemplo, nosso teste eletroquímico de magnetita revelou que sua capacidade cai muito rapidamente dentro dos primeiros 10 ciclos de alta taxa de carga e descarga. "
Para descobrir o que está por trás dessa baixa estabilidade do ciclismo, os cientistas caracterizaram como a estrutura cristalina e a natureza química da magnetita evoluíram à medida que a bateria completava 100 ciclos. Para esses estudos de caracterização, eles combinaram microscopia eletrônica de transmissão (TEM) no CFN e espectroscopia de absorção de raios-X síncrotron (XAS) na Advanced Photon Source (APS) - um DOE Office of Science User Facility no Argonne National Lab. Em TEM, um feixe de elétrons é transmitido através de uma amostra para produzir uma imagem ou um padrão de difração característico da estrutura do material; O XAS usa um feixe de raios-X em vez de sondar a química do material.
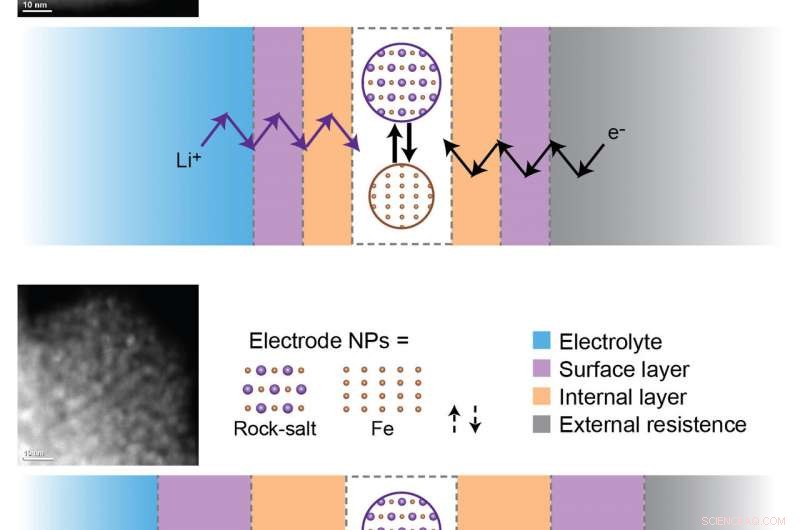
O enfraquecimento da capacidade da bateria é devido à formação e espessamento das camadas de passivação interna e superficial durante os ciclos de carga e descarga. Para que as reações eletroquímicas ocorram, íons de lítio (Li +) e elétrons (e-) devem viajar por todas essas camadas para alcançar nanopartículas ativas (NPs) no eletrodo. Acima:amostra de Fe3O4 (óxido de ferro) após três ciclos. Parte inferior:amostra de Fe3O4 após 100 ciclos. O desenvolvimento de barreiras cinéticas durante os ciclos de longo prazo limita as reações eletroquímicas a tal ponto que nenhuma reação de redução-oxidação ocorre nos materiais do eletrodo após 100 ciclos. Crédito:Laboratório Nacional de Brookhaven
Usando essas técnicas, os cientistas descobriram que a magnetita se decompõe completamente em nanopartículas de ferro metálico e óxido de lítio durante a primeira descarga. Na cobrança a seguir, esta reação de conversão não é completamente reversível - resíduos de ferro metálico e óxido de lítio permanecem. Além disso, a estrutura "espinélio" original da magnetita evolui para uma estrutura "sal-gema" (a localização dos átomos de ferro não é inteiramente idêntica nas duas estruturas) no estado carregado. Com os ciclos subsequentes de carga e descarga, O óxido de ferro sal-gema interage com o lítio para formar um composto de óxido de lítio e nanopartículas de ferro metálico. Como a reação de conversão não é totalmente reversível, esses produtos residuais se acumulam. Os cientistas também descobriram que o eletrólito (o meio químico que permite que os íons de lítio fluam entre os dois eletrodos) se decompõe em ciclos posteriores.
"Nossos estudos TEM em tempo real em vácuo ultra-alto nos permitiram ver como a estrutura do óxido de ferro sal-gema muda conforme o lítio é introduzido após os ciclos iniciais, "disse Su." Este estudo representa exclusivamente a litiação in situ de uma amostra pré-reciclada. Estudos anteriores in situ analisaram apenas os ciclos iniciais de carga e descarga. Contudo, precisamos saber o que acontece ao longo de muitos ciclos para projetar baterias de maior duração, porque a estrutura no eletrodo carregado é diferente daquela do estado original. "
Com base em seus resultados, os cientistas propuseram uma explicação para o enfraquecimento da capacidade.
"Como o óxido de lítio tem baixa condutividade eletrônica, seu acúmulo cria uma barreira para os elétrons que estão indo e voltando entre os eletrodos positivo e negativo da bateria, "explicou a co-autora Sooyeon Hwang, um cientista da equipe do Grupo de Microscopia Eletrônica CFN. "Chamamos essa barreira de camada de passivação interna. Da mesma forma, a decomposição eletrolítica impede a condução iônica, formando uma camada superficial de passivação. Este acúmulo de obstáculos bloqueia os elétrons e íons de lítio de atingir os materiais do eletrodo ativo, onde ocorrem as reações eletroquímicas. "
Os cientistas notaram que operar a bateria em uma corrente baixa pode recuperar parte dessa capacidade diminuindo a taxa de carga para fornecer tempo suficiente para o transporte de elétrons; Contudo, outras soluções são necessárias para resolver o problema. Eles acreditam que adicionar outros elementos ao material do eletrodo e alterar o eletrólito pode melhorar a capacidade de desvanecimento.
"O conhecimento que adquirimos pode geralmente ser aplicado a outros compostos de conversão, que também enfrentam o mesmo problema com as camadas de passivação interna e externa, "disse o co-autor Zhongwei Chen, um professor da Universidade de Waterloo, Canadá. "Esperamos que este estudo possa ajudar a orientar futuras pesquisas fundamentais sobre esses materiais de eletrodo do tipo de conversão promissores."