Uma representação artística de um biofilme abrigando bactérias resistentes a antibióticos em forma de bastonete e esféricas. Crédito:Kateryna Kon / Shutterstock.com
As superfícies com as quais as pessoas interagem todos os dias podem parecer bastante mundanas, mas na escala molecular, há mais atividade do que aparenta.
Cada superfície que tocamos tem suas próprias propriedades químicas exclusivas. É por causa dessas propriedades que alguns materiais aderem às superfícies, enquanto outros deslizam. Para uma pessoa, uma superfície pegajosa pode ser um pequeno incômodo, mas para uma célula bacteriana, o apego superficial pode ser uma questão de vida ou morte. As bactérias desenvolveram suas próprias superfícies para serem pegajosas, como velcro.
Quando as bactérias colonizam uma superfície, eles criam uma comunidade chamada biofilme, que pode ser uma fonte de infecção em dispositivos médicos ou implantes. As crescentes preocupações com essas infecções levaram vários pesquisadores a desenvolver materiais para bloquear esses filmes, às vezes perigosos.
Como químicos biofísicos, meu grupo de pesquisa e eu estamos tentando entender as forças moleculares que permitem que as moléculas biológicas - como as das bactérias - se fixem nas superfícies durante as primeiras fases da formação do biofilme. Ao compreender este estágio inicial de apego, podemos reduzir os riscos de formação de biofilme em dispositivos médicos implantados e representar uma ameaça para os seres humanos.
Colônias bacterianas
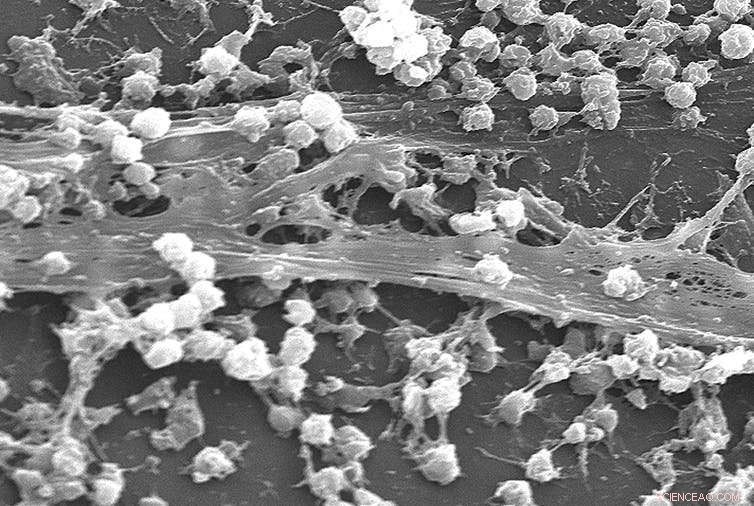
Biofilme de Staphylococcus aureus na superfície de um cateter. Crédito:Rodney M. Donlan, Janice Carr / CDC
Biofilmes são comunidades densamente compactadas de bactérias ou outros microorganismos que vivem em uma superfície. Como uma cidade, crescer dentro de um biofilme tem certas vantagens. Por exemplo, fornece suporte estrutural, como o chão de um prédio alto, e os micróbios podem compartilhar nutrientes. Em comparação com bactérias flutuantes, bactérias em um biofilme são protegidas, permitindo-lhes escapar do nosso sistema imunológico e resistir aos antibióticos.
Quando os biofilmes se formam em dispositivos médicos ou implantes, eles podem servir como uma fonte persistente de infecções difíceis de tratar. Isso custa não apenas bilhões de dólares para tratar, mas reivindicam milhares de vidas todos os anos apenas nos EUA.
Os cientistas estão tentando entender como os biofilmes se formam e como evitá-los. Os biólogos moleculares estão descobrindo como o DNA bacteriano codifica a maquinaria que permite que as células se fixem em superfícies e umas às outras. Microbiologistas e químicos medicinais estão procurando drogas que possam penetrar e romper biofilmes. E químicos biofísicos como eu estão tentando descobrir as interações moleculares que tornam esses biofilmes difíceis de prevenir.
Complexidade da superfície
Staphylococcus aureus e S. epidermidis são duas espécies bacterianas que normalmente representam poucos problemas para o nosso corpo. Contudo, quando um biofilme estafilocócico se forma na superfície de um implante médico, como um quadril artificial, essas células podem causar doenças. Biofilmes estafilocócicos são mantidos juntos por açúcares ou polissacarídeos, proteínas e ácidos nucléicos, os blocos de construção moleculares de todos os organismos vivos. Esses componentes permitem que as células bacterianas se colem não apenas umas às outras, mas também em superfícies naturais e implantadas no corpo - como uma válvula cardíaca.
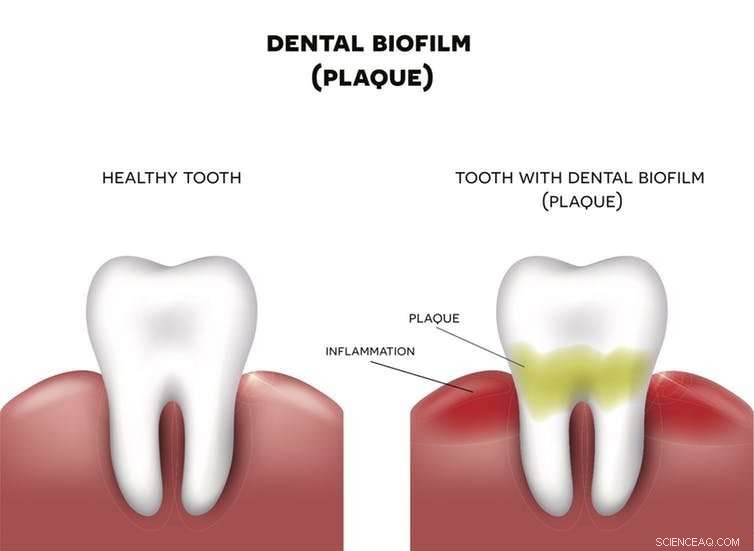
Biofilmes permeiam todos os elementos de nossas vidas. Por exemplo, a placa que se forma nos dentes é um biofilme que protege as bactérias. Se a placa não for removida, o tecido ao redor do dente ficará inflamado. Crédito:Nita_Nita / Shutterstock.com
As superfícies dos dispositivos médicos são complexas, especialmente depois de expostos ao corpo. As proteínas do sangue humano revestem rapidamente a superfície dos implantes médicos, alterando o caráter à medida que o paciente e o dispositivo envelhecem. Quando uma célula bacteriana se liga a uma dessas superfícies, os componentes da célula interagem com a superfície do implante médico, formando uma rede complexa de interações. Em nossa pesquisa, estamos investigando as proteínas da superfície bacteriana que estão envolvidas na fixação da superfície.
Estudar essas interações é desafiador. Tipicamente, experimentos químicos são realizados em solução, mas os experimentos de biofilme devem ser feitos em uma superfície. Detectar as moléculas na superfície é um desafio. Isso porque há menos dessas moléculas em comparação com o volume geral do material, assim como a casca do tomate é uma fração minúscula da massa do tomate inteiro.
Apresentando a nanoescala
Para superar essa limitação, estamos investigando como as proteínas presentes na superfície bacteriana interagem com as superfícies das nanopartículas. Especificamente, estamos usando nanopartículas projetadas para imitar a superfície de dispositivos médicos, e estamos visando proteínas envolvidas em infecções estafilocócicas, uma das principais fontes de doenças hospitalares.
As nanopartículas têm um diâmetro muito menor do que uma célula bacteriana. Mas enquanto uma célula típica tornaria uma nanopartícula anã, a nanopartícula ainda é muito maior do que as moléculas na superfície de uma célula. Ao usar muitas nanopartículas, é mais fácil observar como a bactéria e a partícula interagem e observar as moléculas bacterianas envolvidas na formação do biofilme.

Randika Perera coloca uma amostra de nanopartículas em um espectrômetro de NMR, um dos instrumentos usados para estudar as interações proteína-superfície. Crédito:Sarah Tewolde, MSU Office of Public Affairs, CC BY-SA
Especificamente, estamos tentando entender a estrutura e orientação das proteínas em diferentes tipos de superfícies. Embora não sejamos o primeiro ou o único grupo interessado neste tópico, nosso trabalho começou a revelar os detalhes moleculares de como as proteínas interagem com as superfícies das nanopartículas.
Podemos sondar o quão firmemente as bactérias estão aderindo a uma superfície - e podemos examinar como as moléculas de proteína competem pela mesma superfície. Por exemplo, dada uma coleção de proteínas bacterianas, qual deles acabará por se fixar na superfície de um implante médico?
À medida que descobrimos as respostas a essas perguntas, seremos capazes de identificar os elementos importantes envolvidos na formação inicial do biofilme. Isso será útil para os cientistas que tentam inibir essas interações terapeuticamente, ou aqueles que procuram projetar novas superfícies resistentes ao biofilme.
Este artigo foi republicado de The Conversation sob uma licença Creative Commons. Leia o artigo original. 