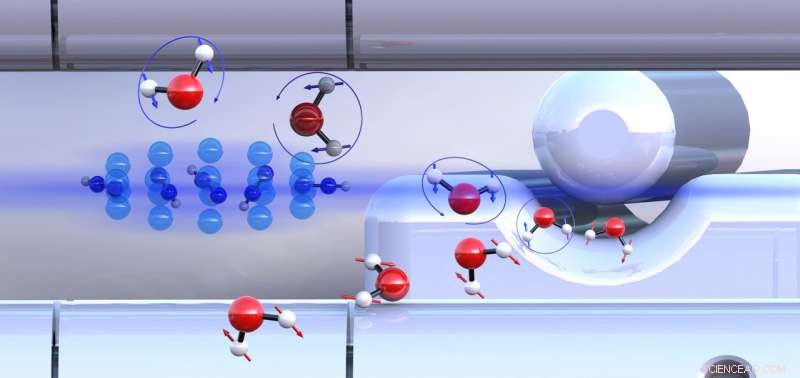
Moléculas pré-classificadas de orto-água e para-água com spins nucleares orientados de forma diferente (setas azuis ou vermelhas) reagem com íons diazenílio (centro esquerdo) em velocidades diferentes. Crédito:Universidade de Basel
As moléculas de água existem em duas formas diferentes com propriedades físicas quase idênticas. Pela primeira vez, os pesquisadores conseguiram separar as duas formas para mostrar que elas podem exibir reatividades químicas diferentes. Esses resultados foram relatados por pesquisadores da Universidade de Basel e seus colegas em Hamburgo na revista científica Nature Communications .
De uma perspectiva química, a água é uma molécula na qual um único átomo de oxigênio está ligado a dois átomos de hidrogênio. É menos conhecido que a água existe em duas formas diferentes (isômeros) no nível molecular. A diferença está na orientação relativa dos spins nucleares dos dois átomos de hidrogênio. Dependendo se os giros estão alinhados na mesma direção ou na direção oposta, um se refere a orto- ou para-água.
Experimentos com moléculas de água classificadas
O grupo de pesquisa liderado pelo professor Stefan Willitsch, do Departamento de Química da Universidade de Basel, investigou como as duas formas de água diferem em termos de sua reatividade química - sua capacidade de sofrer uma reação química. Ambos os isômeros têm propriedades físicas quase idênticas, o que torna sua separação particularmente desafiadora.
Essa separação foi possível por um método baseado em campos elétricos desenvolvido pelo Professor Jochen Küpper do Centro de Ciência de Laser de Eletrons Livres de Hamburgo. Usando essa abordagem, os pesquisadores foram capazes de iniciar reações controladas entre os isômeros de água "pré-classificados" e os íons diazenilium ultracold ("nitrogênio protonado") mantidos em uma armadilha. Durante este processo, um íon diazenílio transfere seu próton para uma molécula de água. Essa reação também é observada na química do espaço interestelar.
Aumento da reatividade
Foi demonstrado que a para-água reage cerca de 25 por cento mais rápido do que a orto-água. Esse efeito pode ser explicado em termos do spin nuclear também influenciando a rotação das moléculas de água. Como resultado, diferentes forças de atração atuam entre os parceiros de reação. Para-água é capaz de atrair seu parceiro de reação mais fortemente do que a forma orto, o que leva a um aumento da reatividade química. Simulações de computador confirmaram essas descobertas experimentais.
Em seus experimentos, os pesquisadores trabalharam com moléculas em temperaturas muito baixas perto do ponto zero absoluto (cerca de -273 ° C). Estas são as condições ideais para preparar com precisão estados quânticos individuais e definir o conteúdo de energia das moléculas, e causar uma reação controlada entre eles. Willitsch explica a abordagem experimental:"Quanto melhor se pode controlar os estados das moléculas envolvidas em uma reação química, melhor os mecanismos subjacentes e a dinâmica de uma reação podem ser investigados e compreendidos. "