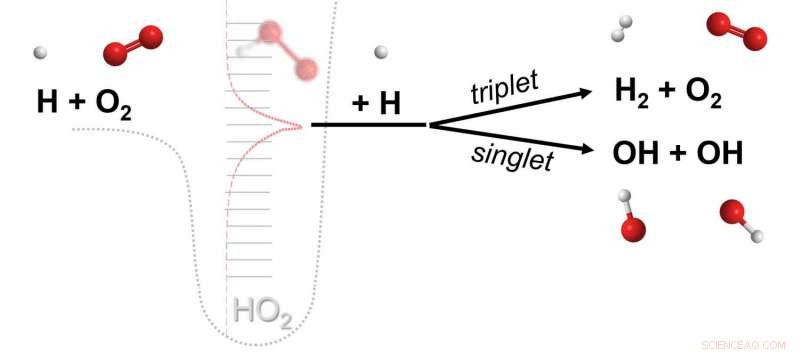
Uma reação química em que três moléculas diferentes (por exemplo, H, O2, H) cada um participa da quebra e formação de ligações químicas. A reação é mediada por um complexo de colisão efêmero (HO2 **) formado a partir da colisão de duas moléculas (H, O2) que então reage ao colidir com uma terceira molécula (H). Os dados de cálculos avançados revelam que as reações desta classe, hipotetizado há quase um século e, posteriormente, considerado sem importância, são as principais vias químicas. Crédito:Michael P. Burke / Columbia Engineering
Um novo estudo liderado por Michael P. Burke, professor assistente de engenharia mecânica na Columbia Engineering, identificou o significado de uma nova classe de reações químicas envolvendo três moléculas, cada uma participando da quebra e formação de ligações químicas. A reação de três moléculas diferentes é possibilitada por um "complexo de colisão efêmero, "formado a partir da colisão de duas moléculas, que vive o suficiente para colidir com uma terceira molécula.
Esta quarta aula, que os pesquisadores chamaram de "reações termoleculares quimicamente, "foi levantada pela primeira vez por Cyril Hinshelwood e Nikolay Semenov em seus estudos de reações em cadeia nas décadas de 1920 e 30 (eles ganharam o Prêmio Nobel de Química em 1956 por este trabalho). Por décadas, pesquisadores consideraram essas reações sem importância - se é que ocorreram - e até agora, ninguém os estudou. Burke, que explora uma variedade de problemas na interface entre físico-química fundamental e dispositivos práticos de engenharia, decidiu investigar essas reações depois de perceber que as situações comuns de combustão, como aqueles encontrados em muitos motores, têm frações suficientemente altas de moléculas altamente reativas conhecidas como radicais livres para tornar essas reações possíveis. O novo estudo é publicado hoje em Química da Natureza .
"A combustão sempre foi um ponto de partida para a compreensão de todos os tipos de outros mecanismos químicos, "diz Burke, que também é membro do Data Science Institute. "Potencialmente, pode haver inúmeras reações desta nova classe que afetam a forma como modelamos a química da fase gasosa, desde o projeto de novos tipos de motores até a compreensão da química planetária responsável pelas formações de nuvens, das Alterações Climáticas, evolução de poluentes, até mesmo talvez a sequência de reações que poderiam impactar as condições de vida extraterrestre. Nossa descoberta abre um novo mundo de possibilidades. "
Por exemplo, veículos espaciais experimentam temperaturas muito altas e frações radicais em sua descida de volta à Terra. Burke especula que esta quarta classe de reações poderia impactar o fluxo de calor para o veículo, com implicações significativas para o projeto de sistemas de proteção térmica para manter os astronautas e / ou cargas úteis em segurança ao descer para a Terra.
Trabalhando com Stephen J. Klippenstein, (Divisão de Ciências Químicas e Engenharia, Laboratório Nacional de Argonne), Burke usou métodos computacionais de última geração, combinar cálculos de química quântica que simulam a quebra e formação de ligações químicas entre moléculas reagentes com cálculos de transporte cinético que simulam as reações e movimentos de gases em massa que governam o desempenho de dispositivos de engenharia.
"O poder desses métodos computacionais de última geração, "diz Burke, "é que eles podem fornecer uma lente única em ambientes químicos agressivos inadequados para técnicas experimentais para estudar a dinâmica de reação individual. Nossos cálculos são baseados em dados computacionais produzidos a partir dos primeiros princípios:a equação de Schrödinger, a equação fundamental da mecânica quântica. Combinar esses dados com outros modelos baseados na física nos permite apontar diretamente o impacto de apenas uma única reação entre muitas, de uma forma que é muito difícil de fazer no laboratório. "
Usando métodos teóricos, incluindo aqueles que desenvolveram para este estudo, os pesquisadores mostraram que essas reações quimicamente termoleculares (ou seja, três moléculas) não são apenas vias químicas importantes, mas também afetam as velocidades de propagação da chama, uma medida da reatividade geral do combustível que governa o desempenho, estabilidade, e eficiência de muitos motores modernos.
A química de muitos sistemas, incluindo combustão e atmosferas planetárias, é governado por mecanismos químicos complexos, onde a conversão geral de um conjunto de reagentes iniciais em um conjunto de produtos finais passa por muitas moléculas químicas intermediárias com muitas reações químicas individuais ocorrendo no nível molecular. Nossa compreensão atual dos complexos mecanismos de combustão e das atmosferas planetárias tem como premissa as classes de reações que podem ocorrer. Até agora, apenas três classes de reações foram consideradas:
O gás do banho é geralmente considerado um inerte, ou não reativo, molécula que não participa de nenhuma quebra ou formação de ligação, mas, em vez disso, tira alguma energia do outro complexo molecular (que teria energia cinética interna suficiente para se decompor espontaneamente se nenhuma energia fosse retirada).
Se, em vez disso, o complexo molecular colide com uma molécula reativa, então, a terceira molécula pode participar do processo de quebra / formação da ligação, produzindo o que Burke e Klippenstein chamam de produto de "reação quimicamente termolecular". "Em nosso jornal, mostramos a importância das reações envolvendo complexos H + O2 com outras espécies radicais, por exemplo. H + O2 + H, em ambientes de combustão, "ele observa." No entanto, dado o fato de que as moléculas reativas, como radicais livres e oxigênio molecular, são os principais constituintes da combustão e de certos ambientes planetários, há um potencial significativo para que outras reações termoleculares quimicamente ocorram e desempenhem um papel significativo em outros ambientes. "
William H. Green, professor de engenharia química no MIT, diz do estudo, "Há muito se sabe que muitas reações de associação de fase gasosa têm taxas efetivas muito baixas, porque o aduto energizado inicial não vive o suficiente para ser estabilizado por transferência de energia por colisão, e simplesmente desmorona de volta para os reagentes. Isso levou o campo a pensar que esses adutos transitórios podem ser completamente ignorados. Este artigo revela que mesmo que as reações unimoleculares de adutos energizados sejam desprezíveis, eles ainda podem participar de reações bimoleculares, com consequências surpreendentemente importantes. "
Burke planeja, em seguida, generalizar essas teorias e métodos para calcular as taxas de reação termolecular quimicamente para permitir cálculos semelhantes em ambientes de alta pressão, onde as colisões entre as moléculas são ainda mais frequentes, importante para projetos de motores de última geração. Ele também explorará as implicações da descoberta para outras reações e ambientes químicos, como aqueles envolvidos na formação e redução de poluentes ou na química das atmosferas planetárias.