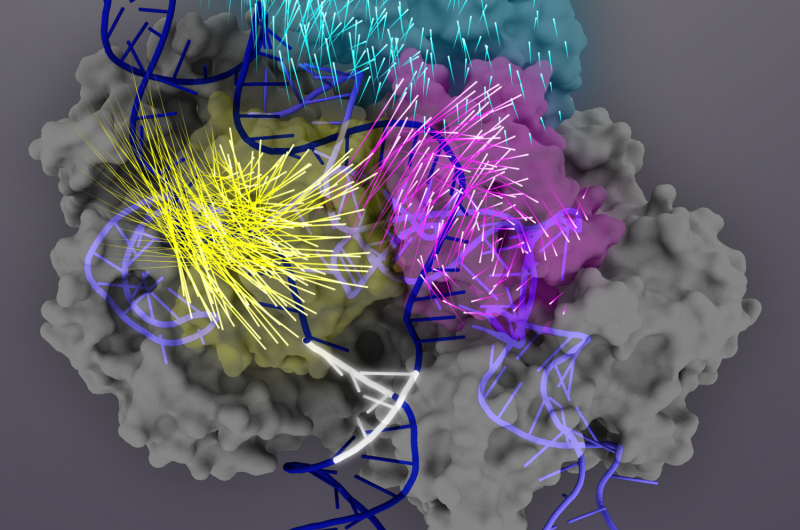
 p A proteína Cas9 (cinza) é uma nuclease guiada por RNA que pode ser programada para se ligar e cortar qualquer sequência de DNA correspondente (dupla hélice azul escura), tornando-o uma ferramenta poderosa para a engenharia do genoma. Após a ligação ao alvo, Os domínios da proteína Cas9 sofrem rearranjos conformacionais (os movimentos de aminoácidos individuais são representados por caudas de foguete) para ativar o complexo Cas9-sgRNA para clivagem alvo. O domínio REC3 (azul-petróleo) é responsável pela detecção do alvo, que sinaliza a rotação para fora do domínio REC2 (magenta) para abrir um caminho para o domínio de nuclease HNH (amarelo). Esta conformação ativa de Cas9 é então capaz de desencadear a clivagem concertada de ambas as fitas do DNA alvo. Crédito:Janet Iwasa gráfico para Doudna Lab
p A proteína Cas9 (cinza) é uma nuclease guiada por RNA que pode ser programada para se ligar e cortar qualquer sequência de DNA correspondente (dupla hélice azul escura), tornando-o uma ferramenta poderosa para a engenharia do genoma. Após a ligação ao alvo, Os domínios da proteína Cas9 sofrem rearranjos conformacionais (os movimentos de aminoácidos individuais são representados por caudas de foguete) para ativar o complexo Cas9-sgRNA para clivagem alvo. O domínio REC3 (azul-petróleo) é responsável pela detecção do alvo, que sinaliza a rotação para fora do domínio REC2 (magenta) para abrir um caminho para o domínio de nuclease HNH (amarelo). Esta conformação ativa de Cas9 é então capaz de desencadear a clivagem concertada de ambas as fitas do DNA alvo. Crédito:Janet Iwasa gráfico para Doudna Lab
p Cientistas da Universidade da Califórnia, Berkeley e o Hospital Geral de Massachusetts identificaram uma região-chave dentro da proteína Cas9 que rege a precisão com que CRISPR-Cas9 se localiza em uma sequência de DNA alvo, e o ajustamos para produzir um editor de genes hiperpreciso com o nível mais baixo de corte fora do alvo até o momento. p O domínio da proteína que os pesquisadores identificaram como um controlador mestre de corte de DNA é um alvo óbvio para a reengenharia para melhorar ainda mais a precisão, dizem os pesquisadores. Esta abordagem deve ajudar os cientistas a personalizar as variantes de Cas9 - a proteína que se liga e corta o DNA - para minimizar a chance de que CRISPR-Cas9 edite o DNA no lugar errado, uma consideração importante ao fazer terapia gênica em humanos.
p Uma estratégia para alcançar maior precisão é criar mutações no domínio da proteína governante, chamado REC3, e veja quais melhoram a precisão sem afetar a eficiência do corte no alvo.
p "Descobrimos que mesmo pequenas alterações no domínio REC3 de Cas9 afetam a diferença entre a edição on- e off-target, o que sugere que este domínio é um candidato óbvio para mutagênese em profundidade para melhorar a especificidade de direcionamento. Como uma extensão deste trabalho, alguém poderia realizar uma mutagênese mais imparcial dentro de REC3 do que as mutações direcionadas que fizemos, "disse a co-autora Janice Chen, uma estudante de pós-graduação no laboratório de Jennifer Doudna, que co-inventou a ferramenta de edição de genes CRISPR-Cas9.
p Co-primeiros autores Chen, Yavuz Dagdas e Benjamin Kleinstiver, e seus colegas da UC Berkeley, O Massachusetts General Hospital e a Harvard University relatam seus resultados online hoje, antes da publicação no jornal
Natureza .
p
Cas9 hiperpreciso
p Desde 2012, quando Doudna, professor de biologia molecular e celular e investigador do Howard Hughes Medical Institute na UC Berkeley, e a colega Emmanuelle Charpentier, do Instituto Max Planck de Biologia de Infecções, reaproveitou a proteína Cas9 para criar um editor de genes preciso e fácil de usar, pesquisadores têm procurado diminuir as chances de edição fora do alvo. Embora a fidelidade melhorada beneficie a pesquisa básica, é absolutamente crítico ao editar genes para aplicações clínicas, uma vez que qualquer corte de DNA fora do alvo pode desativar genes-chave e levar à permanente, efeitos colaterais inesperados.
p Nos últimos dois anos, duas equipes projetaram proteínas Cas9 altamente precisas - uma de especificidade aprimorada chamada eSpCas9 (1.1) e outra de alta fidelidade chamada SpCas9-HF1 - e Chen e Doudna procuraram saber por que cortam com especificidade mais alta do que a proteína Cas9 de tipo selvagem de Streptococcus pyogenes amplamente utilizados hoje.
p Atualmente, pesquisadores usando CRISPR-Cas9 criam um RNA de guia único (sgRNA) - uma molécula de RNA que inclui uma cadeia de 20 ácidos ribonucleicos que complementa uma sequência específica de DNA de 20 ácidos nucleicos que eles desejam ter como alvo - e anexa-a ao Cas9. Este guia de RNA permite que Cas9 se concentre no DNA complementar, ligue-se a ele e corte a hélice de fita dupla. Mas o complexo Cas9-sgRNA também pode se ligar ao DNA que não corresponde exatamente, levando a cortes indesejáveis fora do alvo.
p Em 2015, O laboratório de Doudna descobriu um interruptor conformacional de Cas9 que é ativado quando o guia de RNA e o alvo de DNA combinam. Eles descobriram que apenas quando o RNA e o DNA se combinam de perto a estrutura 3D de Cas9, em particular, a conformação do domínio de nuclease HNH, mude e ative a tesoura de Cas9. Contudo, o processo responsável por detectar os ácidos nucléicos a montante do switch conformacional permaneceu desconhecido.
p No estudo atual, Chen e Dagdas usaram uma técnica chamada FRET de molécula única (transferência de energia de ressonância de Förster) para medir com precisão como os vários domínios de proteína no complexo de proteína Cas9-sgRNA - em particular REC3, REC2 e HNH - movem-se quando o complexo se liga ao DNA.
p Eles primeiro determinaram que os benefícios de especificidade conferidos por eSpCas9 (1.1) e SpCas9-HF1 poderiam ser explicados pelo fato de que o limite para a mudança conformacional de HNH era muito maior para essas variantes Cas9 do que para a proteína Cas9 de tipo selvagem, tornando as variantes eSpCas9 (1.1) e SpCas9-HF1 menos prováveis de ativar a tesoura quando ligadas a uma sequência fora do alvo.
p Próximo, eles descobriram que o domínio REC3 é responsável por detectar a precisão da ligação ao alvo, que então sinaliza a rotação para fora do domínio REC2 para abrir um caminho para o domínio de nuclease HNH, ativando a tesoura. Esta conformação ativa de Cas9 é então capaz de clivar ambas as fitas do DNA alvo.
p Chen, Dagdas e Kleinstiver mostraram que, ao transformar partes de REC3, é possível alterar a especificidade da proteína Cas9 para que a nuclease HNH não seja ativada, a menos que a correspondência do RNA guia e do DNA alvo seja muito próxima. Eles foram capazes de projetar um Cas9 hiperpreciso e aprimorado, apelidado de HypaCas9, que retém sua eficiência no alvo, mas é ligeiramente melhor em discriminar entre locais dentro e fora do alvo em células humanas.
p "Se você transformar certos resíduos de aminoácidos em REC3, você pode ajustar o equilíbrio entre a atividade do Cas9 no alvo e a especificidade aprimorada; conseguimos encontrar o ponto ideal onde há atividade suficiente no alvo pretendido, mas também uma grande redução nos eventos fora do alvo, "Chen disse.
p Continuando a explorar as relações entre a estrutura, função e dinâmica do Cas9, Doudna e sua equipe esperam desenvolver ainda mais a proteína com sensibilidade requintada para realizar de forma confiável e eficiente uma variedade de alterações genéticas.
