Figura 1:Dois feixes de laser interagem com moléculas na superfície do gelo, formando um novo feixe com uma cor diferente. A cor e a intensidade desse feixe de laser contêm informações detalhadas sobre a estrutura molecular da superfície do gelo. Crédito:Organização Holandesa para Pesquisa Científica (NWO)
É a uma temperatura de -70 ° C que as moléculas de água na superfície do gelo fazem mais ligações umas com as outras. Pesquisadores AMOLF, junto com uma equipe internacional de colegas, descreva isso em um artigo em Cartas de revisão física publicado em 28 de setembro. Os insights sobre o comportamento da camada superior de gelo são importantes para entender como as geleiras se movem, como surgem as avalanches, e porque podemos patinar no gelo, entre outras coisas.
A água é uma substância estranha:ela se expande quando congela. Como a forma sólida de água (gelo) tem uma densidade menor do que a variante líquida, o gelo flutua na água. Isso significa que você pode patinar em um lago durante um inverno rigoroso, enquanto os peixes embaixo de você continuam a nadar. Esta propriedade incomum é causada pela estrutura molecular da água. Uma molécula de água consiste em um átomo de oxigênio com dois átomos de hidrogênio. Os átomos de hidrogênio formam uma ligação forte com um átomo de oxigênio de outra molécula de água:chamamos isso de ligação de hidrogênio.
Cada átomo de oxigênio pode se ligar a no máximo quatro átomos de hidrogênio:dois de sua própria molécula de água, e dois de moléculas próximas. Isso pode acontecer no centro de um pedaço de gelo profundamente congelado, em que as moléculas de água assumem uma estrutura cristalina que se parece com uma coleção de hexágonos regulares. Esta estrutura cristalina ocupa muito espaço, e é isso que torna a densidade do gelo baixa.
Contudo, as moléculas de água na superfície do gelo têm um problema. Essas moléculas de água não estão em uma interface com outras moléculas de água, mas com o ar, então eles não podem utilizar suas possibilidades de vínculo ao máximo.
Número máximo de títulos
Wilbert Smit, pesquisador do AMOLF, e Huib Bakker, líder do grupo AMOLF, estudaram como a estrutura da camada mais externa de gelo muda como consequência da temperatura. Eles descobriram que a uma temperatura ambiente de cerca de -70 ° C, as moléculas de água na superfície do gelo formam um número máximo de ligações de hidrogênio. Os pesquisadores também encontraram uma explicação para isso.
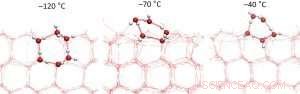
Figura 2:Cortes transversais da superfície do gelo em diferentes temperaturas. A estrutura hexagonal começa a derreter em temperaturas abaixo de −70 ° C, o que inicialmente leva a uma densidade maior de ligações de hidrogênio na superfície do gelo. A -70 ° C, o número máximo de ligações de hidrogênio é atingido. Crédito:Organização Holandesa para Pesquisa Científica (NWO)
"Se estiver muito mais frio do que −70 ° C, então, a camada mais externa do gelo tem a mesma estrutura dos hexágonos regulares abaixo dela, mas perfeitamente cortado ao meio. Você pode comparar a estrutura a uma casa semi-construída onde as hastes de concreto armado ainda estão saindo das paredes do primeiro andar ", diz Wilbert Smit.
Conforme a temperatura sobe, a superfície do gelo torna-se menos estruturada devido às moléculas de água adquirirem mais energia cinética. Como resultado disso, eles se reorganizam de tal forma que o número de ligações entre as moléculas de água aumenta inicialmente. Esse rearranjo produz uma densidade mais alta de ligações de hidrogênio a uma temperatura de -70 ° C.
Em temperaturas acima de −70 ° C, o número de ligações entre as moléculas diminui novamente:a camada superior se comporta cada vez mais como água e menos como gelo. Isso significa, por exemplo, que a superfície do gelo em que patinamos não é realmente gelo, mas uma camada de água.
Simulações e técnica sensível
Os pesquisadores holandeses usaram uma técnica avançada para a pesquisa chamada espectroscopia de geração de frequência de soma. Essa técnica torna possível detectar as vibrações das moléculas em superfícies, iluminando a superfície com dois feixes de luz laser de femtossegundos intensos. Sob as condições certas, os feixes de luz interagem com as moléculas na superfície e um feixe de luz com uma cor diferente é formado. Isso só ocorre quando as vigas são refletidas na superfície e não na estrutura subjacente. A cor e a intensidade da nova viga, portanto, contêm exclusivamente informações detalhadas sobre a estrutura da superfície. Com a ajuda de simulações do Instituto Max Planck em Mainz, os pesquisadores foram capazes de traduzir esses resultados em novos conhecimentos sobre a superfície do gelo.