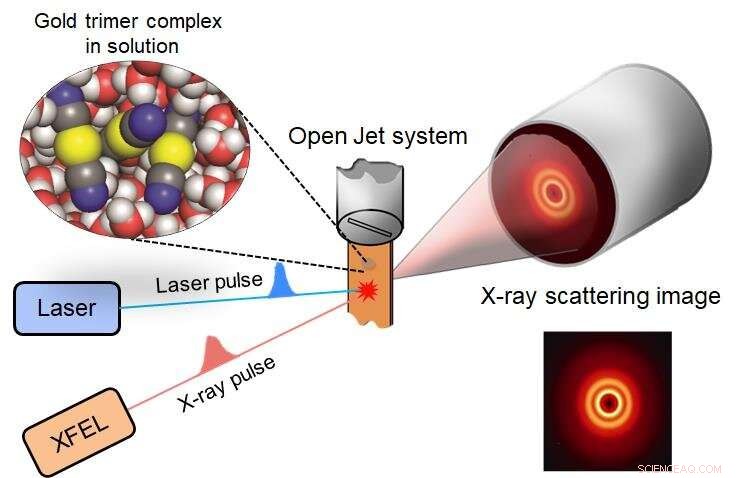
A reação de formação de ligação em um complexo de trímero de ouro é iniciada por um pulso de laser, e uma estrutura tridimensional após um certo atraso de tempo é detectada por uma imagem de espalhamento de raios-x. Crédito:IBS
As drogas direcionadas ao câncer atuam ao estabelecer um vínculo estreito entre as células cancerosas e os alvos moleculares específicos que estão envolvidos no crescimento e na disseminação do câncer. Imagens detalhadas de tais locais de ligação química ou vias podem fornecer informações essenciais necessárias para maximizar a eficácia dos tratamentos de oncogene. Contudo, movimentos atômicos em uma molécula nunca foram capturados no meio da ação, nem mesmo para uma molécula extremamente simples, como uma molécula triatômica, feito de apenas três átomos.
Uma equipe de pesquisa liderada por Ihee Hyotcherl do Institute for Basic Science (IBS, Coreia do Sul) (Professor, Departamento de Química, KAIST), em colaboração com cientistas do Instituto de Ciência da Estrutura de Materiais de KEK (KEK IMSS, Japão), RIKEN (Japão) e Pohang Accelerator Laboratory (PAL, Coreia do Sul), relataram a observação direta do momento do nascimento de ligações químicas rastreando as posições atômicas em tempo real na molécula.
"Finalmente conseguimos capturar o processo de reação em curso da formação da ligação química no trímero de ouro. As imagens de resolução de femtossegundo revelaram que tais eventos moleculares ocorreram em dois estágios separados, não simultaneamente como assumido anteriormente, "diz o Diretor Associado Ihee Hyotcherl, o autor correspondente do estudo. "Os átomos do complexo do trímero de ouro permanecem em movimento mesmo depois que a ligação química está completa. A distância entre os átomos aumentava e diminuía periodicamente, exibindo a vibração molecular. Essas vibrações moleculares visualizadas nos permitiram nomear o movimento característico de cada modo vibracional observado, "acrescenta Ihee.
Os átomos se movem extremamente rápido em uma escala de femtosegundo (fs) - quadrilionésimos de segundo. O movimento é mínimo no nível dos angstroms, igual a um décimo bilionésimo de um metro. Eles são especialmente evasivos durante o estado de transição, em que os intermediários da reação estão em transição de reagentes para produtos em um piscar de olhos. A equipe de pesquisa tornou essa tarefa experimentalmente desafiadora possível usando liquidografia de raios-X de femtosegundo (espalhamento de solução).
Esta técnica experimental combina fotólise a laser e técnicas de espalhamento de raios-X. Quando um pulso de laser atinge a amostra, Os raios X se espalham e iniciam a reação de formação da ligação química no complexo do trímero de ouro. Pulsos de raios-X de femtossegundos obtidos de uma fonte de luz especial chamada laser de elétrons livres de raios-X (XFEL) foram usados para interrogar o processo de formação da ligação. Os experimentos foram realizados em duas instalações XFEL (acelerador linear de 4ª geração), PAL-XFEL na Coreia do Sul e SACLA no Japão, e este estudo foi realizado em colaboração com pesquisadores da KEK IMSS, Pohang Accelerator Laboratory (PAL), RIKEN, e o Instituto de Pesquisa em Radiação Síncrotron do Japão (JASRI).
Ondas dispersas de cada átomo interferem umas nas outras e, portanto, suas imagens de espalhamento de raios-X são caracterizadas por direções de viagem específicas. A equipe de pesquisa IBS traçou as posições em tempo real dos três átomos de ouro ao longo do tempo, analisando imagens de espalhamento de raios-X, que são determinados por uma estrutura tridimensional de uma molécula. Mudanças estruturais no complexo da molécula resultaram em imagens de espalhamento de características múltiplas ao longo do tempo. Quando uma molécula é excitada por um pulso de laser, múltiplos estados quânticos vibracionais são simultaneamente excitados. A superposição de vários estados quânticos vibracionais excitados é chamada de pacote de ondas. Os pesquisadores rastrearam o pacote de ondas em coordenadas nucleares tridimensionais e descobriram que a primeira metade da rodada de ligação química foi formada dentro de 35 fs após a fotoexcitação. A segunda metade da reação seguiu em 360 fs para completar toda a dinâmica da reação.
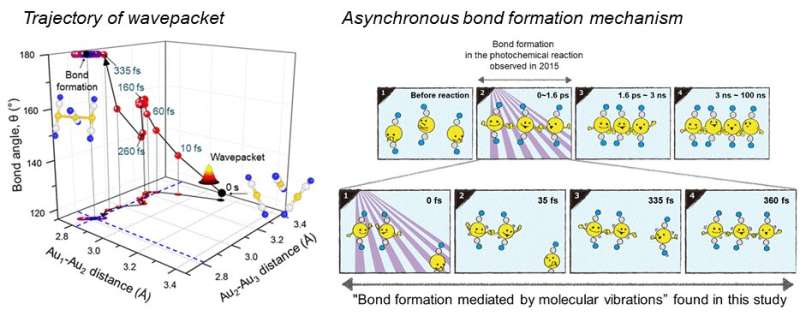
(esquerda) As posições dependentes do tempo do pacote de onda nas coordenadas nucleares multidimensionais foram obtidas a partir do experimento de espalhamento de raios-X de femtossegundo em um complexo de trímero de ouro. (Crédito:Nature &IBS) (à direita) Ao inspecionar o movimento do pacote de ondas, foi revelado que a reação de formação de ligação no complexo de trímero de ouro ocorre através de um mecanismo de formação de ligação assíncrona. (Amarelo:átomos de ouro, cinza:átomo de carbono, azul:átomo de nitrogênio, 1000 vezes 1 fs é 1 picossegundo (ps), 1000 vezes 1 ps é 1 nanossegundo (ns)) Crédito:(esquerda) Nature &IBS, (direita) KEK IMSS
Os pesquisadores também ilustraram com precisão os movimentos de vibração molecular tanto temporal quanto espacialmente. Este é um feito notável, considerando que uma velocidade ultrarrápida e um comprimento mínimo de movimento são condições muito desafiadoras para a aquisição de dados experimentais precisos.
Neste estudo, a equipe de pesquisa IBS melhorou seu estudo de 2015 publicado pela Natureza . No estudo anterior em 2015, a velocidade da câmera de raios-X (resolução de tempo) foi limitada a 500 fs, e a estrutura molecular já havia mudado para ser linear com duas ligações químicas dentro de 500 fs. (Figura 2, superior direito) Neste estudo, o progresso da formação da ligação e da transformação estrutural curvada para linear pode ser observado em tempo real, graças à resolução de tempo de melhoria até 100 fs. Deste modo, o mecanismo de formação de ligação assíncrona em que duas ligações químicas são formadas em 35 fs e 360 fs, respectivamente, e a transformação curvada para linear concluída em 335 fs foram visualizadas (Figura 2, inferior direito). Resumidamente, além de observar o início e o fim das reações químicas, eles relataram cada etapa do intermediário, reorganização contínua das configurações nucleares com métodos experimentais e analíticos dramaticamente aprimorados.
A equipe de pesquisa vai empurrar este método de 'rastreamento em tempo real de posições atômicas em uma molécula e vibração molecular usando espalhamento de raios-X de femtossegundo' para revelar os mecanismos de reações catalíticas orgânicas e inorgânicas e reações envolvendo proteínas no corpo humano. "Ao rastrear diretamente as vibrações moleculares e as posições em tempo real de todos os átomos em uma molécula no meio da reação, seremos capazes de descobrir mecanismos de várias reações catalíticas orgânicas e inorgânicas desconhecidas e reações bioquímicas, "diz o Dr. KIM Jong Goo, o primeiro autor do estudo.
O estudo é publicado em Natureza .