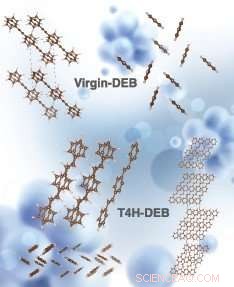
Estruturas cristalinas simuladas de DEB virgem e T4H-DEB (quimicamente conhecido como 1, 4-distirilbenzeno, um isômero trans do produto intermediário DEB após a captura dos primeiros 4 átomos de hidrogênio com 2 ligações CH em lados opostos da cadeia de carbono). As estruturas superior esquerda e superior direita correspondem à vista lateral e superior da DEB virgem, respectivamente. O meio direito, as estruturas inferior direita e inferior esquerda correspondem à vista lateral, vista superior e uma célula unitária (vista lateral) de T4H-DEB, respectivamente. Crédito:A simulação foi realizada por Hom Sharma. A renderização artística da imagem foi feita por Alexandria Holmberg Diaz, Laboratório Nacional Lawrence Livermore.
O excesso de hidrogênio pode causar problemas em diversos setores. Pode corroer semicondutores, eletrônicos, e combustível nuclear armazenado. Também apresenta risco de explosão. Para remover esse hidrogênio extra, os químicos podem usar um composto orgânico chamado getter de hidrogênio, que se liga quimicamente a vários átomos de hidrogênio.
Mas às vezes, durante este processo de ligação - chamado de hidrogenação catalítica - os produtos parcialmente hidrogenados tornam-se voláteis, derretendo e evaporando antes que eles possam se ligar a mais átomos de hidrogênio. Agora, pesquisadores exploraram como e por que essa volatilidade varia durante a hidrogenação, sugerindo que um efeito anteriormente subestimado das ligações carbono-hidrogênio na molécula é o principal culpado.
A nova análise, publicado em The Journal of Chemical Physics , pode ajudar os químicos a identificar as condições ideais necessárias para a hidrogenação catalítica para que possam remover melhor o excesso de hidrogênio.
"Isso cria um modelo para o comportamento de outros getters orgânicos, permitindo-nos prever suas temperaturas e ambientes operacionais ideais, "disse Long Dinh, um físico do Laboratório Nacional Lawrence Livermore.
Dinh e seus colegas se concentraram em um getter chamado 1, 4 bis (feniletinil) benzeno, ou DEB. Para remover o hidrogênio, flocos de cristal de DEB são misturados com catalisadores na forma de pellets sólidos. Os pellets são feitos de carvão ativado - cuja estrutura porosa fornece uma área de superfície abundante - revestidos com nanopartículas de paládio. O catalisador de paládio divide as moléculas de hidrogênio em átomos de hidrogênio, que pode então se ligar a DEB e formar ligações carbono-hidrogênio.
DEB é um getter de alta capacidade, capaz de se ligar a até oito átomos de hidrogênio. A maioria dos pesquisadores pensou que, à medida que getters como o DEB se ligam a mais átomos de hidrogênio e aumentam, eles se tornam mais voláteis. Em altas temperaturas de operação, eles podem então evaporar, afastando-se dos pellets catalíticos, onde não há átomos de hidrogênio com os quais se ligar. "Você para o processo de hidrogenação prematuramente, "Dinh disse.
Mas os pesquisadores descobriram que nas duas primeiras etapas da hidrogenação, quando DEB forma duas ligações carbono-hidrogênio por etapa (as ligações carbono-hidrogênio são criadas em lados opostos da cadeia de carbono da molécula), a molécula realmente diminui em volatilidade. Somente nas etapas subsequentes de hidrogenação o DEB se torna mais volátil.
Para estudar como e por que o DEB muda na volatilidade, os pesquisadores mediram propriedades como pressões de vapor e pontos de fusão, estrutura molecular sondada, e executou simulações de computador de mecânica quântica para modelar o processo de hidrogenação. Sua análise sugere que as ligações carbono-hidrogênio em DEB desempenham um papel fundamental no comportamento volátil da molécula.
Durante a hidrogenação, hidrogênio se liga a átomos de carbono em DEB. De acordo com o pensamento convencional, a ligação carbono-hidrogênio resultante é apolar - nenhuma das extremidades da estrutura da barra tem carga mais negativa ou positiva do que a outra. Mas acontece que a extremidade do carbono é um pouco mais negativa, e a ligação carbono-hidrogênio forma um dipolo fraco, Dinh explicou.
Como um dipolo, uma ligação carbono-hidrogênio pode atrair ou repelir outras ligações carbono-hidrogênio em outras moléculas DEB. Dependendo de como as ligações carbono-hidrogênio estão organizadas e quantas existem nos produtos DEB intermediários, as moléculas podem atrair ou repelir umas às outras, e, portanto, ser menos ou mais volátil, respectivamente. Pesquisas anteriores haviam negligenciado essas interações coletivas entre ligações de carbono-hidrogênio em cristais orgânicos, Disse Dinh.
De sua análise, os pesquisadores determinaram que as condições ideais para hidrogenação de DEB são abaixo de cerca de 175 graus Fahrenheit, se feito em um bom vácuo. "Nossos resultados, "Dinh disse, "pode ser aplicado de forma análoga a outros sistemas catalíticos de obtenção de hidrogênio orgânico também."