Integração de previsão teórica e eletrooxidação experimental de glicerol em nanofolhas
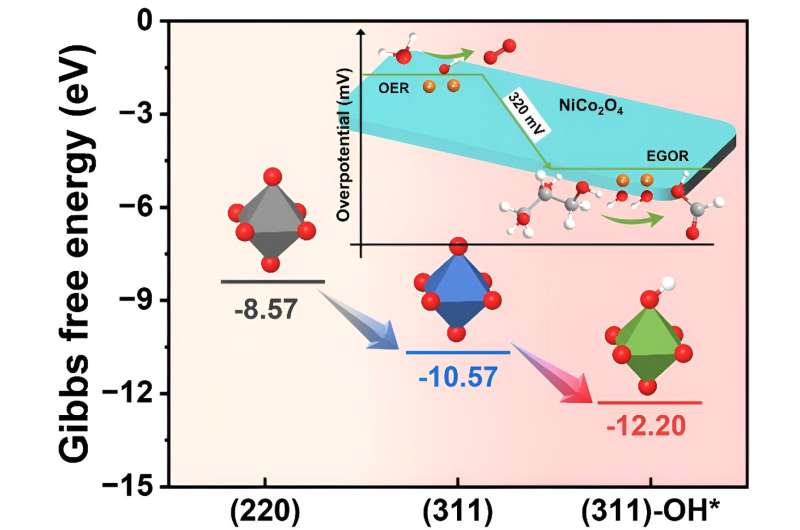 Cálculos DFT combinados com métodos eletroquímicos, o potencial de NiCo2 O4 catalisadores para reação eletrocatalítica de oxidação do glicerol (EGOR) foram explorados. O NiCo meticulosamente construído2 O4 os catalisadores demonstraram excelente potencial de adsorção de OH*. O OH* gerado in-situ durante o processo de reação alcançou excelente eficiência eletrocatalítica, reduzindo a energia de ativação para regular a etapa determinante da taxa (RDS). Crédito:Jornal Chinês de Catálise (2024). DOI:10.1016/S1872-2067(23)64585-1
Cálculos DFT combinados com métodos eletroquímicos, o potencial de NiCo2 O4 catalisadores para reação eletrocatalítica de oxidação do glicerol (EGOR) foram explorados. O NiCo meticulosamente construído2 O4 os catalisadores demonstraram excelente potencial de adsorção de OH*. O OH* gerado in-situ durante o processo de reação alcançou excelente eficiência eletrocatalítica, reduzindo a energia de ativação para regular a etapa determinante da taxa (RDS). Crédito:Jornal Chinês de Catálise (2024). DOI:10.1016/S1872-2067(23)64585-1 O glicerol, um importante subproduto do refino de biomassa, responsável por aproximadamente 10% do rendimento, apresenta um desafio significativo devido ao seu excedente global. A presença de múltiplos grupos hidroxila ativos no glicerol revela um vasto potencial para a produção de produtos químicos de alto valor. O ácido fórmico (AF), um produto chave da conversão do glicerol, é uma matéria-prima química orgânica crítica com alta demanda em setores como pesticidas, produtos farmacêuticos e energia.
A oxidação do glicerol em FA não apenas mitiga o desperdício causado pelo excedente de recursos, mas também atende às necessidades futuras das células de combustível FA. Atualmente, a produção industrial de FA depende principalmente de metanol derivado de petróleo e gás natural, tornando a conversão eletrocatalítica de glicerol à base de biomassa em FA altamente promissora.
No entanto, a reação de oxidação eletrocatalítica do glicerol (RGOR) é complexa, envolvendo desidrogenação, adsorção/dessorção e quebra da ligação CC dos intermediários da reação, colocando desafios à eficiência e seletividade da reação.
Recentemente, uma equipe de pesquisa liderada pelo Prof. Kai Yan da Universidade Sun Yat-sen, China, utilizando uma combinação de cálculos da teoria do funcional da densidade (DFT) e métodos experimentais, revelou o papel crucial da espécie ativa OH* no processo EGOR. na produção de FA. A análise DFT, partindo de uma perspectiva termodinâmica, investigou o mecanismo do OH* no processo EGOR.
Verificou-se que as espécies OH* superficiais, ao reduzir a energia de adsorção do glicerol no NiCo2 O4 superfície do catalisador (de -12,20 a -10,57 eV), facilitou o processo EGOR e otimizou a etapa determinante da taxa (RDS) alterando a energia de adsorção dos intermediários, passando da desidrogenação menos eficiente do ácido glicérico para a etapa de desidrogenação mais eficiente do ácido glicérico. gliceraldeído.
Além disso, a energia de adsorção de OH* durante o processo EGOR foi significativamente menor em comparação com o processo de reação de evolução de oxigênio (REA) (0,66 vs. 2,70 eV), indicando a ocorrência preferencial de EGOR sobre REA.
Além disso, o desempenho de um NiCo2 meticulosamente projetado O4 eletrodo em EGOR foi investigado através de métodos eletroquímicos. Em um eletrólito misto de 1 mol L
-1
KOH e 0,1 mol L
-1
glicerol, o potencial de início do eletrodo caiu para 1,16 VRHE , superando significativamente os REA. Experimentos com eletrodo de disco-anel giratório (RRDE) também confirmaram a ocorrência preferencial de EGOR, alinhando-se com os resultados da análise DFT.
Com base no mecanismo convencional de transferência de elétrons acoplados a prótons, duas possíveis vias de oxidação eletroquímica (via de oxidação direta e via de oxidação indireta) de OH* foram investigadas usando potenciação em múltiplas etapas e métodos simultâneos de ressonância eletrônica. Resultados experimentais demonstraram que o desempenho excepcional do NiCo2 O4 O eletrodo no EGOR está intimamente relacionado à geração in situ de OH* participando diretamente da reação.
Em um teste de estabilidade de ciclo de longo prazo de 120 h, o catalisador também apresentou uma taxa de conversão de glicerol eficiente e estável (89%) e seletividade ao ácido fórmico (70%). Este trabalho fornece orientações e insights valiosos para o projeto e desenvolvimento de catalisadores eficientes e estáveis para a oxidação do glicerol. Os resultados foram publicados no Chinese Journal of Catalysis .
