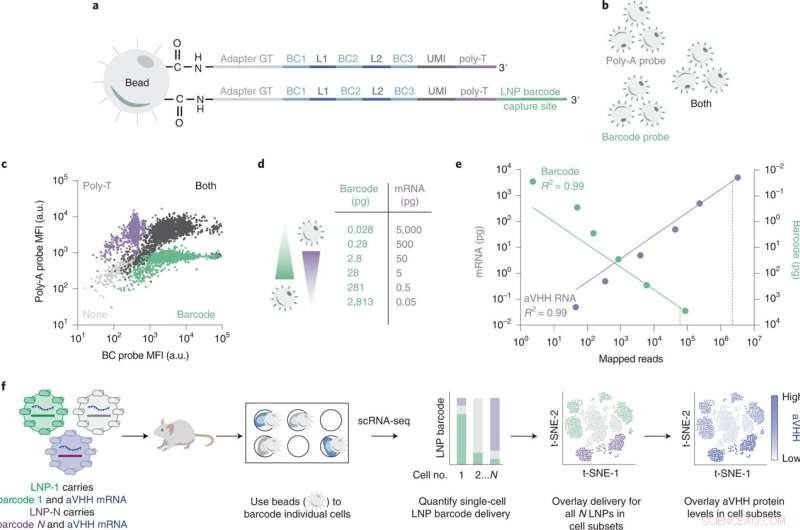
SENT-seq usa sequências de captura ortogonais para gerar leituras multiômicas ajustáveis. Crédito:Natureza Nanotecnologia (2022). DOI:10.1038/s41565-022-01146-9
A terapêutica baseada no RNA mensageiro, ou mRNA, pode potencialmente tratar uma ampla gama de doenças, incluindo câncer, doenças genéticas e, como o mundo aprendeu nos últimos anos, vírus mortais.
Para funcionar, esses medicamentos devem ser entregues diretamente às células-alvo em bolhas de gordura em nanoescala chamadas nanopartículas lipídicas, ou LNPs – o mRNA não é muito bom se não atingir o tipo de célula certo.
Uma equipe de pesquisadores do Instituto de Tecnologia da Geórgia e da Escola de Medicina da Universidade Emory deu mais um passo para melhorar o desenvolvimento desses veículos de entrega personalizados, relatando seu trabalho em 30 de junho na
Nature Nanotechnology . Curtis Dobrowolski e Kalina Paunovska, estagiários no laboratório de James Dahlman, desenvolveram um sistema para tornar os estudos pré-clínicos de nanopartículas mais preditivos. Suas descobertas já estão influenciando a direção da pesquisa neste campo crescente e competitivo.
"Estou muito animado com este estudo e antecipo a mudança da maioria de nossos projetos futuros para essa metodologia", disse Dahlman, professor associado e professor de início de carreira da Fundação McCamish no Departamento de Engenharia Biomédica Wallace H. Coulter da Georgia Tech e Emory.
Sequência de eventos Nos últimos anos, Dahlman fez parceria com o professor Philip Santangelo da Coulter BME em uma empresa de pesquisa movimentada. O laboratório de Santangelo desenvolve terapias de mRNA e o laboratório de Dahlman as entrega usando LNPs.
Para acelerar o processo de testar a eficácia de seus LNPs, a equipe de Dahlman desenvolveu uma técnica chamada DNA barcoding. Nesse processo, os pesquisadores inserem um trecho de DNA que corresponde a um determinado LNP. Os LNPs são então injetados e as células são posteriormente examinadas quanto à presença dos "códigos de barras" usando sequenciamento genético. O sistema identifica quais códigos de barras atingiram quais alvos específicos, destacando as nanopartículas mais promissoras. Uma vez que muitas sequências de DNA podem ser lidas ao mesmo tempo, o processo de código de barras permite que muitos experimentos sejam realizados simultaneamente, acelerando assim a descoberta de transportadores de nanopartículas lipídicas eficazes.
O código de barras de DNA melhorou significativamente o processo de triagem pré-clínica de nanopartículas. Mas ainda há uma barreira significativa que afeta a entrega de medicamentos. Por causa de sua diversidade, as células são como alvos móveis. Dahlman observou que as células anteriormente consideradas homogêneas são compostas de subconjuntos de células distintos e variados. Sua equipe supôs que essa heterogeneidade química e genética tem uma poderosa influência sobre o quão bem os LNPs podem fornecer terapias de mRNA nas células.
"As células não têm apenas uma proteína que as define - elas são complicadas", disse Dahlman. "Eles podem ser definidos por uma combinação de coisas e, se formos honestos, eles são melhor definidos usando todos os genes que expressam ou não."
Para testar sua hipótese, os pesquisadores desenvolveram uma nova ferramenta para medir todas essas coisas de uma só vez. Seu sistema de entrega de nanopartículas multiômicas é chamado de sequenciamento de direcionamento de nanopartículas de célula única, ou SENT-seq.
Abordagem multiômica Usando SENT-seq, os pesquisadores foram capazes de quantificar como os LNPs entregam códigos de barras de DNA e mRNA nas células, a subsequente produção de proteína facilitada pela droga de mRNA, bem como a identidade da célula, em milhares de células individuais.
Essa abordagem multiômica pode representar um importante salto para a descoberta de LNP de alto rendimento. A técnica SENT-seq permitiu à equipe identificar subtipos de células que demonstram uma absorção particularmente alta ou baixa de nanopartículas e os genes associados a esses subtipos.
Assim, além de testar a eficácia de uma droga e como certos subtipos de células reagem às nanopartículas, eles estão identificando quais genes estão envolvidos na absorção bem-sucedida de LNPs. E eles estão fazendo tudo de uma vez.
"Os dados sugerem que esses diferentes subconjuntos de células têm respostas distintas às nanopartículas que influenciam o quão bem uma terapia de mRNA funciona", disse Dahlman. "Ainda há muito trabalho a ser feito, mas achamos que a capacidade de ler simultaneamente a entrega de nanopartículas de alto rendimento e a resposta celular às nanopartículas levará a melhores terapias de mRNA".
O co-autor principal Paunovska disse que ela e Dobrowolski tiveram a ideia do sistema SENT-seq, "organicamente, depois de dois meses trabalhando juntos".
Dahlman added:"I'm proud of the work that Curtis, Kalina, and the team did in the lab. I think this is the beginning of an extremely interesting phase in our work."
+ Explorar mais New system speeds screening of drug-delivering nanoparticles
