Cientistas desenvolvem nova formulação biomimética para o tratamento de glioblastoma
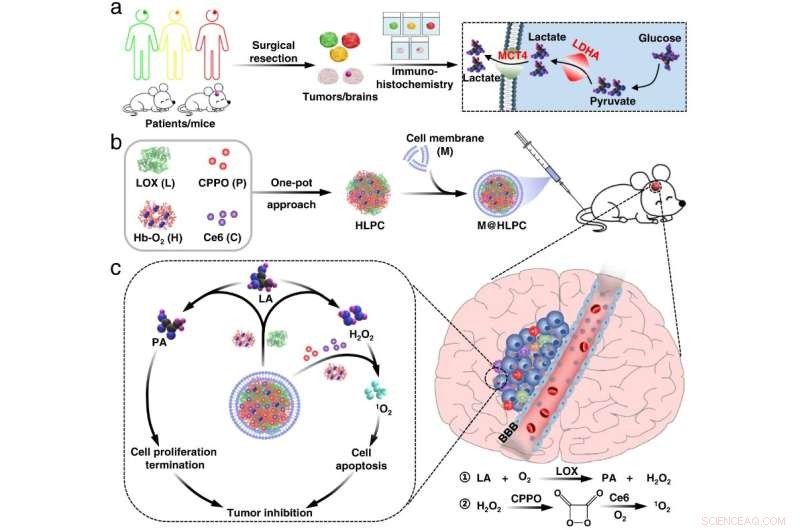
Fig. 1 Preparação da formulação biomimética e mecanismo de inibição do tumor. Crédito:Lu Guihong
O glioblastoma multiforme (GBM) é um câncer cerebral agressivo com prognóstico ruim e poucas opções de tratamento. Novas e eficazes abordagens para o tratamento do GBM são, portanto, urgentemente necessárias.
Com base na observação de lactato elevado em GBM ressecado, pesquisadores do Instituto de Engenharia de Processos (IPE) da Academia Chinesa de Ciências e do Segundo Hospital Popular de Shenzhen desenvolveram uma formulação biomimética usando agentes de entrega direcionados para terapia sinérgica baseada no metabolismo do lactato contra GBM.
O estudo foi publicado em
Nature Communications em 21 de julho.
O direcionamento do metabolismo do lactato é uma estratégia terapêutica atraente para o tumor. No entanto, não há relatos que aproveitem diretamente o metabolismo do lactato para tratamentos de GBM. Uma limitação é a existência da barreira hematoencefálica, que impede que a maioria das moléculas de drogas (incluindo aquelas que interferem no metabolismo do lactato) cheguem ao cérebro.
Além disso, considerando a complexidade e as características infiltrativas do GBM, é muito improvável que a monoterapia metabólica com lactato elimine efetivamente as células do GBM. Portanto, é vital desenvolver estratégias sinérgicas para aumentar a eficiência terapêutica da terapia metabólica com lactato.
Neste estudo, os pesquisadores coletaram amostras de glioma de uma grande coorte de pacientes e quantificaram os indicadores metabólicos de lactato LDHA e MCT4 e um marcador de proliferação representativo Ki67.
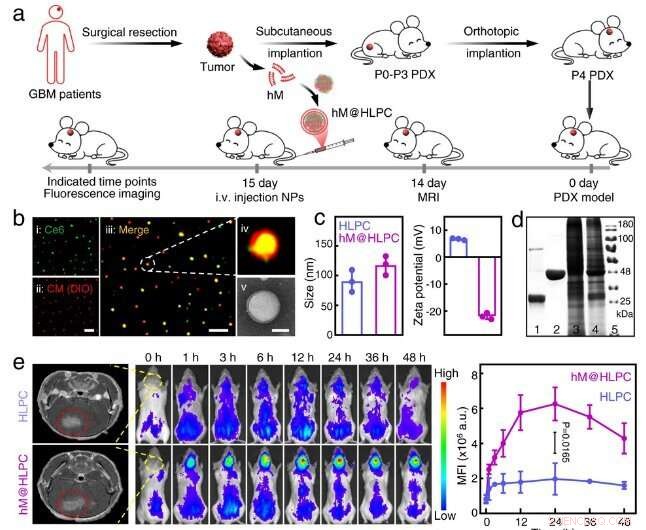
Fig. 2 Avaliação do efeito terapêutico sinérgico da formulação biomimética personalizada no modelo PDX. Crédito:Lu Guihong
"Observamos uma correlação positiva entre os indicadores metabólicos de lactato e a extensão da proliferação do glioma", disse o Prof. Li Weiping, do Segundo Hospital Popular de Shenzhen. Assim, foi proposta uma terapia sinérgica baseada no metabolismo eficiente que aproveitaria diretamente o lactato elevado no GBM.
Os pesquisadores fabricaram nanopartículas de automontagem (NPs) compostas de hemoglobina (Hb), lactato oxidase (LOX), bis[2,4,5-tricloro-6-(pentiloxicarbonil)fenil] oxalato (CPPO) e clorina e6 (Ce6). ) usando uma abordagem de um pote. Posteriormente, eles encapsularam essas NPs automontadas com materiais de membrana preparados a partir de células de glioma U251 para gerar o sistema biomimético M@HLPC. Este conceito de design foi capaz de alcançar entrega direcionada para terapia combinada.
"Após a injeção intravenosa, o M@HLPC pode atravessar a barreira hematoencefálica por meio de transcitose proveniente de integrina e reconhecimento mediado por proteínas de adesão celular vascular e, em seguida, acumulado no GBM por meio de reconhecimento homotípico baseado em proteínas associadas à função de reconhecimento celular, " disse o Prof. Wei Wei do IPE.
Nos tumores, a LOX nas NPs converteu o lactato em ácido pirúvico e peróxido de hidrogênio (H
2 O
2 ). O ácido pirúvico inibiu o crescimento de células cancerosas, bloqueando a expressão de histonas e induzindo a interrupção do ciclo celular. Em paralelo, o H
2 O
2 agiu como um combustível local para reagir com o CPPO entregue para liberar energia, que poderia então ser usada pelo fotossensibilizador co-entregue Ce6 para a geração de oxigênio singleto citotóxico para matar células de glioma.
A eficácia terapêutica potente foi confirmada em modelos de tumor de xenoenxerto derivado de linha celular e xenoenxerto derivado de paciente (PDX).
"Considerando a segurança da formulação e os potentes efeitos terapêuticos contra o modelo PDX compatível, nossa formulação biomimética personalizada tem o potencial de se traduzir em aplicação clínica", disse o Prof. Ma Guanghui do IPE.
+ Explorar mais Monitoramento ao vivo do metabolismo cerebral com fluorescência

