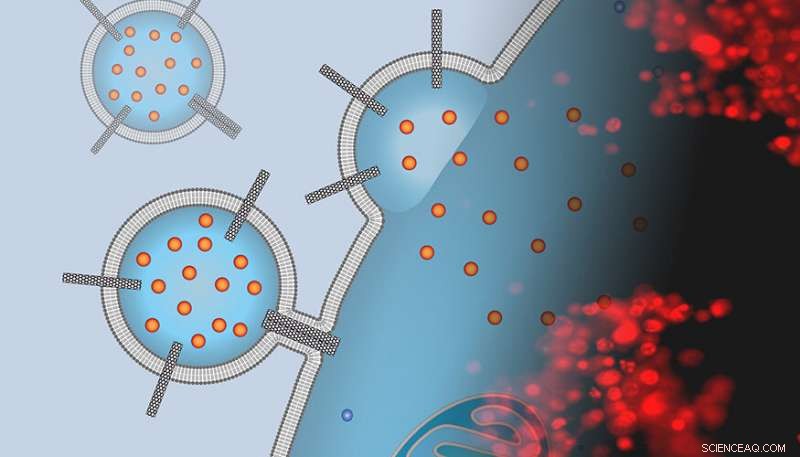
 p A imagem é uma montagem da representação de um artista de um carreador de drogas lipossomal cravejado de porinas de nanotubo de carbono que está acoplando a uma superfície de célula cancerosa e entregando carga de quimioterapia com uma imagem de microscopia de fluorescência de células coradas expostas a esses carreadores. A mancha vermelha indica que as células estão mortas e o tratamento foi bem sucedido. Crédito:P. Lastrico de MPI e N.T. Ho e A. Noy de LLNLL
p A imagem é uma montagem da representação de um artista de um carreador de drogas lipossomal cravejado de porinas de nanotubo de carbono que está acoplando a uma superfície de célula cancerosa e entregando carga de quimioterapia com uma imagem de microscopia de fluorescência de células coradas expostas a esses carreadores. A mancha vermelha indica que as células estão mortas e o tratamento foi bem sucedido. Crédito:P. Lastrico de MPI e N.T. Ho e A. Noy de LLNLL
p A medicina moderna conta com um extenso arsenal de drogas para combater doenças mortais como a pneumonia, tuberculose, HIV-AIDS e malária. Os agentes quimioterápicos prolongaram a vida de milhões de pacientes com câncer, e em alguns casos, curou a doença ou a transformou em uma condição crônica. p Mas fazer com que essas drogas cheguem às células infectadas com doenças continua sendo um grande desafio para a farmacologia e a medicina modernas. Para enfrentar esta dificuldade, Lawrence Livermore National Laboratory (LLNL) e cientistas da University of California Merced e colaboradores do Max Planck Institute of Biophysics na Alemanha usaram nanotubos de carbono para permitir a entrega direta de drogas de lipossomas através da membrana plasmática para o interior da célula, facilitando a fusão da membrana transportadora com o celular. A pesquisa aparece no
Proceedings of the National Academy of Sciences .
p Os medicamentos são frequentemente pouco solúveis, fortemente tóxico para outros tecidos ou enfrenta rápida degradação nos diferentes ambientes químicos de um organismo. Eles podem se acumular em tecidos não-alvo, ligam-se a outros componentes celulares ou podem não se internalizar de forma eficiente nas células-alvo.
p Os sistemas de entrega lipossomal visam mitigar esses problemas encapsulando drogas em portadores externos que circulam pela corrente sanguínea. Contudo, esses sistemas envolvem uma troca entre aumentar a estabilidade lipossomal no caminho para o alvo e facilitar a liberação de carga no citosol da célula alvo.
p A maioria das estratégias atuais de entrega de lipossomas dependem da via endossômica para a entrada na célula, que é inerentemente ineficiente e freqüentemente resulta na degradação da droga. Lípidos catiônicos comumente usados, que aumentam a fusão lipossomal com a membrana alvo e aumentam o escape endossomal, provou ser tóxico.
p "Pensamos que as porinas de nanotubos de carbono - pequenos pedaços de nanotubos de carbono inseridos em membranas lipídicas - podem imitar a funcionalidade do peptídeo de fusão viral e ajudar a fundir os transportadores lipossomais com as membranas das células cancerosas, "disse o cientista Alex Noy, que liderou a pesquisa no LLNL.
p Em uma série de experimentos, a equipe demonstrou que uma plataforma de nanomaterial simples - um dímero de porinas de nanotubos de carbono de pequeno diâmetro (CNTPs) - funciona como um potente promotor de fusão de membrana. Além disso, quando Noy e sua equipe carregaram seus lipossomas com um potente agente quimioterápico (doxorrubicina), esses transportadores entregaram a droga às células cancerosas, matando a maioria deles.
p "Nossos resultados abrem um caminho para transportadores de entrega de medicamentos simples e eficientes, compatíveis com uma ampla gama de terapêuticas, "disse Nga Ho, um pesquisador de pós-doutorado LLNL e o co-autor do artigo.
p Simulações dinâmicas moleculares de granulação grossa, realizado pela equipe da Max Planck, revelou um mecanismo de fusão distinto e incomum onde dímeros de CNTP amarram as vesículas, Puxe as membranas para a proximidade e então funda seus folhetos externos e internos.
p "Ficamos muito felizes em ver que a fusão da membrana facilitada por porinas de nanotubos de carbono de pequeno diâmetro pode levar à mistura completa do material da membrana e do conteúdo do interior da vesícula, "disse Marc Siggel, um estudante de graduação na Max Planck, e co-primeiro autor do estudo.
p "Nossos experimentos demonstram que os lipossomas cravejados de CNTP podem fornecer a base para a construção do desejado, mas até agora indescritível, portador versátil para entrega direta e altamente eficiente de medicamentos e vacinas de DNA e RNA através da membrana plasmática, "Noy disse.
p "Esta estratégia pode contornar a via endocitótica inteiramente e, assim, evitar alguns dos problemas encontrados por estratégias de entrega anteriores, "acrescentou Gerhard Hummer, um biofísico teórico do Instituto Max Planck, que liderou o esforço de modelagem.
