As microcápsulas desequilibradas liberam carga em pressões osmóticas mais baixas necessárias para a administração do medicamento
 p As microcápsulas com conchas de espessura variável (vermelho) podem encapsular a carga de forma estável e liberá-la quando calibrada com precisão, baixa pressão osmótica, permitindo a entrega segura de drogas e outras substâncias dentro do corpo humano. Crédito:Wyss Institute da Harvard University
p As microcápsulas com conchas de espessura variável (vermelho) podem encapsular a carga de forma estável e liberá-la quando calibrada com precisão, baixa pressão osmótica, permitindo a entrega segura de drogas e outras substâncias dentro do corpo humano. Crédito:Wyss Institute da Harvard University
p Quebrar um ovo para liberar sua gema requer a aplicação de força externa (como ser batido contra a borda de uma tigela) para superar a resistência da casca do ovo. De forma similar, entregar biomoléculas terapêuticas contidas em microcápsulas no corpo humano requer que seus recipientes sejam quebrados após serem injetados, para que a carga seja entregue no lugar certo na hora certa. Uma série de estímulos externos podem ser usados para desencadear a liberação de moléculas encapsuladas, uma das mais fáceis é a pressão osmótica, uma vez que simplesmente requer a introdução de água para fazer com que as microcápsulas inchem e estourem. Contudo, a fim de criar pressão interna suficiente para quebrar o invólucro da cápsula, grandes quantidades de um agente osmótico devem ser adicionadas à microcápsula para atrair a água, e a alta pressão de ruptura resultante pode danificar os tecidos ou causar coágulos sanguíneos. p Uma solução para este obstáculo foi agora desenvolvida por pesquisadores do Instituto Wyss de Engenharia Inspirada na Biologia de Harvard e da Escola de Engenharia e Ciências Aplicadas (SEAS) John A. Paulson, que inventou uma maneira de criar microcápsulas com cascas de espessura irregular que lhes permite estourar em pressões osmóticas mais baixas, tornando-os mais seguros para uso no corpo humano. A pesquisa é publicada em
Pequena .
p "A parte mais fraca de nossas cascas é 40 vezes mais fina do que a parte mais forte, o que torna muito mais fácil para eles quebrar e liberar sua carga, "disse o primeiro autor Weixia Zhang, Ph.D., um pós-doutorado no Wyss Institute e SEAS. "Por outro lado, essas microcápsulas são extremamente duráveis e não vazam se não forem expostas a pressão osmótica elevada, tornando-os muito estáveis e capazes de armazenar seu conteúdo por muito tempo. "
p Para fabricar suas microcápsulas não homogêneas, os pesquisadores usaram um dispositivo microfluídico capilar de vidro que empregou um método de água em óleo em água para encapsular uma solução de água contendo sacarose, um agente osmótico, dentro de uma concha de monômeros suspensos em óleo. Quando os monômeros são expostos à luz ultravioleta, eles reagem um com o outro e se reticulam para formar um sólido, concha de polímero em torno da solução de sacarose. Variando as taxas nas quais a solução de sacarose "carrega" e a "casca" do óleo monômero fluem através do dispositivo, a equipe descobriu que eles poderiam introduzir variações na espessura das cascas que se formaram, criando cápsulas assimétricas com paredes mais grossas de um lado e mais finas do outro.
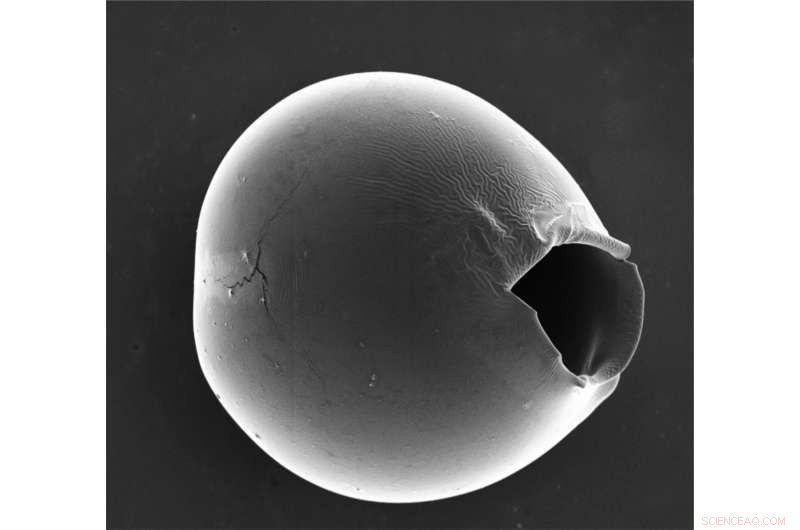 p As microcápsulas estouram na parte mais fina da casca, deixando uma abertura com dezenas de mícrons de tamanho que permite que a maioria das biomoléculas e drogas sejam liberadas. Crédito:Wyss Institute da Harvard University
p As microcápsulas estouram na parte mais fina da casca, deixando uma abertura com dezenas de mícrons de tamanho que permite que a maioria das biomoléculas e drogas sejam liberadas. Crédito:Wyss Institute da Harvard University
p Os pesquisadores então submeteram suas microcápsulas a choque osmótico com a adição de água, que se difundiu nas microcápsulas e as fez começar a inchar na parte mais fina da casca. Após cerca de 20-30 minutos, a casca fina rachou, formando uma abertura com dezenas de micrômetros de tamanho, que é grande o suficiente para que a maioria das biomoléculas e nanomateriais sejam liberados com sucesso. O aumento da diferença entre a parte mais fina e a mais espessa da casca levou a um maior número de microcápsulas estouradas, confirmando que o grau de não homogeneidade impactou a eficácia da liberação da carga.
p “Ser capaz de criar microcápsulas com alto grau de não homogeneidade alterando a espessura do casco durante o processo de fabricação e liberar a carga com pressão osmótica muito menor abre uma nova aplicação na liberação controlada, que é muito importante para a entrega de drogas na medicina, bem como outros campos, "disse o co-primeiro autor Liangliang Qu, Ph.D., um pós-doutorado no Wyss Institute e SEAS.
p Para testar a durabilidade das microcápsulas, a equipe encapsulou um polímero fluorescente dentro deles e mediu a mudança na intensidade fluorescente em seus núcleos ao longo do tempo. Eles não observaram nenhuma mudança na intensidade por 30 dias após o encapsulamento, demonstrando que as microcápsulas retiveram sua carga sem vazar. Além disso, o tamanho do polímero é muito menor do que a maioria das biomoléculas, como anticorpos e enzimas, sugerindo que as conchas poderiam ser usadas para proteger e armazenar biomoléculas ou drogas por longos períodos de tempo.
p Finalmente, os pesquisadores co-encapsularam uma protease (uma enzima que quebra as proteínas) e sacarose dentro de suas microcápsulas por 37 dias, então aplicou choque osmótico para desencadear a liberação de seu conteúdo. A protease reteve 91% de sua atividade original, demonstrando que este método de armazenamento não prejudicou significativamente sua função biológica.
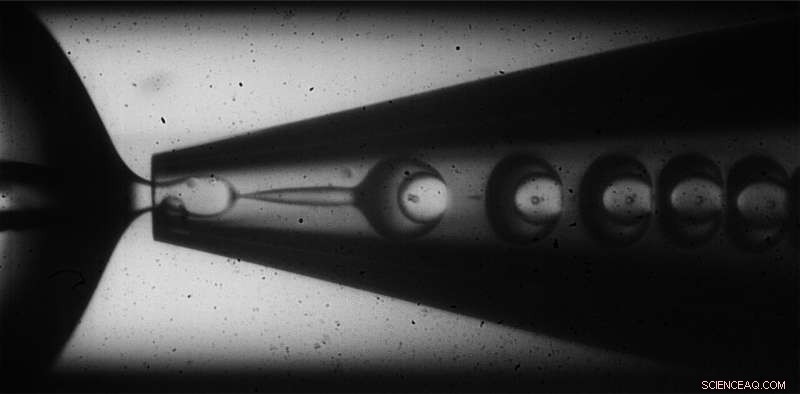 p As microcápsulas são criadas usando uma técnica de óleo em água em óleo que atinge uma espessura de casca não homogênea, variando as taxas de fluxo da casca e dos materiais de carga. Crédito:Wyss Institute da Harvard University
p As microcápsulas são criadas usando uma técnica de óleo em água em óleo que atinge uma espessura de casca não homogênea, variando as taxas de fluxo da casca e dos materiais de carga. Crédito:Wyss Institute da Harvard University
p "Em comparação com outras transportadoras de liberação controlada, como células, nanopartículas, ou vesículas, este sistema é altamente versátil, estábulo, e personalizável, tornando-o uma alternativa atraente para a distribuição segura e eficaz de drogas e outras biomoléculas para a saúde humana e outras aplicações, "disse o autor correspondente David Weitz, Ph.D., um membro do corpo docente do Instituto Wyss, que também é Professor Mallinckrodt de Física e Física Aplicada no SEAS.
p A equipe continua a desenvolver suas microcápsulas, otimizando o material da casca para diminuir ainda mais a pressão osmótica necessária para rompê-las. Eles planejam primeiro aplicar sua tecnologia para a entrega de medicamentos, como anticorpos terapêuticos, com o objetivo de ser capaz de usar o alto teor de água do corpo humano para atuar como o gatilho de ruptura após a injeção.
p "Este projeto é um ótimo exemplo de como as soluções mais simples muitas vezes podem ser melhores do que as complicadas, como a única entrada necessária para estourar as microcápsulas é a pressão mecânica, em vez de químicas complexas ou interruptores moleculares, "disse o co-autor Donald Ingber, M.D., Ph.D., quem é o Diretor Fundador do Wyss Institute, o professor Judah Folkman de Biologia Vascular no HMS e do Programa de Biologia Vascular no Hospital Infantil de Boston, e Professor de Bioengenharia do SEAS.


